
电浮选凝聚法处理酸性污水的工作原理如图所示。下列说法不正确的是
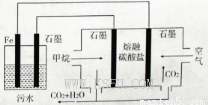
A.铁电极的电极反应式为:? 
B.通人空气的石墨电极的电极反应式为
C.若左池石墨电极产生44. 8L(标准状况)气体,则消耗氧气0. 5mol
D.为增强污水的导电能力,可向污水中加入适量工业用食盐
C
【解析】
试题分析:在甲烷燃料电池中,通入甲烷的一极为原电池的负极,发生氧化反应,电极方程式为CH4+ 4CO32--8e-═5CO2+2H2O,通入空气(氧气)的一极为原电池的正极,发生还原反应,电极方程式为O2+ 2CO2+4e-=2CO32-,铁连接原电池的正极,为电解池的阳极,被氧化,发生Fe-2e-=Fe2+,阴极生成2H++ 2e-=H2↑,A.铁连接原电池的正极,为电解池的阳极,被氧化,电极反应为Fe-2e-=Fe2+,正确; B.甲烷的一极为原电池的负极,发生氧化反应,电极方程式为CH4+4CO32--8e-═5CO2+2H2O,故正确; C.n(H2) =2mol.则电子转移4mol。由于在同一个闭合回路中的电子转移数目相等,所以结合原电池的电极反应式可确定消耗氧气1mol.错误。D.加入的使导电能力增强的电解质必须是可溶于水的、显中性的盐,可用食盐,故正确;
考点:考查本题综合考查原电池和电解池知识.


 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:高中化学 来源: 题型:
 (2009?湖北模拟)现有A、B、C、D四种元素,其原子序数依次递增.已知,A、C为短周期非金属元素,其单质在常温下均为气体,两单质混合见光爆炸生成AC,AC溶液显强酸性.B、D为金属元素,B的原子序数为D的一半,D与C2和AC溶液反应分别得DC3和DC2,烧碱溶液不能与D单质反应,而能与B单质反应.请回答下列问题:
(2009?湖北模拟)现有A、B、C、D四种元素,其原子序数依次递增.已知,A、C为短周期非金属元素,其单质在常温下均为气体,两单质混合见光爆炸生成AC,AC溶液显强酸性.B、D为金属元素,B的原子序数为D的一半,D与C2和AC溶液反应分别得DC3和DC2,烧碱溶液不能与D单质反应,而能与B单质反应.请回答下列问题:



查看答案和解析>>
科目:高中化学 来源:2012-2013学年福建省厦门市毕业班适应性考试理综化学试卷(解析版) 题型:选择题
电浮选凝聚法处理酸性污水的工作原理如图。下列说法不正确的是
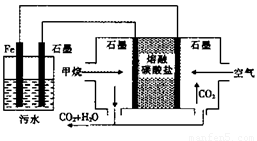
A.铁电极的电极反应式为:Fe—2e—=Fe2+
B.通人甲烷的石墨电极的电极反应式为:CH4+4CO32——8e—=5CO2+2H2O
C.为增强污水的导电能力,可向污水中加人适量工业用食盐
D.若左池石墨电极产生44.8 L气体,则消耗0. 5 mol甲烷
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
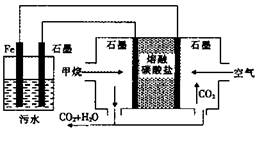
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com