
对于可逆反应2NO2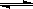 N2O4,下列状态一定是平衡状态的是
N2O4,下列状态一定是平衡状态的是
A.N2O4和NO2的分子数之比为1∶2
B.N2O4和NO2的浓度相等
C.体系中各组分的浓度不再变化
D.单位时间有1mol N2O4转变为NO2的同时,有1 mol NO2转变为N2O4
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:高中化学 来源: 题型:
A.对于有气体参与的平衡体系,若增大压强,使平衡向逆反应方向移动,则在新平衡前的逆反应速率大于正反应速率
B.对于气体的可逆反应,如果气体的平均相对分子质量保持不变时,则此可逆反应就达到了平衡状态
C.对于可逆反应达到平衡时,当增大反应物的浓度达到新的平衡时,则此反应物的转化率一定会提高
D.对于可逆反应:2NO2(g)![]() 2NO(g)+O2(g)达到平衡时,将各气体成分的浓度都增大一倍,则平衡向左移动
2NO(g)+O2(g)达到平衡时,将各气体成分的浓度都增大一倍,则平衡向左移动
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于平衡常数的说法正确的是( )
A.一定温度下的可逆反应,只有达到平衡时才具有平衡常数
B.改变外界条件使化学平衡状态改变时,平衡常数也一定改变
C.对于一个确定的反应来说,平衡常数的数值越大,反应限度越大
D.对于反应2NO2(g) ![]() N2O4(g)正反应的平衡常数为K1,逆反应的平衡常数为K2 ,K1 =K2
N2O4(g)正反应的平衡常数为K1,逆反应的平衡常数为K2 ,K1 =K2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com