
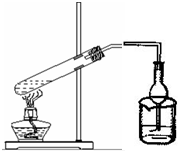
 如图(连接用的橡皮管省略未画出):在试管中依次加入2mL 95%的乙醇、2mL浓硫酸、2mL乙酸,将试管固定在铁架台上;在右边的50mL小烧杯中加入10mL饱和Na2CO3溶液.加热5min后在小烧杯中有油状、水果香味的液体产生.
如图(连接用的橡皮管省略未画出):在试管中依次加入2mL 95%的乙醇、2mL浓硫酸、2mL乙酸,将试管固定在铁架台上;在右边的50mL小烧杯中加入10mL饱和Na2CO3溶液.加热5min后在小烧杯中有油状、水果香味的液体产生.| 浓硫酸 |
| 加热 |
| 浓硫酸 |
| 加热 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
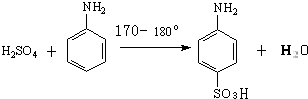
| 名称 | 性状 | 熔点/°C | 沸点/°C | 在水中的溶解度(g/100mL) |
| 苯胺 | 无色油状液体 | -6.1 | 184.4 | 3.6/18℃ |
| 对氨基苯磺酸 | 无色结晶 | 熔点365°C;内盐280~290°C | 0.8/10℃;1.08/20℃;6.67/100℃ | |


查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
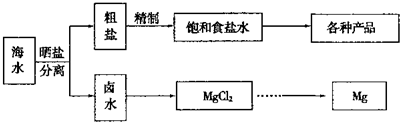
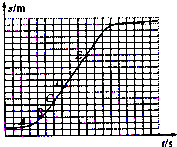
| ||
| ||
| ||
| ||
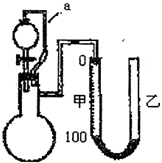
查看答案和解析>>
科目:高中化学 来源: 题型:
 测定1mol氧气在标准状况下所占体积的实验操作的步骤如下:①按如图装配实验装置.②洗净试管然后充分干燥.
测定1mol氧气在标准状况下所占体积的实验操作的步骤如下:①按如图装配实验装置.②洗净试管然后充分干燥.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com