
| A. | Cu和Zn | B. | Na和Ag | C. | Fe和Ca | D. | Cu和Ca |
分析 设金属为+2价,反应消耗金属的物质的量与氯气的物质的量相等,根据M=$\frac{m}{n}$计算出金属的平均摩尔质量,然后对各选项进行判断;注意+3价金属转化成+2价金属时的摩尔质量=原摩尔质量×$\frac{2}{3}$,+1价金属转化成+2价,其摩尔质量为原摩尔质量的2倍.
解答 解:7.1g氯气的物质的量为$\frac{7.1g}{71g/mol}$=0.1mol,
设金属为+2价,则金属的物质的量为0.1mol,混合金属的平均摩尔质量为:M=$\frac{5.6g}{0.1mol}$=56g/mol,
A.铜的摩尔质量为64g/mol,锌的摩尔质量为65g/mol,二者摩尔质量都大于56g/mol,无法满足平均摩尔质量为56g/mol,故A错误;
B.Na+2价时摩尔质量为:46g/mol,Ag+2价时摩尔质量为:216g/mol,二者的平均摩尔质量可以为56g/mol,故B正确;
C.铁的+2的摩尔质量为:56g/mol×$\frac{2}{3}$≈37.3g/mol,Ca为+2价的摩尔质量为:40g/mol,二者的摩尔质量都小于56g/mol,故C错误;
D.铜的摩尔质量为64g/mol,Ca为+2价的摩尔质量为:40g/mol,二者的平均摩尔质量可以为56g/mol,故D正确;
故选BD.
点评 本题考查了有关混合金属反应的化学计算,题目难度中等,注意掌握平均摩尔质量法在化学计算中的应用,试题侧重考查学生的分析、理解能力及化学计算能力.


 华东师大版一课一练系列答案
华东师大版一课一练系列答案科目:高中化学 来源: 题型:推断题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,加聚反应
,加聚反应查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该试剂的物质的量浓度为9.2 mol/L | |
| B. | 该硫酸50 mL若用5 mol/L的氢氧化钠中和,需要该氢氧化钠溶液100毫升 | |
| C. | 该硫酸与等体积的水混合所得溶液的质量分数等于49% | |
| D. | 配制200 mL 4.6 mol/L的稀硫酸需取该硫酸50 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 浓盐酸 | B. | Na2SO4浓溶液 | C. | NaOH浓溶液 | D. | Ba(OH)2浓溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将1mol明矾晶体完全溶于水制成胶体,其中所含胶体粒子数目为NA | |
| B. | 在反应KIO3+6HI=KI+3I2+3H2O中,每生成3molI2转移的电子数为5NA | |
| C. | 0.1 mol•Lˉ1 CaCl2溶液中含有Clˉ离子的数目为0.2NA | |
| D. | 136g熔融的KHSO4中含有2NA个阳离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 硫酸亚铁片 英文名:Ferrous Sulfate Tablets 本品含硫酸亚铁(FeSO4•7H2O)应为标示量的95.0%~110.0% | 氢氧化铝片 英文名:Aluminium Hydroxide Tablets |
| 【主要成分】糖衣、碳酸镁、氢氧化铝、淀粉 | |
| 【性状】本品为糖衣,除去糖衣后显淡绿色 | 【适应症】能缓解胃酸过多 |
| 【鉴别】取本品,除去糖衣,称取适量(约相当于硫酸亚铁片0.2g),加稀盐酸1滴与水20ml,振摇使硫酸亚铁溶解,过滤,滤液进行亚铁盐与硫酸盐的鉴别反应 | 【用法用量】成人:口服,一次0.6~0.9g(一次2~3片),一日3次,餐前1小时服用 |
| 【详细用法】详见说明书 |
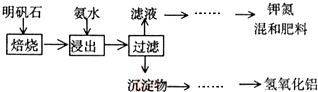
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
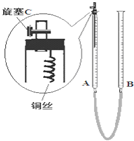 某实验小组同学探究铜与硝酸的反应.
某实验小组同学探究铜与硝酸的反应.| 序号 | 浓硝酸与水的体积比 | 实验现象 |
| Ⅰ | 1:1 | 反应速率快,溶液很快变成蓝色,大量气泡冒出,气体呈红棕色 |
| Ⅱ | 1:3 | 反应速率快,溶液变成蓝色,大量气泡冒出,气体呈无色 |
| Ⅲ | 1:5 | 反应速率慢,微热后加快,溶液变成蓝色,气泡冒出,气体无色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com