
科目:高中化学 来源: 题型:
下列关于元素周期表和元素周期律的说法错误的是
A.Li、Na、K元素的原子核外电子层数随着核电荷数的增加而增多
B.第二周期元素从Li到F,非金属性逐渐增强
C.因为Na比K容易失去电子,所以Na比K的还原性强
D.O与S为同主族元素,且O比S的非金属性强
查看答案和解析>>
科目:高中化学 来源: 题型:
四种短周期元素在周期表中的位置如图,其中只有M为金属元素。下列说法不正确的是
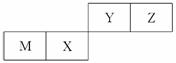
A.原子半径Z<M
B.Y的最高价氧化物对应水化物的酸性比X的弱
C.X的最简单气态氢化物的热稳定性比Z的小
D.Z位于元素周期表中第二周期、第ⅥA族
查看答案和解析>>
科目:高中化学 来源: 题型:
硫酸工业尾气中二氧化硫的含量超过0.05%(体积分数)时需经处理后才能排放。某校兴趣小组欲测定硫酸工业尾气中二氧化硫的含量,采用以下方案:
甲方案:如图所示,图中气体流量计B用于准确测量通过尾气的体积。将尾气通入一定体积已知浓度的碘水中测定SO2的含量。当洗气瓶C中溶液蓝色消失时,立即关闭活塞A。
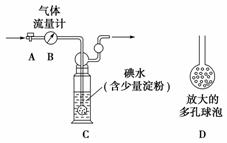
(1)洗气瓶C中导管末端连接一个多孔球泡D,可以提高实验的准确度,其理由是:_________________________。
(2)洗气瓶C中的溶液可以用其他试剂替代,请你举出一种:___________________________________________。
(3)洗气瓶C中溶液蓝色消失后,没有及时关闭活塞A,测得的SO2含量________(填“偏高”、“偏低”或“无影响”)。
乙方案:实验步骤如下面流程图所示:
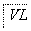
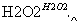

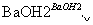
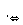
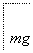
(4)写出步骤②中反应的化学方程式____________________________________________。
(5)步骤③中洗涤沉淀的方法是_________________________________________________。
(6)通过的尾气体积为V L(已换算成标准状况)时,该尾气中二氧化硫的含量(体积分数)为________(用含有V、m的代数式表示)。
丙方案:将乙方案中步骤①省略,直接将尾气通入过量Ba(OH)2溶液中,其余步骤与乙方案相同。
(7)你认为丙方案是否合理,说明理由:____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值,下列说法正确的是
A.常温常压下,22.4LH2含有NA个氢分子
B.标准状况下,22.4LH2O含有NA个水分子
C.1L1 mol/L的K2SO4溶液中,含NA个K+
D.23g钠在氧气中完全燃烧失去NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
海洋中蕴藏着丰富资源,对它的开发利用有利于缓解当前资源紧张的困局,工业上从海水中提取的某些无机物的简易流程可以用下图表示:
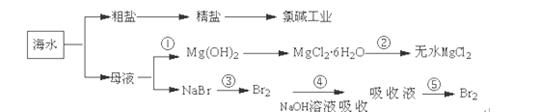
下列有关说法不正确的是
A.氯碱工业中采用阳离子交换膜电解槽,可以防止氯气与碱的反应
B.第②步中结晶出的MgCl2·6H2O不能采用直接在空气中受热分解制无水MgCl2
C.第①步常采用往母液中加浓NaOH溶液来获取Mg(OH)2
D.从第③步到第⑤步的目的是获得含溴单质浓度较高的溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
小明同学设计了如图所示装置来探究铜跟浓硫酸的反应。
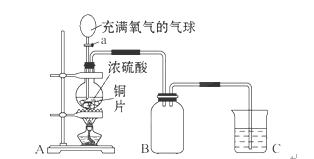
先关闭活塞a,加热至烧瓶中不再有气泡产生时,反应停止,此时烧瓶中铜片仍有剩余。再打开活塞a,将气球中的氧气缓缓挤入烧瓶,铜片慢慢减少。
(1)请写出上述过程A装置中所涉及的化学反应方程式。
______________________________________________;
______________________________________。
(2)张老师认为装置设计有误,你认为_________(填“A”、 “B”或“C”)部分有误。
(3)B中所收集到的气体既具有氧化性又具有还原性,请写出一个体现其还原性的化学方程式:________________________________________________。
(4)装置C的作用是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
1体积某气态烃只能与1体积氯化氢气体发生加成反应,生成氯代烷。1mol此氯代烷可与7mol氯气发生完全的取代反应,则该烃的结构简式为
A.CH2=CH2 B. CH3CH3 C. CH3CH=CH2 D.CH3CH2CH=CH2
查看答案和解析>>
科目:高中化学 来源: 题型:
NH3经一系列反应可以得到HNO3和NH4NO3,如下图所示。

(1)Ⅰ中,NH3和O2在催化剂作用下反应,其化学方程式是_________________________。
(2)Ⅱ中,2NO(g)+O2(g)  2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线(如图)。
2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线(如图)。
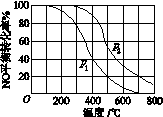
①比较p1、p2的大小关系:________。
②随温度升高,该反应平衡常数变化的趋势是________。
(3)Ⅲ中,降低温度,将NO2(g)转化为N2O4(l),再制备浓硝酸。
①已知:2NO2(g)  N2O4(g) ΔH1 2NO2(g)
N2O4(g) ΔH1 2NO2(g) N2O4(l) ΔH2
N2O4(l) ΔH2
下列能量变化示意图中,正确的是(选填字母)________。
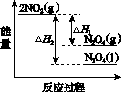
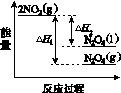

A B C
②N2O4与O2、H2O化合的化学方程式是________________________________________。
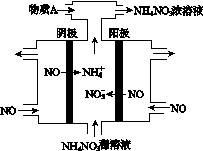
(4)Ⅳ中,电解NO制备NH4NO3,其工作原理如图所示。为使电解产物全部转化为NH4NO3,需补充A。A是________,说明理由:________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com