
A.铁和锌 B.镁和铜
C.铝和镁 D.锌和铁
B
解析:方法(1)—平均相对分子质量M
分析:设金属为+2价,则 X+2HCl![]() XCl2+H2↑
XCl2+H2↑
平均相对分子质量 ![]() g
g
M=
B中:相对分子质量Mg<41.6,Cu不反应 符合
C中:相对分子质量Mg<41.6,Al<41.6 不符合
D中:相对分子质量Zn>41.6,Fe>41.6不符合
方法(2)—平均电子摩尔质量—转移1 mol电子消耗金属的平均质量
因得到H
A中:转移1 mol电子消耗金属的质量Ca>
B中:转移1 mol电子消耗金属的质量Mg<
C中:转移1 mol电子消耗金属的质量Mg<
D中:转移1 mol电子消耗金属的质量Zn>


 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案科目:高中化学 来源:全程教与学 题型:013
今有两种金属的混合物粉末25g,投入足量的盐酸中,充分反应后得到11.2L![]() (标况),混合物可能的组成是
(标况),混合物可能的组成是
[ ]
|
①Zn和Ag |
②Ca和Zn |
③Mg和Fe |
|
|
④Mg和Cu |
⑤Zn和Fe |
||
|
A.② |
B.②③④ |
||
|
C.②③ |
D.①③⑤ |
||
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:022
查看答案和解析>>
科目:高中化学 来源: 题型:038
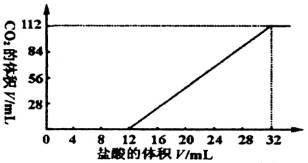
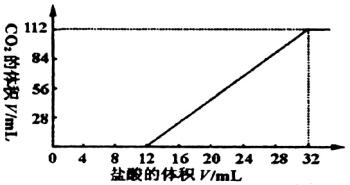
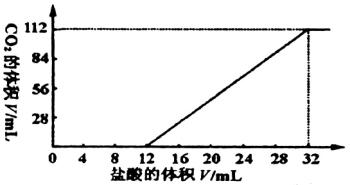
今有碱金属的两种碳酸盐和碱土金属(Mg、Ca等二价金属)的一种不溶性碳酸盐组成的混合物。取7.560 g该混合物与过量盐酸完全反应,放出CO2体积为1.344 L(标准状况)。另取等质量的原混合物加水搅拌,可滤出不溶性盐1.420 g。取过滤后滤液的![]() 体积,向其中缓慢滴加浓度为0.2500 mol/L的盐酸,并同时记录放出的CO2的体积(标准状况)和消耗盐酸的体积,得到如图所示的曲线。通过计算,确定这两种碱金属碳酸盐的化学式。
体积,向其中缓慢滴加浓度为0.2500 mol/L的盐酸,并同时记录放出的CO2的体积(标准状况)和消耗盐酸的体积,得到如图所示的曲线。通过计算,确定这两种碱金属碳酸盐的化学式。
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:038
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com