
药物贝诺酯可以水杨酸为原料在一定条件下反应制得,主要反应过程如下:
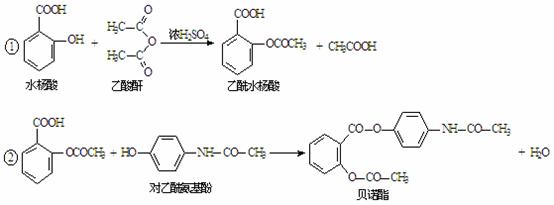
请回答下列问题:
(1)水杨酸的分子式为: ,它的含氧官能团分别名称为: 和 。
(2)1mol 水杨酸完全燃烧需要消耗 mol O2。
(3)水杨酸溶液中加入几滴FeCl3溶液,溶液显 色。
(4)反应①的反应类型为: ,请写出水杨酸与足量NaOH溶液反应的化学方程式: 。
(5)苯胺(C6H5—NH2)与乙酸酐在一定条件下发生类似①的反应,生成乙酰苯胺,试写出该反应的化学方程式: 。
科目:高中化学 来源: 题型:
下列关于晶体的说法一定正确的是
A.分子晶体中都存在共价键
B.CaTiO3晶体中每个Ti4+和12个O2-相紧邻
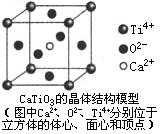
C.SiO2晶体中每个硅原子与两个氧原子以共价键相结合
D.金属晶体的熔点都比分子晶体的熔点高
查看答案和解析>>
科目:高中化学 来源: 题型:
水溶液中能大量共存的一组离子是
A.Ba2+、Na+、Cl-、OH- B.Fe2+、H+、SO42-、NO3-
C.Na+、Mg2+、Cl-、CO32- D.K+、Fe3+、NO3-、SCN-
查看答案和解析>>
科目:高中化学 来源: 题型:
乙酰水杨酸俗称阿司匹林,是一种历史悠久的解热镇痛热。合成原理是:
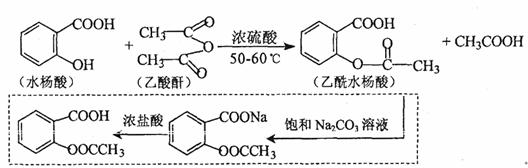
(1)水杨酸中含氧官能团的名称是 ,有关水杨酸的说法,正确的是 。
A.遇 FeCl3溶液可能显紫色 B.可发生酯化反应和水解反应
C.能与溴水发生取代反应和加成反应 D.1mol水杨酸最多能与3molH2发生加成反应
(2)水杨酸与乙酸酐反应的反应类型是 。
(3)乙酰水杨酸的分子式为 ,1mol乙酰水杨酸最多能与 molNaOH反应。
(4)虚框中为提纯,是为了除去该反应的副产物:水杨酸、乙酰水杨酸水杨酯、乙酰水杨酸酐和聚合物等,请写出乙酰水杨酸粗品中加入饱和Na2CO3溶液发生的主要化学反应方程式为:
。
(5)写出一种符合下列条件的乙酰水杨酸的同分异构体的结构简式: 。
Ⅰ.能遇FeCl3溶液显紫色 Ⅱ.苯环上只有一种一溴取代物
Ⅲ.能发生银镜反应 Ⅳ. 1mol该化合物能分别与1molNaOH和2mol金属钠反应
(6)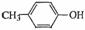 也能与乙酸酐发生类似反应,请写出化学反应方程式,可不写条件:
也能与乙酸酐发生类似反应,请写出化学反应方程式,可不写条件:
。
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏伽德罗常数的数值,下列叙述正确的是
A.已知N2(g)+3H2(g) 2NH3(g) ΔH=-92.4kJ/mol,在该反
2NH3(g) ΔH=-92.4kJ/mol,在该反
应中,当有3NA电子转移时,上述热化学反应方程式的焓变变为ΔH=
46.2kJ/mol
B.1 L 0.1mol·L-1碳酸钠溶液的阴离子总数等于0.1 NA
C.室温下pH=13的NaOH溶液中含有的OH-0.1 NA
D.浓度分别为1 mol·L-1 和 0.5mol·L-1的 CH3COOH和CH3COONa 混合液共1L,含CH3COOH 和 CH3COO-共1.5 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
早期发现的一种天然二十面体准晶颗粒由 Al、Cu、Fe 三种金属元素组成。回答下列问题:
(1) 准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过 方法区分晶体、准晶体和非晶体。
(2) 基态 Fe原子有 个未成对电子,Fe3+的电子排布式为 。可用硫氰化钾检验 Fe3+,形成配合物的配离子可表示为 。
(3) 新制备的 Cu(OH) 2 可将乙醛(CH3CHO)氧化为乙酸,而自身还原成 Cu2O,乙醛中碳原子的杂化轨道类型为 ,1mol 乙醛分子中含有的 键的数目为 , 乙酸的沸点明显高于乙醛,其主要原因是 。Cu2O 为半导体材料,在其立方晶胞内部有 4 个氧原子,其余氧原子位于面心和顶点,则该晶胞中有 个铜原子。
键的数目为 , 乙酸的沸点明显高于乙醛,其主要原因是 。Cu2O 为半导体材料,在其立方晶胞内部有 4 个氧原子,其余氧原子位于面心和顶点,则该晶胞中有 个铜原子。
(4) Al 单质为面心立方晶体,其晶胞边长 a=0.405nm,晶胞中铝原子的配位数为 。
列式表示 Al 单质的密度 g·cm-3(不必计算出结果)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com