
某苯的衍生物,含有两个互为对位的取代基,其分子式为C8H10O,其中不跟NaOH溶液反应的衍生物种类有:
A.2种 B.3种 C.4种 D.5种
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源:2014-2015湖南省娄底市高一上学期期末考试化学试卷(解析版) 题型:选择题
对I~IV的实验操作现象判断正确的是
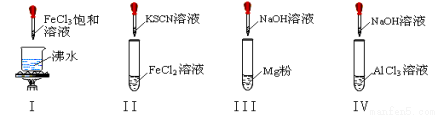
A.实验I:产生红褐色沉淀
B.实验II:溶液颜色变红
C.实验III:放出大量气体
D.实验IV:先出现白色沉淀,后沉淀又溶解
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省茂名市高三一模考试理综化学试卷(解析版) 题型:实验题
研究性学习小组利用下列有关装置进行探究实验,回答相关问题。

(1)写出A中的反应化学方程式
(2)实验时,旋开装置A中分液漏斗的旋塞,发现液体流出缓慢,最终停止,其可能的原因是 。
(3)装置B中的溶液出现浑浊,该实验证明SO2具有 性 。
(4)实验后,测定装置C中溶液呈碱性。溶液为什么呈碱性呢?大家有不同意见:①是生成的Na2SO3水解;②是氢氧化钠剩余。请设计实验方案证明哪种意见成立。选用下列试剂进行实验:Na2SO3溶液、酚酞溶液、氯水、BaCl2溶液、稀硫酸
实验步骤 | 实验操作 | 预期现象与结论 |
(5)另一小组利用装置D进行实验:用注射器向装置D共注入v mL实验室制备SO2的空气,当溶液刚好褪色,停止实验。
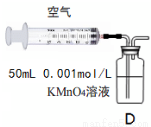
该小组的实验目的是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省部分普高高三2月联考化学试卷(解析版) 题型:填空题
(12分)某强酸性溶液X中仅含有Ba2+、Al3+、NH4+、Fe2+、Fe3+、CO32-、SO32-、SO42-、Cl-、NO3-中的一种或几种,取该溶液进行连续实验,实验过程如下:
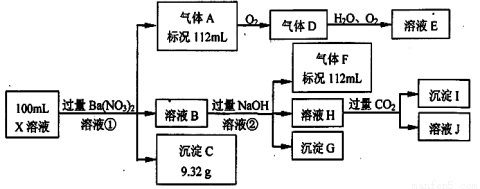
根据以上信息,回答下列问题:
(1)仅根据上述连续实验不能确定溶液X中是否含有的阳、阴离子分别是_____________。
(2)用离子方程表达下列反应:
①中生成气体A:___________ __。
②中生成溶液H:____________ _。
(3)若②中所用氢氧化钠浓度为2mol/L,当加入l0 ml时开始产生沉淀,55 ml时沉淀的量达到最大值0.03 mol,继续滴加沉淀的量保持不变,随后再滴加沉淀部分溶解,到60ml时沉淀的量降为0.025 mol且保持不变,则原溶液中c(Fe2+)为___________mol/L、c(Fe3+)为___________mol/L、c(Cl-)为___________mol/L。(若有些离子不存在,请填0 mol/L)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省部分普高高三2月联考化学试卷(解析版) 题型:选择题
中学常见物质A、B、C、D、E、X,存在下图转化关系(部分生成物和反应条件略去)。下列推断不正确的是:
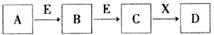
A.若D是一种白色沉淀,在空气中最终变为红褐色,则A可能是铁
B.若D是一种强碱,则A、B、C均可与X反应生成D
C.若D为NaCl,且A可与C反应生成B,则E可能是CO2
D.若D是一种强酸,则A既可以是单质,也可以是化合物,且D可与铜反应生成B或C
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省部分普高高三2月联考化学试卷(解析版) 题型:选择题
有五种饱和溶液①Ba(NO3)2 ②Ca(OH)2 ③NaAlO2 ④Na2CO3 ⑤NH3和NaCl,分别持续通入CO2,最终得到沉淀或析出晶体的是:
A.①②③④⑤ B.②③④⑤ C.③④⑤ D.③④
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省福州市高三第六次月考理综化学试卷(解析版) 题型:填空题
选考(13分)【有机化学基础】
A是一种重要的化工原料,已知A是一种卤代烃相对分子质量为92.5,其核磁共振氢谱中只有一个峰,C是一种高分子化合物,M是一种六元环状酯,转化关系如图所示,回答下列问题:

(1)A的分子式为 ;A→B的反应类型 ;
(2)有机物D的结构式为 。 M的结构简式为 。
(3)写出下列反应的化学方程式:
B→C: ;
E→F: 。
(4)写出满足下列条件的H的同分异构体d的结构简式 。
①属于酯类;
②能发生银镜反应;
③能与金属钠反应放出气体。
④核磁共振氢谱有三个峰,且峰面积比为6:1:1
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高三上学期期末考试化学试卷(解析版) 题型:选择题
TESLA电动汽车的电池采用了松下提供的NCA系列(镍钴铝体系)的18650A型钴酸锂(LiCoO2)锂离子电池。电池正极材料为钴酸锂(LiCoO2),负极材料是石墨(C6)。电池反应为: LiCoO2+C6 C6Lix+Li1-xCoO2。下列有关说法不正确的是
C6Lix+Li1-xCoO2。下列有关说法不正确的是
A.锂离子电池与传统铅蓄电池相比,具有高比能量(比能量指的是单位重量或单位体积的能量)的特点
B.废旧锂离子电池先进行“放电处理”让Li+进入石墨(C6)中而利于回收
C.放电时,正极锂的化合价未发生改变
D.充电时电池正极上发生的反应为:LiCoO2—x e-=== Li1-x CoO2+xLi+
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙、丙、丁为前三周期元素形成的微粒,它们的电子总数均为14.已知甲为原子;乙、丙、丁为双原子分子或离子。
(1)甲的原子结构示意图是 。
(2)乙是双原子分子,在高温时是一种还原剂。14 g乙燃烧放出的热量是141.5 kJ。
写出乙燃烧的热化学方程式 。
(3)丙为双原子二价阴离子,与钙离子组成的化合物能跟水反应产生一种可燃性气体,请写出该可燃性气体与氢气1:1加成后的产物发生加聚反应的方程式
。
(4)由丁分子组成的物质属于单质,组成丁的元素的最高价氧化物对应的水化物X有下图所示转化关系(反应条件和其他物质已略)

①已知W为常见金属单质,W在周期表中的位置 。写出X的稀溶液与Z反应的离子方程式 。
②X的浓溶液与W在加热条件下反应生成气体Q,已知Q受热发生可逆的分解反应,
1mol Q分解时,有2 mol电子转移。Q发生分解反应的化学方程式是
。将Q装入密闭容器中,加热到T ℃,达平衡时,测得密闭容器中气体压强是反应开始时的1.25倍。Q的分解率为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com