
甲、乙、丙、丁为前三周期元素形成的微粒,它们的电子总数均为14.已知甲为原子;乙、丙、丁为双原子分子或离子。
(1)甲的原子结构示意图是 。
(2)乙是双原子分子,在高温时是一种还原剂。14 g乙燃烧放出的热量是141.5 kJ。
写出乙燃烧的热化学方程式 。
(3)丙为双原子二价阴离子,与钙离子组成的化合物能跟水反应产生一种可燃性气体,请写出该可燃性气体与氢气1:1加成后的产物发生加聚反应的方程式
。
(4)由丁分子组成的物质属于单质,组成丁的元素的最高价氧化物对应的水化物X有下图所示转化关系(反应条件和其他物质已略)

①已知W为常见金属单质,W在周期表中的位置 。写出X的稀溶液与Z反应的离子方程式 。
②X的浓溶液与W在加热条件下反应生成气体Q,已知Q受热发生可逆的分解反应,
1mol Q分解时,有2 mol电子转移。Q发生分解反应的化学方程式是
。将Q装入密闭容器中,加热到T ℃,达平衡时,测得密闭容器中气体压强是反应开始时的1.25倍。Q的分解率为 。
科目:高中化学 来源:2014-2015学年甘肃省部分普高高三2月联考化学试卷(解析版) 题型:选择题
某苯的衍生物,含有两个互为对位的取代基,其分子式为C8H10O,其中不跟NaOH溶液反应的衍生物种类有:
A.2种 B.3种 C.4种 D.5种
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高三上学期期末考试化学试卷(解析版) 题型:选择题
25℃时,弱酸的电离平衡常数如表所示,下列说法正确的是
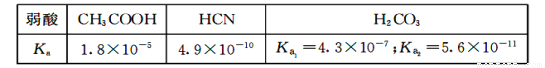
A.物质的量浓度相等的三种溶液中,pH大小关系为:pH(NaCN)> pH(Na2 CO3 )pH(CH3 COONa)
B.amol·L-1 HCN与b mol·L-1 NaOH溶液等体积混合所得的溶液中c(Na+)>c(CN-),则a一定小于b
C.向冰醋酸中逐滴加水稀释的过程中,溶液导电能力先增大,后减小
D.将0.1 mol·L-1的Na2 CO3溶液逐滴加入到等浓度的HCN溶液中,无明显现象,说明未反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验现象、解释与结论均正确的是
| 编号 | 实验操作 | 实验现象 | 解释与结论 |
| A | 铜与浓硝酸反应,生成气体用湿润KI-淀粉试纸检验 | 试纸变蓝 | NO2为酸性气体 |
| B | 向某溶液中加入稀盐酸酸化的BaCl2溶液 | 有白色沉淀产生 | 该沉淀是BaSO4,该溶液中只含有SO42- |
| C | 向甲苯中滴入少量浓溴水,振荡,静置 | 溶液分层,上层呈橙红色,下层几乎无色 | 甲苯和溴水发生取代反应,使溴水退色 |
| D | 在稀AgNO3溶液中先加入少量0.1mol·L-1 NaCl溶液,再加入少量0.1mol·L-1 NaI溶液 | 先产生白色沉淀,后出现黄色沉淀 | 说明Ksp(AgCl)>Ksp(AgI) |
查看答案和解析>>
科目:高中化学 来源: 题型:
A为药用有机物,从A出发可发生下图所示的一系列反应。已知A在一定条件下能跟醇发生酯化反应,A分子中苯环上的两个取代基连在相邻的碳原子上;D不能跟NaHCO3溶液反应,但能跟NaOH溶液反应。

请回答:
(1)A转化为B、C时,涉及到的反应类型有 _____、_______________。
(2)E的一种同分异构体Q能在一定条件下发生银镜反应,也能与Na反应放出H2Q结构简式为______。
(3)D的结构简式为__________________。
(4)已知:酰氯能与含有羟基的物质反应生成酯类物质。例如:
 写出草酰氯(分子式C2O2Cl2,
写出草酰氯(分子式C2O2Cl2,
分子结构式: )与足量有机物D反应的最终化学方程式
)与足量有机物D反应的最终化学方程式
_______________________________________________________________。
(5)已知:
由邻甲基苯酚——中间产物——有机物A,请选择正确中间产物(填B或C) ,并解释原因: 。
B: C:
C:
查看答案和解析>>
科目:高中化学 来源: 题型:
在其它条件不变时,10℃时以某物质表示的反应速率为3 mol•(L· s )-1 ,已知温度每升高10℃反应速率是原来的2倍,则温度为50℃时,该反应的速率为
A.48 mol•(L· s )-1 B.36 mol•(L· s )-1
C.24 mol•(L· s )-1 D.12 mol•(L· s )-1
查看答案和解析>>
科目:高中化学 来源: 题型:
在体积固定的密闭容器中N2 与H2发生反应:N2(g)+3H2(g)  2NH3(g) ,
2NH3(g) ,
达到平衡时c (N2)=3.5 mol·L-1 ,c (H2)=1 mol·L-1 ,c (NH3)=5 mol·L-1 ,求:
(1)N2和H2的起始浓度(4分)
(2)N2的转化率(2分)(要求有解题过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
高氯酸、硫酸、硝酸和盐酸都是强酸,其酸性在水溶液中差别不大。以下是某温度下这四种酸在冰醋酸中的电离常数:从下表格中判断下列说法正确的是
| 酸 | HClO4 | H2SO4 | HCl | HNO3 |
| Ka | 1.6×10-5 | 6.3×10-9 | 1.6×10-9 | 4.2×10-10 |
A.在冰醋酸和水中这四种酸都没有完全电离
B.在冰醋酸中高氯酸是这四种酸中最弱的酸
C.在冰醋酸中硫酸的电离方程式为H2SO4=2H++SO42-
D.水对于这四种酸的强弱没有区分能力,但醋酸可以区别这四种酸的强弱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com