
【题目】把0.6molX气体和0.4molY气体混合于2L容器中,使它们发生如下反应:3X(气)+Y(气)Z(气)+2W(气) 5min时达到平衡,且生成0.2molW 求
(1)5min内用W、Y表示的反应速率_______________
(2)平衡时,Y的转化率_____________.(Y的转化率=![]()
![]()
![]() )
)
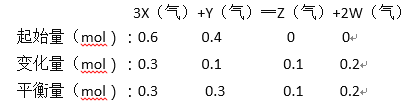
【答案】 3X(气)+Y(气)═Z(气)+2W(气)
起始量(mol):0.6 0.4 0 0
变化量(mol):0.3 0.1 0.1 0.2
平衡量(mol):0.3 0.3 0.1 0.2
v(W)= 0.2/(2×5) mol/(L.min)=0.02mol/(L.min) v(Y)= 0.1/(2×5) mol/(L.min)=0.01mol/(L.min) Y的转化率=![]() ×100%=25%
×100%=25%
【解析】试题分析:根据“三段”计算。
解析:
(1)v(W)= 0.2/(2×5) mol/(L.min)=0.02mol/(L.min)
v(Y)= 0.1/(2×5) mol/(L.min)=0.01mol/(L.min)
(2). Y的转化率=![]() ×100%=25%
×100%=25%


 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源: 题型:
【题目】I.根据下列叙述写出相应的热化学方程式:
(1)已知16 g固体硫完全燃烧时放出148.4 kJ的热量,该反应的热化学方程式是__________________________。
(2)下图是198 K时N2与H2反应过程中能量变化的曲线图。
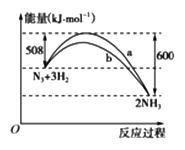
该反应的热化学方程式为:_____________________。
(3)甲硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态水。已知室温下1 g甲硅烷自燃放出热量44.6 kJ,其热化学方程式是___________________。
II.
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是_____________________。
A.C(s)+H2O(g)=CO(g)+H2(g) △H>0
B.NaOH(aq)+HC1(aq)=NaC1(aq)+H2O(1) △H<0
C.2H2(g)+O2(g)=2H2O(1) △H<0
(2)以KOH溶液为电解质溶液,依据所选反应设计一个原电池,其负极反应为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某气态烷烃和气态单烯烃组成的混合气体在同温同压下对氢气的相对密度为13,取标准状况下此混合气体4.48 L通入足量溴水中,溴水增重2.8 g,此两种烃是( )
A.甲烷和丙烯 B.乙烷和2丁烯
C.甲烷和2甲基丙烯 D.乙烯和1丁烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】炼油厂的废碱液含有废油、苯酚钠、碳酸钠等,实验室通过以下四个步骤处理废碱液获取氢氧化钠固体。下列说法正确的是

A. 用装置甲制取CO2并通入废碱液
B. 用装置乙从下口放出分液后上层的有机相
C. 用装置丙分离水相中加入Ca(OH)2产生的CaCO3
D. 用装置丁将滤液蒸发结晶得到NaOH固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】任何一个自发的氧化还原反应都可以设计成一个原电池。请根据:
Fe+CuSO4== Cu+FeSO4设计成一个原电池。
(1)该电池的负极材料为______,其电极反应为_______;
(2)正极材料为_____,电解质溶液为_____,其电极反应为___________________________。
(3)画出装置的简图,并注明正负极和电解质________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某有机物X的结构简式为 ,下列有关叙述不正确的是 ( )
,下列有关叙述不正确的是 ( )
A. 1 mol X分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别为3 mol、4 mol、1 mol
B. X在一定条件下能与FeCl3溶液发生显色反应
C. X在一定条件下能发生消去反应和酯化反应
D. X的化学式为C10H10O6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中,下列行为不符合安全要求的是
A. 在通风橱内制备有毒气体
B. 闻气体时,用手轻轻扇动使少量气体飘进鼻孔
C. 稀释浓硫酸时,将水注入浓硫酸中
D. 实验结束后,将废液倒入指定容器中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肼是一种强还原剂,用NaClO与NH3反应可用于生产肼(N2H4),其反应的化学方程式为:NaClO+2NH3= N2H4+NaCl+H2O。
⑴生产1000 g质量分数为25.6%的肼溶液最少需要___________L(标准状况)NH3。
⑵工业次氯酸钠溶液中含有氯酸钠会影响所得肼的产品质量。测定次氯酸钠样品中的氯酸钠含量的方法如下:取10.00 mL 碱性NaClO溶液试样,加入过量H2O2,将次氯酸钠完全还原(ClO3-在酸性条件下具有强氧化性,但碱性条件下几乎无氧化性),加热煮沸,冷却至室温,加入硫酸至酸性,再加入0.1000 mol·L-1 硫酸亚铁标准溶液30.00 mL,充分反应后,用0.01000 mol·L-1酸性K2Cr2O7溶液滴定至终点(Cr2O72-被还原为Cr3+),消耗该溶液20.00 mL。
①用H2O2与次氯酸钠反应的离子方程式为___________。
②实验中加热煮沸的目的是___________。
③计算样品中NaClO3的含量(以g·L-1表示),写出计算过程。___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化妆品的组分Z具有美白功效,原从杨树中提取,现可用如下反应制备:

下列叙述错误的是
A. X、Y和Z均能使溴水褪色
B. X和Z均能与NaHCO3溶液反应放出CO2
C. Y既能发生取代反应,也能发生加成反应
D. Y可作加聚反应单体,X可作缩聚反应单体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com