
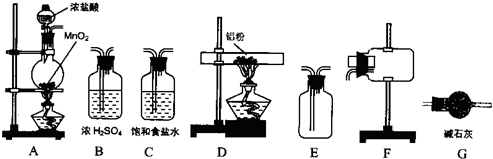
 MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:
(11分)某实验小组欲制取氧化铜并证明其能加快氯酸钾的分解,进行如下实验:
I.制取氧化铜
①称取2gCuSO4·5H2O研细后倒人烧杯,加10 mL蒸馏水溶解;
②向上述CuSO4溶液中逐滴加入NaOH溶液。直到不再产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀全部变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后研细备用。
回答下列问题:
(1)上述实验步骤中需要使用玻璃棒的是 (填实验序号),步骤①、③中研磨固体所用仪器的名称是 。
(2)步骤③中洗涤沉淀的操作是 。
Ⅱ.证明氧化铜能加快氯酸钾的分解并与二氧化锰的催化效果进行比较。实验时均以生成25 mL气体为准,其他可能影响实验的因素均已忽略,相关数据见下表:
| 实验序号 | KClO3质量 | 其他物质的质量 | 待测数据 |
| ④ | 1. 2g | 无其他物质 |
|
| ⑤ | 1. 2g | CuO 0.5g |
|
| ⑥ | 1. 2g | MnO2 0.5g |
|
回答下列问题:
(3)上述实验中的“待测数据”指 。
(4)若要证明实验中产生的气体是O2,可用小试管收集气体,后续操作为 。
(5)为探究CuO在实验⑤中是否起催化作用,需补做如下实验(无需写出具体操作):
a. 。b. CuO的化学性质有没有改变。
查看答案和解析>>
科目:高中化学 来源:湖北省武汉市部分重点中学2011届高三8月模拟考试化学试题 题型:实验题
(11分)某实验小组欲制取氧化铜并证明其能加快氯酸钾的分解,进行如下实验:
I.制取氧化铜
①称取2gCuSO4·5H2O研细后倒人烧杯,加10 mL蒸馏水溶解;
②向上述CuSO4溶液中逐滴加入NaOH 溶液。直到不再产生沉淀,然后将所得混合物转
溶液。直到不再产生沉淀,然后将所得混合物转 移到蒸发皿,加热至沉淀全部变为黑色;
移到蒸发皿,加热至沉淀全部变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后研细备用。
回答下列问题:
(1)上述实验步骤中需要使用玻璃棒的是 (填实验序号),步骤①、③中研磨固体所用仪器的名称是 。
(2)步骤③中洗涤沉淀的操作是 。
Ⅱ.证明氧化铜能加快氯酸钾的分解并与二氧化锰的催化效果进行比较。实验时均以生成25 mL气体为准,其他可能影响实验的因素均已忽略,相关数据见下表:
| 实验序号 | KClO3质量 | 其他物质的质量 | 待测数据 |
| ④ | 1. 2g 2g | 无其他物质 | |
| ⑤ | 1. 2g | Cu O 0.5g O 0.5g |  |
| ⑥ | 1. 2g | MnO2 0.5g | |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年广东省韶关市高三第二次模拟考试理综化学试卷(解析版) 题型:实验题
某化学兴趣小组在学习“硫酸盐的某些性质和用途”中,进行了如下实验探究:
【实验一】检验(NH4)2Fe(SO4)2·6H2O溶液中含有的阳离子。
(1)在下表中写出操作步骤和实验现象:
限选试剂:新制氯水、1mol/LH2SO4溶液、0.1mol/L KSCN溶液、NaOH浓溶液、浓盐酸、1mol/LNa2CO3溶液
|
操 作 步 骤 |
实验现象 |
结 论 |
|
步骤I:取少量待检液于试管中, 。 |
|
溶液中含有Fe2+ |
|
步骤II:取少量待检液于试管中, 。 |
|
溶液中含有NH4+ |
【实验二】用KHSO4制取H2O2并测其质量分数:
查阅资料得知:工业上用电解KHSO4饱和溶液可制取一定浓度的H2O2。兴趣小组进行下列实验测定H2O2的质量分数。已知:2MnO4-+5H2O2+6H+= 2Mn2++8H2O+5O2↑
操作①:取5.00 mL H2O2溶液(密度为1.00 g/mL)置于锥形瓶中加水稀释,再加稀硫酸酸化;
操作②:用0.1000 mol/L KMnO4溶液滴定;
操作③:用同样方法滴定,四次消耗KMnO4溶液的体积分别为20.00 mL、19.98 mL、20.02 mL、22.00 mL。
回答下列问题:
(2)操作②中,开始滴入KMnO4溶液时反应速率很慢,随着KMnO4溶液滴入反应速率显著加快,最有可能的原因______________________。
(3)滴定时盛装KMnO4溶液应选取的仪器是 (填序号)。
A.50mL酸式滴定管 B.50mL碱式滴定管
C.25mL酸式滴定管 D.25mL碱式滴定管
(4)在上述实验中,下列操作会造成测定结果偏高的有 (填序号)。
A.锥形瓶用待测液润洗
B.量取 H2O2溶液的滴定管用蒸馏水洗净,未用H2O2溶液润洗
C.滴定速度过快,又未摇匀,停止滴定后发现紫红色褪去
D.滴定前读数时平视,滴定终点读数时仰视
(5)分析数据,计算H2O2溶液中溶质的质量百分含量为___________(保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源:湖北省武汉市2010-2011学年高三8月模拟考试化学试题 题型:实验题
(11分)某实验小组欲制取氧化铜并证明其能加快氯酸钾的分解,进行如下实验:
I.制取氧化铜
①称取2gCuSO4·5H2O研细后倒人烧杯,加10 mL蒸馏水溶解;
②向上述CuSO4溶液中逐滴加入NaOH溶液。直到不再产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀全部变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后研细备用。
回答下列问题:
(1)上述实验步骤中需要使用玻璃棒的是 (填实验序号),步骤①、③中研磨固体所用仪器的名称是 。
(2)步骤③中洗涤沉淀的操作是 。
Ⅱ.证明氧化铜能加快氯酸钾的分解并与二氧化锰的催化效果进行比较。实验时均以生成25 mL气体为准,其他可能影响实验的因素均已忽略,相关数据见下表:
|
实验序号 |
KClO3质量 |
其他物质的质量 |
待测数据 |
|
④ |
1. 2g |
无其他物质 |
|
|
⑤ |
1. 2g |
CuO 0.5g |
|
|
⑥ |
1. 2g |
MnO2 0.5g |
|
回答下列问题:
(3)上述实验中的“待测数据”指 。
(4)若要证明实验中产生的气体是O2,可用小试管收集气体,后续操作为 。
(5)为探究CuO在实验⑤中是否起催化作用,需补做如下实验(无需写出具体操作):
a. 。b. CuO的化学性质有没有改变。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com