
【题目】某同学帮助水质检测站配制480 mL 0.5 mol/LNaOH溶液以备使用。
(1)该同学应用托盘天平称取NaOH固体_____g。
(2)用质量为23.1 g的烧杯放在托盘天平上称取所需NaOH固体时,请在附表中选取所需的砝码大小(填字母)__________,并在下图中选出能正确表示游码位置的选项(填字母) ____________。
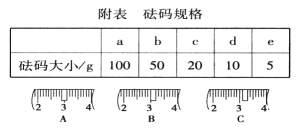
(3)配制时,正确的操作顺序是________
A.用30mL蒸馏水洗涤烧杯2-3次,洗涤液均注入容量瓶中,振荡
B.用天平准确称取所需的NaOH的质量,加入少量水,用玻璃棒慢慢搅动,使其充分溶解
C.将已冷却的氢氧化钠溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.改用胶头滴管滴加蒸馏水,使溶液凹液面恰好与刻度线相切
F.往容量瓶内加蒸馏水,直到溶液在刻度线下1~2cm处
(4)若出现以下情况,对所配溶液浓度将有何影响?(填"偏高""偏低"或"无影响")
①没有进行A操作__________
②转移溶液时不慎将少量的溶液洒在容量瓶外__________
③定容时俯视刻度线___________
【答案】10.0 cd c BCAFED 偏低 偏低 偏高
【解析】
(1)选取容量瓶的规格应该等于或稍大于配制溶液的体积;根据m=cVM计算所需的氢氧化钠的质量;
(2)氢氧化钠具有腐蚀性且易潮解,应放在烧杯内称量,根据氢氧化钠与烧杯质量确定需要的砝码;由表中升高可知,最小的砝码为5g,故游码的最大刻度为5g,故小于5g用游码.
(3)根据配制步骤是计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶来对操作顺序进行排序;
(4)根据c=n/V并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析;
(1)选取容量瓶的规格应该等于或稍大于配制溶液的体积,实验室没有480mL容量瓶,所以应该选500mL容量瓶;
配制500mL0.5mol·L-1NaOH溶液需要氢氧化钠的质量为0.5L×0.5mol·L-1×40g·mol-1=10.0g;
(2)氢氧化钠具有腐蚀性且易潮解,应放在烧杯内称量,根据氢氧化钠与烧杯总质量为10.0g+23.1g=33.1g,故应选择20g与10g的砝码,即选择cd;
由表中升高可知,最小的砝码为5g,故游码的最大刻度为5g,故小于5g所以游码,所以游码应在3.1g的位置,故选择C;
(3)根据配制步骤是计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶可知正确的操作顺序是:B、C、A、F、E、D;
(4)若出现以下情况,对所配溶液浓度将有何影响?(填"偏高""偏低"或"无影响")
①没有进行A操作:有少量NaOH溶液残留在烧杯内,会导致溶质的损失,则浓度偏低;
②转移溶液时不慎将少量的溶液洒在容量瓶外,会导致溶质的损失,则浓度偏低;
③定容时俯视刻度线,则导致溶液体积偏小,浓度偏高。


科目:高中化学 来源: 题型:
【题目】锌锰干电池的负极是作为电池壳体的金属锌,正极是被二氧化锰和碳粉包围的石墨电极,电解质是氯化锌和氯化铵的糊状物,该电池放电过程中产生 MnOOH。废旧电池中的Zn、Mn元素的回收,对环境保护有重要的意义。
Ⅰ. 回收锌元素,制备ZnCl2
步骤一:向除去壳体及石墨电极的黑色糊状物中加水,搅拌,充分溶解,经过滤分离得固体和滤液。
步骤二:处理滤液,得到ZnCl2·xH2O晶体。
步骤三:将SOCl2与ZnCl2·xH2O晶体混合制取无水ZnCl2。
制取无水ZnCl2,回收剩余的SOCl2并验证生成物中含有SO2(夹持及加热装置略) 的装置如下:

(已知: SOCl2是一种常用的脱水剂,熔点-105℃,沸点79℃,140℃以上时易分解,与水剧烈水解生成两种气体。)
(1)写出SOCl2与水反应的化学方程式:______________________。
(2)接口的连接顺序为a→___→___→ h → h →___→___→___→e。______________
Ⅱ. 回收锰元素,制备MnO2
(3)洗涤步骤一得到的固体,判断固体洗涤干净的方法:_________________________。
(4)洗涤后的固体经初步蒸干后进行灼烧,灼烧的目的__________________________。
Ⅲ. 二氧化锰纯度的测定
称取1.40g灼烧后的产品,加入2.68g草酸钠(Na2C2O4)固体,再加入足量的稀硫酸并加热(杂质不参与反应),充分反应后冷却,将所得溶液转移到100mL容量瓶中用蒸馏水稀释至刻线,从中取出20.00mL,用0.0200mol/L高锰酸钾溶液进行滴定,滴定三次,消耗高锰酸钾溶液体积的平均值为17.30mL。
(5)写出MnO2溶解反应的离子方程__________________________________________。
(6)产品的纯度为______________________ 。
(7)若灼烧不充分,滴定时消耗高锰酸钾溶液体积_____(填“偏大”、“ 偏小”、“ 不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对金属制品进行抗腐蚀处理,可延长其使用寿命。
(1)以下为铝材表面处理的一种方法:

①碱洗的目的是洗去铝材表面的自然氧化膜,碱洗时候常有气泡冒出,原因是(用离子方程式表示)_____。为将碱洗槽液中的铝以沉淀形式回收,最好向槽液中加入下列试剂中的____。
a.NH3 b.CO2 c.NaOH d.HNO3
②以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应式为 _________。
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨做阳极的原因是________。
(3)利用图装置,可以模拟铁的电化学防护。

若X为碳棒,为减缓铁的腐蚀,开关K应该置于____处(填“M”或“N”);若X为锌,开关K置于M处,该电化学防护法称为_______。
(4)已知:H2O2是弱酸,在碱性条件下以HO2-存在。目前研究比较热门的Al-H2O2燃料电池,其原理如下图所示:

电池总反应如下:2Al+3HO2-=2AlO2-+OH-+H2O 。写出负极反应式为_______;写出正极反应式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废旧电池的回收处理,既能减少对环境的污染,又能实现资源的再生利用。将废旧锌锰电池初步处理后,所得废料含MnO2、MnOOH、Zn(OH)2及少量Fe等,用该废料制备Zn和MnO2的一种工艺流程如下:

已知:
①Mn2+在酸性条件下比较稳定,pH高于5.5时易被O2氧化
②有关Ksp数据如下表所示
化合物 | Mn(OH)2 | Zn(OH)2 | Fe(OH)3 |
Ksp近似值 | 10-13 | 10-17 | 10-38 |
回答下列问题:
(1)还原焙烧过程中, MnOOH与炭黑反应,锰元素被还原为MnO,该反应的化学方程式为___________。传统的工艺是使用浓盐酸在加热条件下直接处理废料,缺点是___________。
(2)酸漫时一般会适当加热并不断搅拌,其作用是___________,滤渣1和滤渣2主要成分的化学式依次是___________。
(3)净化时,先通入O2再加入MnCO3,其目的是___________;已知净化时溶液中Mn2+、Zn2+的浓度约为0.1mol·L-1,调节pH的合理范围是___________。
(4)电解制取MnO2时,MnO2在___________极产生。
(5)中科院研究人员将MnO2和生物质置于一个由滤纸制成的折纸通道内形成电池,该电池可将软饮料中的葡萄糖作为燃料获得能量,装置如图所示。此装置中b极的电极反应式为______________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是某些姜科植物根茎的提取物,具有抗肿瘤、抗菌、抗氧化等功效,其一种合成路线如下:

已知:i 质谱图显示有机物D的最大质荷比为94,且D遇FeCl3溶液显紫色
ii RMgBr+R′CHO→![]()
回答下列问题:
(1)D的化学式为___________;B的名称为___________。
(2)反应①的反应类型是___________:I中所含官能团的名称为___________。
(3)反应④的化学方程式是______________________。
(4)X是H的同系物,其相对分子质量比H小14,则X的同分异构体中,符合下列条件的有___________种(不含立体异构)
a.属于芳香族化合物 b.能发生水解反应 c.能发生银镜反应
其中核磁共振氢谱有4组峰,且峰面积之比为6:2:1:1的结构简式是___________(写一种即可)。
(5)补充完成由甲苯和丙醛为原料,制备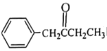 的合成路线(无机试剂任选)
的合成路线(无机试剂任选) ____________
____________ 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业采用氯化铵焙烧菱锰矿制备高纯碳酸锰的流程如图所示:

已知:①菱锰矿的主要成分是MnCO3,其中含Fe、Ca、Mg、Al等元素。
②Al3+、Fe3+沉淀完全的pH分别为4.7、3.2,Mn2+、Mg2+开始沉淀的pH分别为8.1、9.1。
③焙烧过程中主要反应为MnCO3+2NH4Cl![]() MnCl2+2NH3↑+CO2↑+H2O。
MnCl2+2NH3↑+CO2↑+H2O。
(1)结合图1、2、3,分析焙烧过程中最佳的焙烧温度、焙烧时间、![]() 分别为_____、_____、_______。
分别为_____、_____、_______。

(2)对浸出液净化除杂时,需先加入MnO2将Fe2+转化为Fe3+,再调节溶液pH的范围为_______,将Fe3+和Al3+变为沉淀而除去,然后加入NH4F将Ca2+、Mg2+变为氟化物沉淀除去。
(3)“碳化结晶”步骤中,加入碳酸氢铵时反应的离子方程式为______________。
(4)上述流程中可循环使用的物质是________。
(5)现用滴定法测定浸出液中Mn2+的含量。实验步骤:称取1.000 g试样,向其中加入稍过量的磷酸和硝酸,加热使反应2Mn2++![]() +4
+4![]() +2H+
+2H+![]() 2[Mn(PO4)2]3+
2[Mn(PO4)2]3+![]() +H2O充分进行;加入稍过量的硫酸铵,发生反应
+H2O充分进行;加入稍过量的硫酸铵,发生反应![]() +
+![]()
![]() N2↑+2H2O以除去
N2↑+2H2O以除去![]() ;加入稀硫酸酸化,用2.00 mol·L110.00 mL硫酸亚铁铵标准溶液进行滴定,发生的反应为[Mn(PO4)2]3+Fe2+
;加入稀硫酸酸化,用2.00 mol·L110.00 mL硫酸亚铁铵标准溶液进行滴定,发生的反应为[Mn(PO4)2]3+Fe2+![]() Mn2++ Fe3++2
Mn2++ Fe3++2![]() ;用0.10 mol·L110.00 mL酸性K2Cr2O7溶液恰好除去过量的Fe2+。
;用0.10 mol·L110.00 mL酸性K2Cr2O7溶液恰好除去过量的Fe2+。
①酸性K2Cr2O7溶液与Fe2+反应的离子方程式为_____________(还原产物是Cr3+)。
②试样中锰的质量分数为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下述实验不能达到预期实验目的是( )
序号 | 实验内容 | 实验目的 |
A | 将2.5gCuSO4.5H2O溶解在97.5g水中 | 配制质量分数为1.6%的CuSO4溶液 |
B | 向盛有1mL硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶液 | 说明一种沉淀能转化为另一种溶解度更小的沉淀 |
C | 室温下,用pH试纸测定浓度为0.1mol.L-1NaClO溶液和0.1mol?L-1CH3COONa溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
D | 室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入相同体积不同浓度的稀硫酸 | 研究浓度对反应速率的影响 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知化学反应A2(g)+B2(g)===2AB(g)的能量变化如图所示,判断下列叙述中正确的是

A. 每生成2分子AB吸收b kJ热量
B. 该反应热ΔH=+(a-b) kJ·mol-1
C. 该反应中反应物的总能量高于生成物的总能量
D. 断裂1 mol A—A和1 mol B—B键,放出a kJ能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸氢钠俗称“小苏打”,在生活、生产中用途广泛。
(1)泡沫灭火器中主要成分是NaHCO3溶液和Al2(SO4)3溶液,两者混合后发生双水解反应生成Al(OH)3和CO2进行灭火,写出该反应的化学方程式_________________________________________________。
(2)Na2O2和NaHCO3都属于钠的化合物,它具有很强的氧化性。少量Na2O2与FeCl2溶液能发生如下反应:____Na2O2+____FeCl2+____H2O→____Fe(OH)3![]() +____FeCl3+____NaCl,已知FeCl2前面系数为6,配平上述化学方程式______,并标出电子转移方向和数目______。该反应中被还原的元素是_________,氧化产物是_________。
+____FeCl3+____NaCl,已知FeCl2前面系数为6,配平上述化学方程式______,并标出电子转移方向和数目______。该反应中被还原的元素是_________,氧化产物是_________。
(3)向NaHCO3溶液中加入少许Ba(OH)2固体,忽略溶液体积变化,溶液中的c(CO32-)的变化是_____(选填“增大”、“减小”或“不变”)。
(4)NaHCO3是氨碱法和联合制碱法制纯碱的中间产物,在滤出小苏打后,母液提取氯化铵有两种方法:①通入氨,冷却、加食盐,过滤 ②不通入氨,冷却、加食盐,过滤对两种方法的评价正确的是______(选填编号)。
a.①析出的氯化铵纯度更高 b.②析出的氯化铵纯度更高
c.①的滤液可直接循环使用 d.②的滤液可直接循环使用
(5)已知HCO3-在水中既能水解也能电离。NaHCO3溶液呈碱性,溶液中c(H2CO3)___c(CO32-)(选填“>”、“<”、“=”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com