
【题目】SO2能使品红溶液褪色,体现了SO2的( )
A.酸性氧化物的性质
B.漂白性
C.氧化性
D.还原性
科目:高中化学 来源: 题型:
【题目】A、B、C为短周期元素,在周期表中所处的位置如图所示。
A | C | |
B |
A、C两元素的原子核外电子数之和等于B原子的质子数。
(1)写出A、B元素的名称 、 。
(2)B位于元素周期表中第 周期第 族。
(3)C的原子结构示意图为 。
(4)写出A的气态氢化物与其最高价氧化物对应的水化物反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国女科学家屠呦呦因为发现青蒿素获颁诺贝尔医学奖。右图是青蒿素的结构,则有关青蒿素的说法中不正确的是
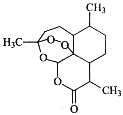
A.有“—O—”键,分子式C15H22O5,可发生取代反应
B.有“六元环”结构,是苯的同系物,可发生加成反应
C.有“—O—O—”键,氧化性较强,可发生还原反应
D.有“—COO—”键,碱性条件下,可发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子,能在溶液中大量共存的是( )
A.H+、K+、OH﹣
B.H+、Cl﹣、CO32﹣
C.Ba+、Na+、SO42﹣
D.Na+、Cu2+、Cl﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是

A.该反应的化学方程式为3B+2D 6A+4C
B.反应进行到1 s时,v(A)=3v(D)
C.反应进行到6 s时,B的平均反应速率为0.1mol/(Ls)
D.反应进行到6 s时,各物质的反应速率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】日常生活中使用的购物袋的材料多为聚乙烯,下列说法中正确的是
A.用纯净的乙烯合成的聚乙烯是纯净物
B.聚乙烯可以人工合成,也可以是天然高分子化合物
C.聚乙烯能使酸性高锰酸钾溶液褪色
D.聚乙烯的单体能够使溴的四氯化碳溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过粮食发酵可获得某有机化合物X,其相对分子质量为46,其中碳的质量分数为52.2%,氢的质量分数为13.0%。
(1)X的分子式是_______;
(2)X与金属钠反应放出H2,反应化学方程式是_______(有机物用结构简式表达);
(3)X与空气中的氧气在铜或银催化下反应生成Y,Y的结构简式是______________;
(4)X与高锰酸钾酸性溶液反应可生成Z。在加热和浓硫酸作用下,X与Z反应可生成一种无色具有水果香味的液体W,装置如图所示:
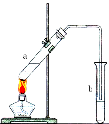
①生成液体W的化学方程式为 ;
②为了防止a中液体暴沸,加热前应采取的措施是 ;
③b试管中导管不能伸入到液面以下的理由是 ;
④试管b中加有饱和Na2CO3溶液,其作用是 ;
⑤若184 g X和120 g Z反应能生成106 g W,则该反应的产率为 。
(已知 ![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某市场销售的某种食用精制盐包装袋上有如下说明:
产品标准 | GB5461 |
产品等级 | 一级 |
配料 | 食盐、碘酸钾、抗结剂 |
碘含量(以I计) | 20~50 mg/kg |
分装日期 | |
分装企业 |
(1)I2可用四氯化碳检验。向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。
①Na2SO3稀溶液与I2反应的离子方程式是:________________________________________________。
②某学生设计回收四氯化碳的操作步骤为:
a.将碘的四氯化碳溶液置于分液漏斗中;
b.加入适量Na2SO3稀溶液;
c.分离出下层液体。
以上设计中遗漏的操作及在上述步骤中的位置是____________________________________________。
(2)已知:I2+2S2O32-===2I-+S4O62-。
某学生测定食用精制盐的碘含量,其步骤为:
a.准确称取w g食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉溶液为指示剂,逐滴加入物质的量浓度为2.0×10-3 mol·L-1的Na2S2O3溶液10.0 mL,恰好反应完全。
①判断c中反应恰好完全依据的现象是________________________。
②b中反应所产生的I2的物质的量是______________mol。
③根据以上实验和包装袋说明,所测精制盐的碘含量是(以含w的代数式表示)____________mg/kg。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com