
.除去下列物质中的杂质,所用试剂和方法不正确的是
| 物质 | 杂质 | 除杂质所用试剂和方法 |
A | KCl溶液 | I2 | CCl4,萃取 |
B | KNO3 | K2SO4 | Ba(NO3)2溶液,过滤 |
C | Cu | CuO | 盐酸,过滤 |
D | CaCO3 | CaO | 盐酸,过滤 |
科目:高中化学 来源:2014-2015学年北京市高一上第一次质量检测化学试卷(解析版) 题型:实验题
某同学配制1000mL 1.00mol/L NaCl溶液的步骤如下:
①用托盘天平称取58.5g NaCl固体并全部移入烧杯中;
②在上述烧杯中加入适量的蒸馏水,搅拌至NaCl固体全部溶解,冷却至室温;
③将烧杯中的溶液倾倒至容量瓶中;
④将蒸馏水注入容量瓶至刻度线下1cm~2cm;
⑤用胶头滴管滴加蒸馏水至液面与刻度线相切;
⑥盖好瓶塞,反复上下颠倒摇匀;
⑦静置后因液面低于刻度线再用胶头滴管滴加蒸馏水至液面与刻度线相切。
你认为上述步骤中不合理或不正确的是 (填写序号)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省玉溪市高二上学期期中考试化学试卷(解析版) 题型:选择题
在反应aA+bB cC的平衡体系中,无论升高温度或增加压强,C的浓度都会增大,则以下说法正确的是
cC的平衡体系中,无论升高温度或增加压强,C的浓度都会增大,则以下说法正确的是
A.a+b<c 正反应吸热 B.a+b>c 正反应吸热
C.a+b>c 正反应放热 D.无法确定系数关系 正反应吸热
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省玉溪市高一上学期期中化学试卷(解析版) 题型:选择题
若以ω1和ω2分别表示浓度为a mol/L和b mol/L氨水的质量分数,且知2a=b,则下列推断正确的是(氨水的密度比纯水的小)
A.2ω1 = ω2 B.2ω2 = ω1 C.ω2﹥2ω1 D.2ω1﹥ω2﹥ω1
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省玉溪市高一上学期期中化学试卷(解析版) 题型:选择题
在一定条件下,某化合物Χ受热分【解析】
2Χ=A↑+2B↑+4C↑。在相同条件下测得反应后生成的混合气体对H2的相对密度为11.43,Χ的相对分子质量是
A.11.43 B.22.85 C.80.01 D.160.02
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省玉溪市高一上学期期中化学试卷(解析版) 题型:选择题
将5mol/L的Mg(NO3)2溶液a mol稀释至b mol,稀释后溶液中NO3—的物质的量浓度为
A.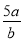 mol/L B.
mol/L B.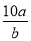 mol/L C.
mol/L C.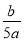 mol/L D.
mol/L D.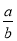 mol/L
mol/L
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省玉溪市高一上学期期中化学试卷(解析版) 题型:选择题
用NA表示阿伏德罗常数,下列叙述正确的是
A.标准状况下,4.48L H2O中所含的原子总数为0.6NA
B.常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA
C.通常状况下,NA 个CO2分子占有的体积为22.4L
D.物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl- 个数为 NA
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市闵行区八校高二上学期期中联考化学试卷(解析版) 题型:选择题
工业生产中常将两种或多种金属(或金属与非金属)在同一容器中加热使其熔合,冷凝后得到具有金属特性的熔合物——合金。这是制取合金的常用方法之一。仅根据下表数据判断,不宜用上述方法制取的合金是
金属 | Na | K | Al | Cu | Fe |
熔点(℃) | 97.5 | 63.6 | 660 | 1083 | 1535 |
沸点(℃) | 883 | 774 | 2467 | 2567 | 2750 |
A.Fe—Cu合金 B.Cu—Al合金
C.Al—Na合金 D.Cu—Na合金
查看答案和解析>>
科目:高中化学 来源:2014-2015吉林省松原市高二上学期期中化学试卷(解析版) 题型:填空题
(14分)
 (1)物质的量浓度均为0.1 mol/L的下列溶液:①NH4Cl、②Na2CO3、③NaHCO3、④NaHSO4、⑤CH3COOH、⑥NaOH,pH由大到小的顺为: (填数字代号)
(1)物质的量浓度均为0.1 mol/L的下列溶液:①NH4Cl、②Na2CO3、③NaHCO3、④NaHSO4、⑤CH3COOH、⑥NaOH,pH由大到小的顺为: (填数字代号)
(2)氢气燃烧热值高。实验测得,在常温常压下,1 g H2完全燃烧生成液态水,放出142.9 kJ热量。则H2燃烧的热化学方程式为 __________________________________。
(3)常温下,0.1 mol/L的NaHCO3溶液的pH大于8,则溶液中H2CO3____ CO32-(填>、=或<),原因________________________(用离子方程式和必要的文字说明)
(4)常温下,pH=a某强酸溶液V1 L,pH=b某强碱溶液V2 L,已知a+b=12,两溶液混合后pH=7,求V1 和V2的关系
(5)25℃下,某Na2SO4溶液中c(SO42-)=5×10-4 mol·L-1,取该溶液1 mL,加水稀释至10 mL,则稀释后溶液中c (Na+)∶c (OH-)=________
(6)常温下,已知Ksp(Mg(OH)2)=1.8×10-11,则Mg(OH)2在pH=12.00的NaOH溶液中的Mg2+浓度为 mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com