
【题目】已知下列热化学方程式: ①Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H1=﹣26.7kJmol﹣1
②3Fe2O3(s)+CO(g)═2Fe3O4(s)+CO2(g)△H2=﹣50.75kJmol﹣1
③Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H3=﹣36.5kJmol﹣1
则反应FeO(s)+CO(g)═Fe(s)+CO2(g)的焓变为( )
A.+7.28 kJmol﹣1
B.﹣7.28 kJmol﹣1
C.+43.68 kJmol﹣1
D.﹣43.68 kJmol﹣1
科目:高中化学 来源: 题型:
【题目】材料是人类赖以生存的物质基础. ①制造水泥、玻璃都要用到的原料是(填字母).
a.石灰石 b.纯碱 c.黏土
②不锈钢丝与棉纤维可织成一种防辐射布料.这种布料属于(填字母).
a.合金材料b.复合材料 c.陶瓷材料
③天然橡胶的结构简式是(填字母).
a. ![]() b.
b. ![]() c.
c. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是由短周期元素组成的一些单质及其化合物之间的转化关系图.常温常压下D、F、K均为无色无刺激气味的气体,B是常见的无色液体,A是由单质C在D中燃烧产生的淡黄色的固体.(反应中部分生成物质己略去) 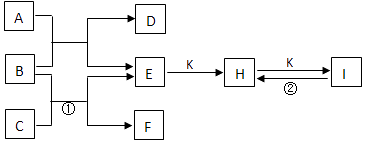
请回答下列问题:
(1)物质A的化学式为 .
(2)实验室C的保存方法 .
(3)反应①的离子方程式为 .
(4)反应②的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.乳酸薄荷醇酯( ![]() )仅能发生水解、氧化、消去反应
)仅能发生水解、氧化、消去反应
B.乙醛和丙烯醛( ![]() )不是同系物,它们与氢气充分反应后的产物也不是同系物
)不是同系物,它们与氢气充分反应后的产物也不是同系物
C.淀粉和纤维素在酸催化下完全水解后的产物都是葡萄糖
D.CH3COOCH2CH3与CH3CH2COOCH3互为同分异构体,1H﹣NMR谱显示两者均有三种不同的氢原子且三种氢原子的比例相同,故不能用1H﹣NMR来鉴别
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知化学反应:C(s)+ ![]() O2(g)═CO(g)△H1<0,CO(g)+
O2(g)═CO(g)△H1<0,CO(g)+ ![]() O2(g)═CO2(g)△H2<0, C(s)+O2(g)═CO2(g)△H3<0;下列说法正确的是( )
O2(g)═CO2(g)△H2<0, C(s)+O2(g)═CO2(g)△H3<0;下列说法正确的是( )
A.56 g CO和32 g O2所具有的总能量小于88 g CO2所具有的总能量
B.碳的燃烧热是△H3
C.△H1<△H3
D.28 g CO的总能量比44 g CO2的总能量高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)现有下列十种物质:①蔗糖②熔融NaCl③石墨④铜丝⑤NaOH固体⑥SO2⑦NaHSO4固体⑧K2O固体⑨液态H2SO4⑩饱和FeCl3溶液 上述物质中可导电的是________(填序号,下同);上述物质中不能导电,但属于电解质的是_______________________。
(2)NaHSO4是一种酸式盐,请填写下列空白:
①NaHSO4晶体熔化时的电离方程式为______________________________。
②3 mol·L-1 NaHSO4与2 mol·L-1 Ba(OH)2溶液等体积混合,该反应总的离子方程为___________。
(3)实验室制备少量Fe(OH)3胶体所用的物质有__________(填序号),反应的离子方程式为________________________________________________。
(4)某强酸性反应体系中,反应物和生成物共六种物质:O2、MnO4-、H2O、Mn2+、H2O2、H+,已知该反应中H2O2只发生了如下过程:H2O2→O2。写出该反应的离子方程式:_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气溶于水达到平衡后,若其他条件不变,只改变某一条件,下列叙述正确的是( )
A.再通入少量氯气, ![]() 减小
减小
B.通入少量SO2 , 溶液的漂白性增强
C.加入少量水,水的电离平衡向正反应方向移动
D.加入少量固体NaOH,一定有c(Na+)=c(Cl﹣)+c(ClO﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)某溶液中可能含有Fe2+、Mg2+、Cu2+、NH4+、Al3+中的一种或几种。当加入一种淡黄色固体并加热溶液时,有刺激性气体放出和白色沉淀生成,加入淡黄色固体的物质的量(横坐标)与析出沉淀和产生气体的物质的量(纵坐标)的关系,如下图1所示。请填写下列空白:
(1)在该溶液中含有的离子是_____________,物质的量浓度之比为_______________。
(2)所加的淡黄色固体是________________(化学式)。

(二)黄铁矿石的主要成分为FeS2和少量FeS(假设其他杂质中不含Fe、S元素,且高温下不发生化学变化),是我国大多数硫酸厂制取硫酸的主要原料。某化学兴趣小组对该黄铁矿石进行如下实验探究。将m1 g该黄铁矿石的样品放入如图2装置(夹持和加热装置略)的石英管中,从a处不断地缓缓通入空气,高温灼烧黄铁矿样品至反应完全。其反应的化学方程式为:![]()
【实验一】:测定硫元素的含量
反应结束后,将乙瓶中的溶液进行如下处理:

(3)反应结束后乙瓶中的溶液需加足量H2O2溶液的目的是(用化学方程式表示)________________________________________。
(4)该黄铁矿石中硫元素的质量分数为______________(列出表达式即可)。
【实验二】:测定铁元素的含量

(5)③中,需要用到的仪器除烧杯、玻璃棒、胶头滴管外,还有_________________。
(6)某同学一共进行了三次滴定实验,实验结果记录如下:
实验次数 | 第一次 | 第二次 | 第三次 |
消耗KMnO4溶液体积/mL | 25.00 | 25.03 | 24.97 |
根据所给数据,计算该稀释液中Fe2+的物质的量浓度为c(Fe2+) =_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com