
【题目】COCl2俗名光气,有毒,在一定条件下,可发生:COCL2(g) ![]() CO(g)+CL2(g) △H<0.下列有关说法正确的是
CO(g)+CL2(g) △H<0.下列有关说法正确的是
A.在一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率
B.当反应达平衡时,恒温恒压条件下通入氨气能提高COCl2的转化率
C.单位时间内生成CO和Cl2的物质的量比为1∶1时,反应达到平衡状态
D.平衡时,其他条件不变,升高温度可使该反应的平衡常数增大
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. 凡是放热反应都是自发的,吸热反应都是非自发的
B. 自发反应的熵一定增大,非自发反应的熵一定减小或不变
C. ΔH<0、ΔS<0的反应一定能自发进行
D. ΔH>0、ΔS<0的反应一定不能自发进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是( )
A. 铁粉溶于稀盐酸:2Fe+6H+=2Fe3++3H2↑
B. 碳酸钙溶于稀盐酸:CO32-+2H+=CO2↑+H2O
C. 氧化铜溶于醋酸:CuO+2CH3COOH =Cu2+ +2CH3COO- +H2O
D. 硫酸铜与氢氧化钡溶液混合:Ba2++SO42-=BaSO4 ↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在处于化学平衡状态的体系中,如果下列量发生变化,其中一定能表明化学平衡移动的是
A.反应混合物的浓度
B.反应体系的压强
C.正、逆反应的速率
D.反应物的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在pH=1的无色溶液中,下列离子能大量共存的是
A.NH4+、Ba2+、NO3-、CO32-
B.Fe2+、OH-、SO42-、MnO4-
C.K+、Mg2+、NO3-、SO42-
D.Na+、Fe3+、Cl-、AlO2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将6 mol H2和3 mol CO充入容积为0.5 L的密闭容器中,进行如下反应:
2H2(g)+CO(g)![]() CH3OH(g),6秒末时容器内压强为开始时的0.6倍。
CH3OH(g),6秒末时容器内压强为开始时的0.6倍。
试计算:(1)H2的反应速率是多少?(2)CO的转化率为多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物甲中含有明矾KAl(SO4)2·12H2O、Al2O3和Fe2O3。在一定条件下由甲可实现下图所示的物质之间的转化。
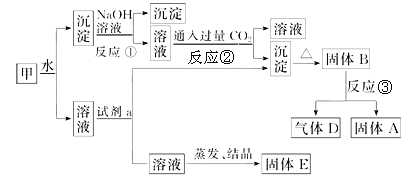
请回答下列问题:
(1)写出A、B的化学式:A______;B_____。
试剂a最好选用______________(填序号),写出反应的离子方程式:_________。
(2)除去固体A中混有的镁选用__________(填序号),写出反应的化学方程式:___________。
a.NaOH溶液 b.稀盐酸 c.二氧化碳 d.氨水
(3)写出反应②的离子方程式:_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁是最常见的金属材料。铁能形成[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(III)〕 和Fe(CO)x等多种配合物。
(1)基态Fe3+的核外电子排布式为_____,与NO3-互为等电子体的分子是__________。
(2)尿素(H2NCONH2)分子中C、N原子的杂化方式依次为______。C、N、O三种元素的第一电离能由大到小的顺序是______。
(3)配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=______。Fe(CO)x常温下呈液态,熔点为-20 .5 ℃,沸点为103 ℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于_______(填晶体类型)。
(4)铁有δ、γ、a三种同素异形体,δ、γ、a三种晶胞中铁原子的配位数之比为_______。
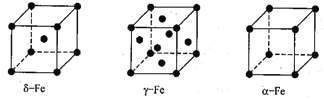
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com