
【题目】在溶液中,反应A+2BC分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.100mol/L、c(B)=0.200mol/L 及 c(C)=0mol/L.反应物A的浓度随时间的变化如图所示. 
请回答下列问题:
(1)与①比较,②和③分别仅改变一种反应条件.所改变的条件和判断的理由是: ②; .
③; .
(2)实验②平衡时B的转化率为;实验③平衡时C的浓度为;
(3)该反应的△H0,其判断理由是
(4)该反应进行到4.0min时的平均反应速率: 实验②:vB=
实验③:vc= .
【答案】
(1)加催化剂;达到平衡的时间缩短,平衡时A的浓度未变;温度升高;达到平衡的时间缩短,平衡时A的浓度减小
(2)40%;0.06mol/L
(3)>;温度升高,平衡向正反应方向移动,
(4)0.014mol(L?min)﹣1;0.009mol(L?min)﹣1
【解析】解:(1)与①比较,②缩短达到平衡的时间,因催化剂能加快化学反应速度率,化学平衡不移动,所以②为使用催化剂;
与①比较,③缩短达到平衡的时间,平衡时A的浓度减小,因升高温度,化学反应速度率加快,化学平衡移动,平衡时A的浓度减小,
所以答案是:②加催化剂;达到平衡的时间缩短,平衡时A的浓度未变;③温度升高;达到平衡的时间缩短,平衡时A的浓度减小;(2)由图可知,实验②平衡时A的浓度为0.06mol/L,故A的浓度变化量0.1mol/L﹣0.06mol/L=0.04mol/L,由方程式可知B的浓度变化量为0.04mol/L×2=0.08mol/L,故平衡时B的转化率为 ![]() ×100%=40%;
×100%=40%;
实验③平衡时A的浓度为0.04mol/L,故A的浓度变化量0.1mol/L﹣0.04mol/L=0.06mol/L,由方程式可知C的浓度变化量为0.06mol/L,故平衡时C的浓度为0.06mol/L,
所以答案是:40%;0.06mol/L;(3)因③温度升高,平衡时A的浓度减小,化学平衡向吸热的方向移动,说明正反应方向吸热,即△H>0,
所以答案是:>;温度升高,平衡向正反应方向移动;(4)实验②中,vA= ![]() =0.007mol(Lmin)﹣1,所以vB=2vA=0.014mol(Lmin)﹣1;
=0.007mol(Lmin)﹣1,所以vB=2vA=0.014mol(Lmin)﹣1;
实验③中,vA= ![]() =0.009mol(Lmin)﹣1,所以vC=vA=0.009mol(Lmin)﹣1,
=0.009mol(Lmin)﹣1,所以vC=vA=0.009mol(Lmin)﹣1,
所以答案是:0.014mol(Lmin)﹣1;0.009mol(Lmin)﹣1.
【考点精析】本题主要考查了化学平衡状态本质及特征和化学平衡的计算的相关知识点,需要掌握化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效);反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%才能正确解答此题.


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
【题目】利用周期表中同族元素的相似性,可预测元素的性质.
(1)P元素的基态原子有个未成对电子,白磷的分子式为P4 , 其结构如图1所示. 
科学家目前合成了N4分子,N原子的杂化轨道类型是 , N﹣N键的键角为;N4分解后能产生N2并释放出大量能量,推测其用途为 .
(2)N、P、As原子的第一电离能由大到小的顺序为 .
(3)立方氮化硼晶体的结构如图2所示:
该晶体中,B原子填充在N原子的空隙,且占据此类空隙的比例为 (填百分数).
(4)N与As是同族元素,B与Ga是同族元素,立方砷化镓晶体与立方氮化硼晶体结构类似,两种晶体中熔点较高的是;立方砷化镓晶体的晶胞边长为a pm,则其密度为gcm﹣3 (用含a的式子表示,设NA为阿伏加德罗常数的值).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关有机物的说法正确的是( )
A.1mol ![]() 能与4molNaOH充分反应
能与4molNaOH充分反应
B.![]() 系统命名法为3﹣丁烯
系统命名法为3﹣丁烯
C.![]() 的碳原子都在一个平面内,且它的二氯代物为3种
的碳原子都在一个平面内,且它的二氯代物为3种
D.1mol ![]() 可以与4molH2发生加成
可以与4molH2发生加成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置进行下列实验,能得出相应实验结论的是( ) 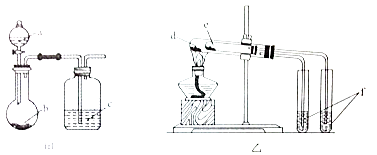
选项 | 实验试剂 | 实验结论 | ||
A | a.稀硫酸 | b.碳酸氢钠 | c.硅酸钠溶液 | 酸性:硫酸>碳酸>硅酸 |
B | a.稀盐酸 | b.二氧化锰 | c.溴化钠溶液 | 氧化性:MnO2>Cl2>Br2 |
C | d.小苏打 | e.苏打 | f.石灰水 | 热稳定性:苏打>小苏打 |
D | d.氯化钠 | e.氯化铵 | f.硝酸银溶液 | 沸点:氯化钠>氯化铵 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.工业上将氯气通入澄清石灰水制取漂白液。
B.油脂和氨基酸在一定条件下均可以与氢氧化钠溶液反应
C.向鸡蛋清水溶液中滴加硫酸铵溶液可使蛋白质发生变性
D.胶体与溶液的本质区别是胶体具有丁达尔效应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列各图的叙述正确的是( )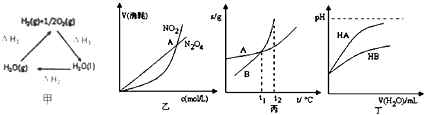
A.甲中△H1=﹣(△H2+△H3)
B.乙表示恒温恒容条件下发生的可逆反应2NO2(g)═N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
C.丙表示A,B两物质的溶解度随温度变化情况,将tl℃时A、B的饱和溶液分别升温至t2℃时,溶质的质量分数B>A
D.丁表示常温下,稀释HA,HB两种酸的稀溶液时,溶液pH随加水量的变化,则NaA溶液的pH大于等物质的量浓度的NaB溶液的pH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用如图所示装置制备并检验Cl2的性质.下列说法正确的是( ) 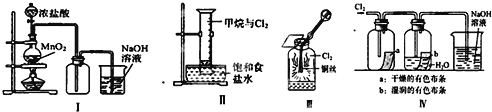
A.Ⅰ图中:如果MnO2过量,浓盐酸就可全部被消耗
B.Ⅱ图中:量筒中发生了加成反应
C.Ⅲ图中:生成蓝色的烟
D.Ⅳ图中:湿润的有色布条能褪色,将硫酸溶液滴入烧杯中,至溶液显酸性,结果有Cl2生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把aL一个大气压,120℃的氢气氧气混合于密闭容器中,电火花引爆后恢复至原状态,测得体积为bL,则下列表述不可能正确的是( )
A.2a=3b
B.7b=4a
C.原混合气体中V(H2)=bL,V(O2)=(a﹣b)L
D.原混合气体中V(H2)=2(a﹣b)L,V(O2)=(2b﹣a)L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com