
【题目】主族元素镓(Ga)的原子结构示意图是  ,下列关系不正确的是( )
,下列关系不正确的是( )
A.原子半径:K>Ga>Al
B.碱性:KOH>Ga(OH)3>Al(OH) 3
C.离子的氧化性:K+>Ga3+>Al3+
D.与水反应的剧烈程度:K>Ga>Al
【答案】C
【解析】解:A.K、Ga位于同一周期,从左到右原子半径逐渐减小,则K>Ga,Ga、Al位于同一主族,从上到下原子半径逐渐增大,则Ga>Al,故A正确; B.K、Ga位于同一周期,从左到右金属性逐渐减弱,则K>Ga,Ga、Al位于同一主族,从上到下金属性逐渐增大,则Ga>Al,则金属性K>Ga>Al,原子的金属性越强,对应的最高价氧化物的水化物的碱性越强,则碱性:KOH>Ga(OH)3>Al(OH) 3 , 故B正确;
C.金属性K>Ga>Al,元素的金属性越强,对应的阳离子的氧化性越弱,故C错误;
D.金属性K>Ga>Al,金属性越强,对应的单质与水反应越剧烈,故D正确.
故选C.


科目:高中化学 来源: 题型:
【题目】已知某溶液中含有Cl﹣、Br﹣、I﹣的物质的量之比为2:3:4,要使溶液中Cl﹣、Br﹣、I﹣的物质的量之比为4:3:2,则通入的Cl2物质的量是原溶液中I﹣物质的量的( )
A.![]()
B.![]()
C.![]()
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氯气的叙述正确的是
A. 氯气可用于漂白,这是氯气的漂白作用
B. 纯净的氢气可以在氯气中安静地燃烧,发出苍白色火焰
C. 钠在氯气中燃烧产生白色烟雾
D. 红热的铜丝可以在氯气中燃烧,产生棕黄色烟雾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,苯甲酸可实现如下转化:
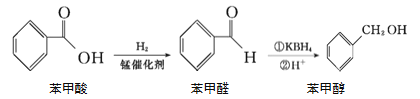
(1)Mn2+基态核外电子排布式为________。
(2)B、C、O、K 的第一电离能由小到大的顺序是________。
(3)1mol苯甲酸分子含有δ键的数目为________,苯甲醇分子中O原子的轨道杂化类型为____。
(4)KBH4中所含BH4-离子空间构型为_____,写出一种与BH4-互为等电子体的阳离子的化学式:_________。
(5)苯甲酸、苯甲醛、苯甲醇三种物质中沸点最低的是____,原因是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于硅及其化合物的叙述正确的是
A. 陶瓷、玻璃、水泥都是硅酸盐产品
B. 硅晶体可用于制造光导纤维
C. 二氧化硅在电子工业中是重要的半导体材料
D. 二氧化硅与氢氟酸和氢氧化钠均能反应,属于两性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向两个体积可变的密闭容器中均充入1mol的A 和2 mol 的B,发生反应:A2(g)+2B2(g)![]() 2AB2(g) △H。维持两个容器的压强分别为p1和p2,在不同温度下达到平衡,测得平衡时AB2的体积分数随温度的变化如图所示。
2AB2(g) △H。维持两个容器的压强分别为p1和p2,在不同温度下达到平衡,测得平衡时AB2的体积分数随温度的变化如图所示。
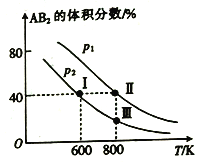
已知: ①图中I、Ⅱ、Ⅲ点均处于曲线上;②点Ⅱ时容器的体积为0.1L。下列叙述正确的是
A. 由图像可知:p1>p2 △H<0
B. 点I时A2的平衡转化率为40%
C. 点Ⅲ所对应的反应平衡常数K=0.2
D. 将点Ⅱ所对应的容器冷却到600 K,可变成点I
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去空气中的二氧化硫和氨氧化物气体对环境保护有重要意义。
(1)二氧化硫易溶于水,溶于水后所得溶液中H2SO3、HSO3-和SO32- 占三种粒子总数的比例随pH的变化如下图所示。由图可知H2SO3 的电离平衡常数Ka1=____________。
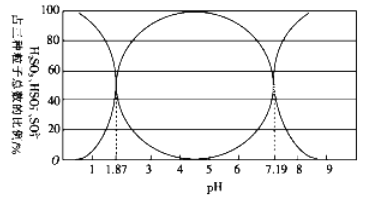
(2)利用尿素[CO(NH2)2]水解的溶液可以吸收含SO2 的空气。已知尿素水解放热,常温下水解反应较慢,水解的反应方程式如下:CO(NH2)2+H2O=H2NCOONH4(氨基甲酸铵)。
①氨基甲酸铵会与空气中的SO2 和O2 反应生成(NH4)2SO4,该反应的化学方程式为__________。
②一定条件下,用尿素溶液吸收含SO2 的空气,测得SO2 的吸收率随溶液的温度变化如图甲所示。温度高于60 ℃时,SO2 的吸收率逐渐升高的原因是_____________。
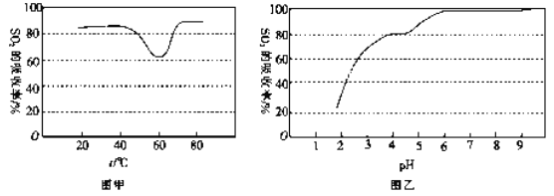
③尿素溶液吸收SO2 的吸收率随溶液的pH变化如图乙所示。尿素溶液吸收含SO2的空气后溶液的pH会降低,为提高SO2 的吸收率和充分回收产物,最好向溶液中加入_____(填溶液的名称)并控制pH 为_______。
(3)一种电化学脱硝法的原理如图所示。
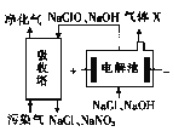
①电解池阴极所发生的电极反应为_____________。
②相同条件下通入的污染气和生成的X 的体积比为40 :3,污染气中NO 和NO2 占总体积的10%,若NaClO完全反应,污染气中NO和NO2 被完全吸收且其余气体不参与反应,则NO和NO2 的体积比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、 D、E、F 原子序数依次增大的六种元素,它们位于元素周期表的前四周期。A元素能级数与核外电子数相等;B 元素含有3个能级,且每个能级所含的电子数相同;D 的原子核外有8 个运动状态不同的电子,E元素与F元素处于同一周期相邻的族,它们的原子序数相差3,且E 元素的基态原子有4 个未成对电子。请回答下列问题:
(1)请写出D 基态的价层电子排布图_______________。
(2)下列说法错误的是______________。
A.二氧化硅的相对分子质量比二氧化碳大,所以沸点: SiO2>CO2
B.电负性顺序: C
C.N 2 与CO 为等电子体,结构相以,化学性质相似
D.稳定性:H2O>H2S,原因是水分子间存在氢键
(3)某化合物与F(I)(I 表示化合价为+1)结合形成下图所示的离子,该离子中碳原子的杂化方式是______。

(4)己知(BC)2 是直线性分子,并有对称性,且分子中每个原子最外层都达到8电子稳定结构,则(BC)2中σ键和π键的个数比为_________________。
(5) C元素最高价含氧酸与硫酸酸性强度相近,原因是______________。
(6) B单质的一种的晶体结构如图所示,则一个晶胞中所含B 原子数为__________;其中原子坐标参数a 为0,0,0), b 为(1/2,1/2,0),则c点原子的坐标参数为______________。

(7)D与F 形成离子个数比为1:1的化合物,晶胞与NaCl类似,D 离子的配位数是______;设D离子的半径为apm,F离子的半径为bpm,求该晶胞的空间利用率为__________(列出计算式即可)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com