
下列实验装置或实验操作中错误的是( )
|
| A. |
| B. |
| C. |
| D. |
|
| 化学实验方案的评价.. | |
| 专题: | 实验评价题. |
| 分析: | A.用量筒量取液体时,读数时视线应与量筒内液体凹液面的最低处保持水平; B.符合一贴二低三靠; C.瓶塞倒放、标签向手心; D.二氧化碳密度大于空气,用向上排空气法收集. |
| 解答: | 解:A.用量筒量取液体时,读数时视线应与量筒内液体凹液面的最低处保持水平,如图仰视读数会偏大,故A错误; B.如图过滤操作所用仪器和操作均正确,故B正确; C.液体倾倒瓶塞倒放、标签向手心、瓶口紧靠容器口,故C正确; D.实验室二氧化碳的制取常用固液不加热装置如图,长颈漏斗浸没,集气瓶正放,因为它密度大于空气,故D正确. 故选A. |
| 点评: | 本题考查化学实验方案的评价,难度不大,侧重实验基本操作和实验原理的考查,注意装置的作用及实验的操作性、评价性分析,题目难度不大. |


科目:高中化学 来源: 题型:
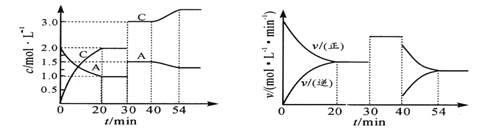
一定温度下,某密闭容器中充入等物质的量的气体A和B,发生如下反应:A(g)+xB(g)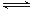 2C(g)。达到平衡后,只改变反应的一个条件,测得容器内有关物质的浓度、反应速率随时间的变化如下图所示。请回答下列问题:
2C(g)。达到平衡后,只改变反应的一个条件,测得容器内有关物质的浓度、反应速率随时间的变化如下图所示。请回答下列问题:
(1)在该条件下,当V(B)正 : V(C)逆 = ▲ 时反应达到了化学平衡状态。
(2)若25min、35min时的化学平衡常数分别为K1、K2,则二者的大小关系是 ▲ 。
(3)在甲、乙、丙三个相同的密闭容器中按表中所述投料,在恒温、恒容的条件下进行反应,平衡后测得A的浓度如表中所示:
| 容器 | 甲 | 乙 | 丙 |
| 起始投料 | 1molA和1molB | 2molC | 2molA和2molB |
| A的平衡浓度 | C1 | C2 | C3 |
则:C1、C2、C3三者数值的关系式为 ▲ (用代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
把质量为m g的铜丝灼烧变黑,立即放入下列物质中,能使铜丝变红,而且质量仍为m g的是( )
A. 稀H2SO4 B. C2H5OH C. 稀HNO3 D. CH3COOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是CO2电催化还原为CH4的工作原理示意图。下列说法不正确的是
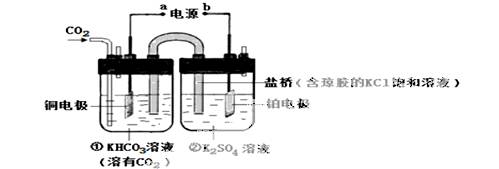
A.该过程是电能转化为化学能的过程
B.一段时间后,①池中n(KHCO3)不变
C.一段时间后,②池中溶液的pH 一定下降
D.铜电极的电极反应式为CO2+8H++8e- = CH4+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
肼是重要的化工原料。某探究小组利用下列反应制取水合肼(N2H4·H2O)。
 CO(NH2)2+ 2NaOH + NaClO = Na2CO3 + N2H4·H2O + NaCl
CO(NH2)2+ 2NaOH + NaClO = Na2CO3 + N2H4·H2O + NaCl
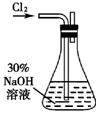
实验一: 制备NaClO溶液。(实验装置如右图所示)
(1)配制30%NaOH溶液时,所需玻璃仪器除量筒外还有 (填标号)。
A.容量瓶 B.烧杯 C.烧瓶 D.玻璃棒
(2) 锥形瓶中发生反应的化学方程式是 。
 (3) 因后续实验需要,需利用中和滴定原理测定反应后锥形瓶中混合溶液的NaOH的浓度。请选用所提供的试剂(H2O2溶液、FeCl2溶液、0.1000mol·L-1盐酸、酚酞试液),设计实验方案。
(3) 因后续实验需要,需利用中和滴定原理测定反应后锥形瓶中混合溶液的NaOH的浓度。请选用所提供的试剂(H2O2溶液、FeCl2溶液、0.1000mol·L-1盐酸、酚酞试液),设计实验方案。
。
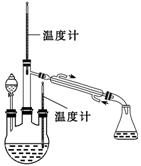
实验二: 制取水合肼。(实验装置如右图所示)
控制反应温度,将分液漏斗中溶液缓慢滴入三颈烧瓶中,充分反应。
加热蒸馏三颈烧瓶内的溶液,收集108~114℃馏分。
(已知:N2H4·H2O + 2NaClO = N2↑ + 3H2O + 2NaCl)
(4)分液漏斗中的溶液是 (填标号)。
A.CO (NH2) 2溶液 B.NaOH和NaClO混合溶液
选择的理由是 。
实验三: 测定馏分中肼含量。
称取馏分5.000g,加入适量NaHCO3固体,加水配成250mL溶液,移出25.00mL,用0.1000mol·L-1的I2溶液滴定。滴定过程中,溶液的pH保持在6.5左右。
(已知:N2H4·H2O + 2I2 = N2↑+ 4HI + H2O)
(5)滴定过程中,NaHCO3能控制溶液的pH在6.5左右,原因是 。
(6)实验测得消耗I2溶液的平均值为18.00mL,馏分中水合肼(N2H4·H2O)的质量分数为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中正确的是( )
|
| A. | 1mol任何纯净物都含有相同的分子数 |
|
| B. | 1molO2中约含有6.02×1023个氧分子 |
|
| C. | 1mol氢中含有2mol氢原子 |
|
| D. | 阿伏加德罗常数就是6.02×1023mol﹣1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验的叙述中,正确的是( )
|
| A. | 容量瓶用蒸馏水洗净后,可不经干燥直接用于配制溶液 |
|
| B. | 用分液的方法分离水和酒精的混合物 |
|
| C. | 配制1L0.1mol/L的NaCl溶液时可用托盘天平称量5.85gNaCl固体 |
|
| D. | 用滴管滴加液体时,为防止液滴飞溅,滴管紧贴试管内壁 |
查看答案和解析>>
科目:高中化学 来源: 题型:
分子式为C7H8的某有机物,它能使酸性高锰酸钾溶液褪色,但不能与溴水反应。在一定条件下与H2完全加成,加成产物一氯代物的同分异构体数目与该有机物一氯代物的同分异构体数目相比
A.前者多 B.后者多 C.一样多 D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
元素周期表和元素周期律可以指导人们进行规律性的推测和判断。下列说法不合理的是
A.微粒X2-与Y2+核外电子排布相同,离子半径:X2-> Y2+
B.人们可在周期表的过渡元素中寻找催化剂、耐腐蚀和耐高温的合金材料
C.由水溶液的酸性:HCl>HF,可推断出元素的非金属性:Cl>F
D.Be元素与Al元素同处在周期表的金属与非金属的交界处,可推出:
Be(OH)2+ 2OH-=BeO22-+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com