
下面是有关物质的转化关系图(部分产物已省略),其中A为单质,E在常温下为液体,D是一种温室气体,C的相对分子质量为78。请回答相关问题。

(1)下列对C的结构、性质推断中不正确的是 ( )。
A.久置于空气中会变成白色
B.具有强氧化性
C.晶体中存在离子键与非极性键
D.是一种碱性氧化物
(2)A的原子结构示意图为____________________,H的电子式为____________________,E的结构式为____________________。
(3)C和E反应生成H的离子方程式为__________________,反应中氧化剂与还原剂的物质的量之比为______。
解析 由题知,E可能为水,A→B→C连续反应,可能为连续氧化,能发生连续氧化的单质有Na、S、C、N2,单质、两种氧化物均能与水反应,只有钠、氧化钠、过氧化钠,过氧化钠的相对分子质量为78,验证正确。则A为钠、F为氧气,B为氧化钠,C为过氧化钠,D为二氧化碳,H为氢氧化钠。(1)A项,Na2O2放置空气中最终变成白色的Na2CO3,正确;B项,Na2O2中-1价的氧既有氧化性又有还原性,以强氧化性为主,正确;C项,Na+与O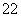 间存在离子键,O
间存在离子键,O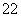 内部存在非极性共价键,正确;D项,Na2O2与酸反应除生成盐和水外还有O2生成,不是碱性氧化物。
内部存在非极性共价键,正确;D项,Na2O2与酸反应除生成盐和水外还有O2生成,不是碱性氧化物。
答案 (1)D (2) Na+[
Na+[
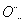
 H]-
H]- 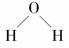 (3)2Na2O2+2H2O===4Na++4OH-+O2↑ 1∶1
(3)2Na2O2+2H2O===4Na++4OH-+O2↑ 1∶1


 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:高中化学 来源: 题型:
下列各组离子在无色溶液中能大量共存的是
A.H+、Cl-、SO42-、K+ B.K+、H+、Na+、HCO3-
C.Cu2+、K+、SO42-、Cl- D.Ag+、NO3-、Cl-、K+
查看答案和解析>>
科目:高中化学 来源: 题型:
苯甲酸广泛应用于制药和化工行业。某化学小组用甲苯作主要原料制备苯甲酸,反应
过程如下:

甲苯、苯甲酸钾、苯甲酸的部分物理性质见下表:
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g·cm-3 | 在水中溶解性 |
| 甲苯 | -95 | 110.6 | 0.8669 | 难溶 |
| 苯甲酸钾 | 121.5~123.5 |
|
| 易溶 |
| 苯甲酸 | 122.4 | 248 | 1.2659 | 微溶 |
(1)将步骤①得到混合物加少量水,分离有机相和水相。有机相在 ▲ (填“上”或“下”)层;实验操作的名称是 ▲ 。
(2)步骤②用浓盐酸酸化的目的是 ▲ 。
(3)减压过滤装置所包含的仪器除减压系统外,还有 ▲ 、 ▲ (填仪器名称)。
(4)已知温度越低苯甲酸的溶解度越小,但为了得到更多的苯甲酸晶体,重结晶时并非温度越低越好,理由是 ▲ 。
(5)重结晶时需要趁热过滤,目的是 ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)广州亚运会“潮流”火炬内熊熊大火来源于丙烷的燃烧,丙烷是一种优良的燃料。试回答下列问题:
若使23 g液态无水酒精完全燃烧,并恢复到室温,则整个过程中放出的热量为______kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中不正确的是 ( )。
A.分散质微粒直径介于1~100 nm之间的分散系称为胶体
B.在水溶液里或熔融状态下能够导电的化合物中一定是离子化合物
C.液态氯化氢、熔融氧化铝、固体硫酸钡都是电解质
D.非金属氧化物不一定是酸性氧化物,有些金属氧化物也可能是酸性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.糖类、油脂、蛋白质在一定条件都能发生水解反应
B.苯只能发生取代反应,不能发生加成反应
C.棉、麻、羊毛及合成纤维完全燃烧都只生成CO2和H2O
D.溴乙烷与NaOH的乙醇溶液共热生成乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室采用MgCl2、AlCl3的混合溶液与过量氨水反应制备MgAl2O4二主要流程如下:


 ⑴制备MgAl2O4过程中,高温焙烧时发生反应的化学方程式 。
⑴制备MgAl2O4过程中,高温焙烧时发生反应的化学方程式 。
⑵如图所示,过滤操作中的一处错误是 。
判断流程中沉淀是否洗净所用的试剂是 。高温焙烧时,用于盛放固体的仪器名称是 。
⑶在25℃下,向浓度均为0.01 mol·L-1的MgCl2和AlCl3混合溶液中逐滴加入氨 水,先生成_________________沉淀(填化学式),生成该沉淀的离子方程式_____________________(已知25℃时Ksp[Mg(OH)2]=1.8×1
水,先生成_________________沉淀(填化学式),生成该沉淀的离子方程式_____________________(已知25℃时Ksp[Mg(OH)2]=1.8×1 0-11,Ksp[Al(OH)3]=3×10 -34。)
0-11,Ksp[Al(OH)3]=3×10 -34。)
⑷无水AlCl3(183℃升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。

装置B中盛放饱和NaCl溶液,该装置的主要作用是 ;F中试剂的作用是 ;用一件仪器装填适当试剂后也可起到F和G的作用,所装填的试剂为 。
⑸将Mg、Cu组成的3.92g混合物投入过量稀硝酸中,充分反应后,固体完全溶解时收集到还原产物NO气体1.792L(标准状况),向反应后的溶液中加入4mol/L的NaOH溶液80mL时金属离子恰好完全沉淀。则形成沉淀的质量为 g。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式中,属于水解反应的是
A.H2SO3+H2O HSO3- + H3O+ B.CO32— + H2O
HSO3- + H3O+ B.CO32— + H2O HCO3— + OH—
HCO3— + OH—
C.NH3·H2O NH4+ +OH- D.HS— + H2O
NH4+ +OH- D.HS— + H2O S2— + H3O+
S2— + H3O+
查看答案和解析>>
科目:高中化学 来源: 题型:
“天蓝蓝海蓝蓝,海边小城威海卫”。威海海水资源丰富,回答下列问题:
(1)海水中主要含有 等离子(写离子符号,至少答出4种)。
(2)海水脱硫是一种有效除去火力发电产生的SO2的方法。其工艺流程如下图所示:

天然海水吸收了含硫烟气后,要用O2进行氧化处理,其反应的化学方程式是: ;氧化后的“海水”需要用大量的天然海水与之混合后才能排放,该操作的主要目的是 。
(3)下图是海水综合利用的一个方面。

请回答下列问题:
I.①步主要反应的离子方程式: 。
溴及其化合物的用途有很多,写出其中的一种 。
II.第③步需要加入 ,其前面分离出氢氧化镁的操作称为 ,将镁条在二氧化碳中燃烧的产物为 。
III.粗盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4 等杂质,通过如下几个实验步骤,可制得纯净的食盐水:① 加入稍过量的Na2CO3溶液;② 加入稍过量的NaOH溶液;③ 加入稍过量的BaCl2 溶液;④滴入稀盐酸至无气泡产生;⑤ 过滤 正确的操作顺序是
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com