
【题目】已知:
R-CH=CH2+H2O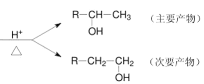
现以2-甲基丙烷为有机原料,配以其他必要的无机物原料,选择反应中的主要产物按以下流程合成产品:
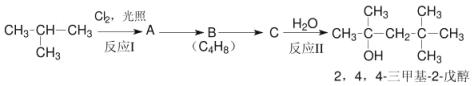
请回答:
(1)写出丙烯与氯化氢反应的主要产物的结构简式__________________;
(2)写出反应Ⅰ得到产物可能的结构简式__________________;
(3)写出反应类型:反应Ⅰ_________、反应Ⅱ_________;
(4)写出 A→B 的反应条件_____;B→C 的化学方程式_____。
【答案】![]()
 取代反应 加成反应 NaOH 醇溶液、加热
取代反应 加成反应 NaOH 醇溶液、加热 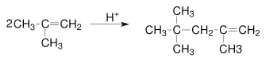
【解析】
根据合成图及题给信息用逆推和正推相结合的方法分析得:C为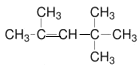 ,根据B的分子式分析,B为
,根据B的分子式分析,B为![]() ;2-甲基丙烷与氯气发生取代反应得到A,A的结构为
;2-甲基丙烷与氯气发生取代反应得到A,A的结构为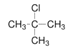 ,A发生消去反应得到B,据此分析解答。
,A发生消去反应得到B,据此分析解答。
(1)根据题给反应分析,双键发生加成反应时,主要产物为氢原子加在氢原子较多的碳原子上,所以丙烯与氯化氢反应的主要产物的结构简式为![]() ,故答案为:
,故答案为:![]() ;
;
(2)2-甲基丙烷与氯气发生取代反应时,氯原子可以取代甲基上的氢原子,也可以取代次甲基上的氢原子,所以产物有两种:![]() 、
、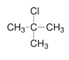 ,故答案为:
,故答案为:![]() 、
、 ;
;
(3)根据上述分析,比较反应前后结构的变化得,反应I为取代反应;反应II为加成反应,故答案为:取代反应;加成反应;
(4)A→B的反应为卤代烃的消去反应,反应条件是NaOH 醇溶液、加热; B→C根据反应物和生成物的结构变化及碳碳双键的性质分析,化学方程式为: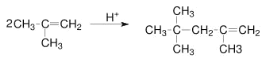 ,故答案为:NaOH 醇溶液、加热 ;
,故答案为:NaOH 醇溶液、加热 ; 。
。


科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y 和 Z 的原子序数依次增大,W 的气态氢化物的水溶液使酚酞变红 并且可与X 的氢化物形成一种共价化合物。Y 是地壳中含量最多的金属元素,Z原子最外层电子数是其内层电子总数的 3/5。下列说法中一定正确的是
A.它们的简单离子半径大小顺序: W<X<Y<Z
B.X的简单气态氢化物稳定性比Z 的强
C.W的氧化物对应水化物为强酸,具有强氧化性
D.工业上一般采取电解Y 的熔融氯化物来生产Y的单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在 120℃时,将下列各组烃以任意比例混合,与过量 O2 在一密闭容器中完全反应,测知反应前后的压强没有变化,则该混合烃是( )
A.CH4 和 C2H4B.CH4 和 C2H6C.C2H2 和 C2H4D.C3H4 和 C3H6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液的说法不正确的是
A. 向![]() 溶液中通入
溶液中通入![]() ,
,![]() 减小
减小
B. 将![]() 的
的![]() 溶液从
溶液从![]() 升温至
升温至![]() ,
,![]() 增大
增大
C. 向![]() 的HF溶液中滴加NaOH溶液至中性,
的HF溶液中滴加NaOH溶液至中性,![]() =1
=1
D. 向![]() 的
的![]() 溶液中加入少量水,
溶液中加入少量水,![]() 增大
增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下实验原理或操作中,正确的是![]()
A.用NaOH溶液滴定盐酸,滴定前尖嘴下端有气泡,滴定后气泡消失,会使结果偏高
B.仰视量筒刻度量取一定量浓硫酸所配制的![]()
![]()
![]() 溶液的浓度结果偏低
溶液的浓度结果偏低
C.焰色反应实验中,铂丝在蘸取待测溶液前应先用稀硫酸洗净并灼烧至无色
D.要将溶解在![]() 中的碘分离出来,应用蒸馏法,因为碘易升华,先分离出来
中的碘分离出来,应用蒸馏法,因为碘易升华,先分离出来
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下用![]() 盐酸分别滴定
盐酸分别滴定![]() 浓度均为
浓度均为![]() 的NaOH溶液和二甲胺
的NaOH溶液和二甲胺![]() 溶液
溶液![]() 在水中电离方式与氨相似
在水中电离方式与氨相似![]() ,利电用传感器测得滴定过程中溶液的电导率如图所示。已知电解质溶液电导率越大导电能力越强。
,利电用传感器测得滴定过程中溶液的电导率如图所示。已知电解质溶液电导率越大导电能力越强。
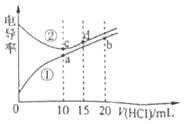
①a、b、c、d四点的水溶液中,由水电离出氢离子浓度大于1.0×10-7![]() 的是______,原因为______。
的是______,原因为______。
②化学反应往往伴有热效应,若为绝热体系,a的温度______![]() 填“
填“![]() ”,“
”,“![]() ”或“
”或“![]() ”
”![]() 点的温度。
点的温度。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】熟悉和使用中学化学实验中常见仪器及用途,是化学学习的基本要求。试回答下列问题。
(1)在仪器a.分液漏斗 b.试剂瓶 c.集气瓶 d.滴定管 e.容量瓶 f.量筒 g.托盘天平中,标有“0”刻度的是________(填序号)。
(2)“磨砂”是增加玻璃仪器密封性的一种处理工艺,在下列仪器中,没有用到“磨砂”工艺处理的有________(填序号)。
a.试管 b.分液漏斗 c.带滴管的试剂瓶(滴瓶)d.集气瓶 e.酸式滴定管 f.碱式滴定管
(3)用装置甲、乙、丙和乳胶管组成一套装置(气密性已检查),可用于制取并收集NH3或HCl气体,可供选择的液体试剂有:浓硫酸、浓盐酸、浓氨水,丙中试剂为紫色石蕊溶液。试回答下列问题:
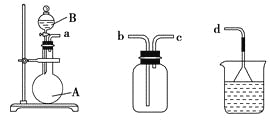
甲 乙 丙
①若制取某气体的过程中,丙中的石蕊溶液变红,且烧瓶中的试剂A与分液漏斗中的试剂B均为无色液体,则试剂A为________,制取该气体利用了B的性质有________、________。
通过丙中紫色石蕊溶液变红或变蓝,说明乙中气体已集满。若石蕊溶液变蓝,则烧瓶甲中应加入的固体试剂A为________。
②若在乙中收集氨气,气体流经装置的顺序是:a―→____―→_____―→d(填接口代号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化镓(GaN)被称为第三代半导体材料,其应用取得了突破性的进展。一种镍催化法生产GaN的工艺如图:

(1)“热转化”时Ga转化为GaN的化学方程式是_____。
(2)“酸浸”的目的是_____,“操作Ⅰ”中包含的操作是_____。
某学校化学兴趣小组在实验室利用图装置模拟制备氮化镓:

(3)仪器X中的试剂是_____,仪器Y的名称是_____,装置G的作用是_____。
(4)加热前需先通入一段时间的H2,原因是_____。
(5)取某GaN样品m克溶于足量热NaOH溶液,发生反应 GaN+OH﹣+H2O![]() GaO2-+NH3↑,用H3BO2溶液将产生的NH3完全吸收,滴定吸收液时消耗浓度为c mol/L的盐酸V mL,则样品的纯度是_____。(已知:NH3+H3BO3=NH3H3BO3;NH3H3BO3+HCl=NH4Cl+H3BO3)
GaO2-+NH3↑,用H3BO2溶液将产生的NH3完全吸收,滴定吸收液时消耗浓度为c mol/L的盐酸V mL,则样品的纯度是_____。(已知:NH3+H3BO3=NH3H3BO3;NH3H3BO3+HCl=NH4Cl+H3BO3)
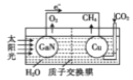
(6)科学家用氮化镓材料与铜组装成如图所示的人工光合系统,成功地实现了用CO2和H2O合成CH4,请写出铜极的电极反应式_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com