
【题目】下列物质中既能与强酸反应又能与强碱反应的是( )
A.AlB.Mg(OH)2C.AlCl3D.SiO2
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、R、Q为前30号元素,且原子序数依次增大.X是所有元素中原子半径最小的,Y有三个能级,且每个能级上的电子数相等,Z原子单电子数在同周期元素中最多,W与Z同周期,第一电离能比Z的低,R与Y同一主族,Q的最外层只有一个电子,其他电子层电子均处于饱和状态.请回答下列问题:
(1)Q+核外电子排布式为___________;
(2)化合物X2W2中W的杂化方式为___________,ZW2-离子的立体构型是___________;
(3)Y、R的最高价氧化物的沸点较高的是___________(填化学式),原因是___________;
(4)将Q单质的粉末加入到ZX3的浓溶液中,并通入W2,充分反应后溶液呈深蓝色,该反应的离子方程式为___________;
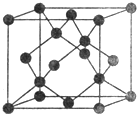
(5)Y有多种同素异形体,其中一种同素异形体的晶胞结构如图,该晶体一个晶胞的Y原子数为___________,Y原子的配位数为___________,若晶胞的边长为a pm,晶体的密度为ρ g/cm3,则阿伏加德罗常数的数值为___________(用含a和ρ的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B都为短周期元素,且甲、乙、丙常温下都为气体(如图所示)。2 mol甲分子反应生成1 mol 丙和3 mol乙,下列对此判断不正确的是( )

A. 1个乙分子中含有2个A原子
B. 甲的摩尔质量为17 g·mol-1
C. 同温同压下,生成丙和乙的体积比为1∶3
D. 标准状况下,11.2 L甲溶于500 mL水中,所得溶液中甲的物质的量浓度为1 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】①~⑧在元素周期表的对应位置如图所示,用化学式或元素符号回答下列问题。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ⑦ | ① | ② | |||||
3 | ③ | ④ | ⑤ | ⑧ | ⑥ |
(1)元素⑧的原子结构示意图__________;
(2)请写出⑦的单质与⑧的最高价氧化物对应的水化物的浓溶液在加热条件下反应的化学方程式为:__。
(3)元素③的最高价氧化物对应的水化物中含有_____(填离子键、极性共价键或非极性共价键),该物质的电子式为________
(4)元素①的氢化物与其最高价氧化物所对的水化物反应的产物为______,该物质为_______(填离子化合物或共价化合物);一定条件下①的氢化物与⑥的单质混合,得到另一种单质和盐的化学方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有IL1.0mol/L的氨水,下列关于该氨水的说法正确的是
A. NH3H2O的物质的量为1mol B. NH4+为1mol
C. NH3、NH3H2O、NH4+的物质的量之和为1mol D. NH3为1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁粉在焰火、闪光粉、鞭炮中是不可缺少的原料,工业制造镁粉是将镁蒸气在某冷却剂中冷却。①空气、②氧气、③氩气、④氢气、⑤氮气、⑥二氧化碳,其中可作为镁蒸气冷却剂的是
( )
A.①②B.③④C.③⑥D.③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴被誉为战略物资,有出色的性能和广泛的应用。以水钴矿(主要成分为Co2O3、CoO、CuO、Fe2O3、CaO、MgO、NiO和SiO2等)为原料制备CoCl2·6H2O的工艺流程如图所示:

回答下列问题:
(1)“酸浸”
①钴的浸出率随酸浸时间、温度的变化关系如下图所示。综合考虑成本,应选择的最佳工艺条件为_________________;滤渣A的主要成分为__________。

②写出Co2O3与浓硫酸反应生成CoSO4的化学方程式___________________________。
(2)“净化除杂”过程包括除铁、除钙镁、除铜等步骤。
①除铁:加入适量Na2SO4固体,析出淡黄色晶体黄钠铁矾Na2Fe6(SO4)4(OH)12,写出反应的离子方程式____________________________________。
②除铜:加入适量Na2S2O3,发生反应2CuSO4+2Na2S2O3+2H2O=Cu2S↓+S↓+2Na2SO4+2H2SO4,Na2S2O3中硫元素的化合价是___________,上述反应每消耗15.8 g Na2S2O3,反应中转移电子___________mol。
(3)“萃取和反萃取”
①“水相C”中的溶质主要是Na2SO4和________(写化学式)。
②实验室称取100g原料(含钴11.80%),反萃取时得到浓度为0.036mol·L-1的CoCl2溶液5L,忽略损耗,钴的产率=____________(产率= )。
)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com