
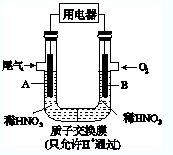
 某化学小组构想将汽车尾气(NO、NO2)转化为重要的化工原料HNO3,其原理如图所示,其中A、B为多孔材料.下列说法正确的是( )
某化学小组构想将汽车尾气(NO、NO2)转化为重要的化工原料HNO3,其原理如图所示,其中A、B为多孔材料.下列说法正确的是( )| A、电极A表面反应之一为NO2-e-+H2O═NO3-+2H+ |
| B、电极B附近的c(NO3-)增大 |
| C、电解质溶液中电流的方向由B到A,电子的流向与之相反 |
| D、该电池工作时,每转移4 mol电子,生成22.4LO2 |


科目:高中化学 来源: 题型:
| A、Na+ Fe3+ Cl- I- |
| B、Ca2+、K+、Cl-、HCO3- |
| C、Mg2+ Na+ SO42-Cl- |
| D、K+ Na+ SO42-NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、P、Q、R、S的浓度相等 |
| B、P、Q、R、S在容器中共存 |
| C、P、Q、R、S的浓度不再变化 |
| D、P、Q的反应速率相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实例 | 影响速率的因素 | 如何影响 |
| 粉状的碳酸钙与盐酸反应比块状的碳酸钙反应快 | 反应物颗粒的大小(或 反应物接触面积的大小) | 反应物的颗粒越小(或 反应物接触面积越大),反应速率越快 |
| 夏天食物易变质 | ||
| 硫在氧气中比在空气中燃烧快 | ||
| 双氧水与二氧化锰混合可快速产生氧气 | ||
| 工业合成氨通常要在高压下进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2H2(g)+O2(g)═2H2O(g)△H=-Q1 2H2(g)+O2(g)═2H2O(l)△H=-Q2 | ||||
| B、S(g)+O2(g)═SO2(g)△H=-Q1 S(s)+O2(g)═SO2(g)△H=-Q2 | ||||
C、C(s)+
| ||||
D、H2(g)+Cl2(g)═2HCl(g)△H=-Q1
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、根据物质能否溶于水,将物质分为易溶物质和难溶物质 |
| B、根据化学反应中是否有单质生成把化学反应分为氧化还原反应和非氧化还原反应 |
| C、根据物质中是否含碳元素,将物质分为无机物和有机物 |
| D、根据酸中是否含有氧元素,将酸分为无氧酸和含氧酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com