
 �ܹ����CH3COOH ��
�ܹ����CH3COOH �� ��
�� ��
�� �����
�����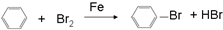 ��
�� ��
�� ��
�� ���� ��1����2������������ͨʽCnH2n+2�����㣻
��3������ʽ��ͬ���ṹ��ͬ���л��ﻥΪͬ���칹�壻
��4������������ζ��������ȡ�������л�����Һ�巢��ȡ����Ӧ����Ϊ���������嵥�ʷ�Ӧ�����屽��
��5��̼ԭ�Ӹ���Խ�࣬�е�Խ����̼ͬԭ�Ӹ�����������֧����ķе�ͣ�
��6���Ҵ���CuO��Ӧ������ȩ��Cu��ˮ��
��7����������ˮΪ���壬��Ӧǰ����������û�з����ı䣬��ǰ������Ļ�ѧ��������ȣ������������������г��ȼ�յ�ͨʽ���㣻
��8���������Ҵ�����������Ӧ��������������ˮ��
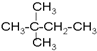
��� �⣺��1��������ͨʽΪ��CnH2n+2����Է�������Ϊ44����������12n+2n+2=44������n=3���������ķ���ʽΪC3H8���ṹ��ʽΪCH3CH2CH3��
�ʴ�Ϊ��CH3CH2CH3��
��2����������ͨʽCnH2n+2����2n+2=14�����n=6������ΪC6H14��
�ʴ�Ϊ��C6H14��
��3����ۻ�Ϊͬ���칹����Ǣߣ����߷���ʽ��ͬ���ṹ��ͬ��
�ʴ�Ϊ���ߣ�
��4������������ζ��������ȡ�����л���Ϊ������������������������Һ�巢��һȡ����Ӧ�Ļ�ѧ����ʽΪ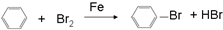 ��
��
�ʴ�Ϊ��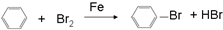 ��
��
��5��̼ԭ�Ӹ���Խ�࣬�е�Խ����̼ͬԭ�Ӹ�����������֧����ķе�ͣ���е�Ϊ�ܣ��ۣ���٣�
�ʴ�Ϊ���ܣ��ۣ���٣�
��6���Ҵ���CuO��Ӧ������ȩ��Cu��ˮ����ӦΪ ��
��
�ʴ�Ϊ�� ��
��
��7����120�棬1.01��105Pa�����£����ɵ�ˮΪ��̬����CxHy+��x+$\frac{y}{4}$��O2$\stackrel{��ȼ}{��}$xCO2+$\frac{y}{2}$H2O��g������ 1+��x+$\frac{y}{4}$��=x+$\frac{y}{2}$�����y=4��������ʽ����ԭ����ĿΪ4��
Ϊ���飬����Ϊͬϵ�
�ʴ�Ϊ���٣�ͬϵ�
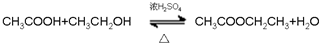
��8���������Ҵ�����������Ӧ��������������ˮ���÷�ӦΪ ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼���л���Ľṹ�����ʣ����չ����������ʵĹ�ϵ���л���ӦΪ���Ĺؼ������ط�����Ӧ�������Ŀ��飬�ۺ��Խ�ǿ����Ŀ�ѶȲ���


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������һ��Ԫ����ɵ����ʣ�����һ��Ԫ����ɵ�����һ���ǵ��� | |
| B�� | ��Ԫ������Ԫ��ԭ�ӵ�������������ͬ�����Զ��߾������ƵĻ�ѧ���� | |
| C�� | ��Һ���о���������������������С���������ʵ���������һ����С | |
| D�� | ����Һ��ʹ��̪��Һ��죬�����̪��Һ�����һ���Ǽ���Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
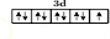 ��
��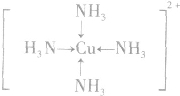 ���������İ���ͭ���ӣ�[Cu��NH3��4]2+�е�����NH3������Cl-ȡ�����ܵõ����ֲ�ͬ�ṹ�IJ����[Cu��NH3��4]2+�Ŀռ乹��Ϊƽ�������Σ�
���������İ���ͭ���ӣ�[Cu��NH3��4]2+�е�����NH3������Cl-ȡ�����ܵõ����ֲ�ͬ�ṹ�IJ����[Cu��NH3��4]2+�Ŀռ乹��Ϊƽ�������Σ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C��N��O | B�� | S��P��Si | C�� | F��O��Br | D�� | H��Ca��Al |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| H2O2��Ũ�ȣ����������� | �¶ȣ��棩 | ���� | |
| A | 5 | 10 | ��ʹ�� |
| B | 5 | 15 | ʹ��FeCl3 |
| C | 15 | 20 | ��ʹ�� |
| D | 15 | 30 | ʹ��MnO2 |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ױ������е�����ԭ�ӿ��ܹ�ƽ�� | |
| B�� | CH2�TCH-C6H5�����е�����ԭ�ӿ��ܹ�ƽ�� | |
| C�� | ��������е�����ԭ�ӿ��ܹ�ƽ�� | |
| D�� | ���ȼ������Ϊ��������ṹ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| �¶ȡ� | 10 | 30 | 60 | 90 |
| Ũ�ȣ�mol/L�� | 0.21 | 0.17 | 0.14 | 0.10 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
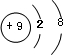 ����Ԫ�����������ǿ��Ԫ���γɵĻ�����ĵ���ʽΪ
����Ԫ�����������ǿ��Ԫ���γɵĻ�����ĵ���ʽΪ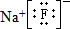 ���û������д��ڵĻ�ѧ��Ϊ���Ӽ� ��ѡ����Ӽ������ۼ�������
���û������д��ڵĻ�ѧ��Ϊ���Ӽ� ��ѡ����Ӽ������ۼ��������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
| �� | E | A | B | ||
| C | �� | D |

�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com