
【题目】下列微粒中,半径最大的是
A.S2-离子B.Cl-离子C.Cl原子D.K+离子
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】如图是草酸溶液中H2C2O4、HC2O4-、C2O42-三种微粒的分布分数(某微粒物质的量浓度与三种微粒物质的量浓度和的比值)与pH的关系,下列有关说法不正确的是

A. pH=5 的溶液中c(C2O42-)>c(HC2O4-)
B. NaHC2O4溶液中:c(OH-)+c(C2O42-)=c(H+)+c(H2C2O4)
C. 向NaHC2O4溶液中加强酸至pH与a点对应时,溶液中 2c(Na+)=c(HC2O4-)+ c(H2C2O4)
D. 为使溶液中c(c(HC2O4-)尽可能多一些,溶液的pH最好控制在2.7左右
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一些常见有机物的转化如图下列说法正确的是( )

A. 上述有机物中只有C6H12O6属于糖类物质 B. 物质A和B都属于电解质
C. 物质C和油脂类物质互为同系物 D. 转化1可在人体内完成,该催化剂属于蛋白质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组将一批电子废弃物简单处理后,得到含Cu、Al、Fe及少量Au、Pt等金属的混合物,并设计如下制备硫酸铜晶体和无水氯化铁的方案:
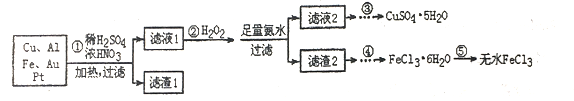
已知:Cu2++4NH3·H2O=[Cu(NH3)4]2++4H2O
请回答下列问题:
(1)步骤①Cu与酸反应的离子方程式为_________________________。
(2)步骤②加H2O2的作用是______________,滤渣2为(填化学式)__________。
(3)步骤⑤不能直接加热脱水的理由是________
(4)若滤液1中Cu2+的浓度为0.02mol·L-1,则氢氧化铜开始沉淀时的pH=________(已知:Ksp[Cu(OH)2]=2.0x10-20)
(5)已知:2Cu2++4I-=2CuI↓+I2 I2+2S2O32-=2I-+S4O62-
某同学为了测定CuSO4·5H2O产品的质量分数可按如下方法:取3.00g产品,用水溶解后,加入足量的KI溶液,充分反应后过滤、洗涤,将滤液稀释至250mL,取50mL加入淀粉溶液作指示剂,用0.080mol·L-1Na2S2O3标准溶液滴定,达到滴定终点的依据是______________。
四次平行实验耗去Na2S2O3标准溶液数据如下:
实验序号 | 1 | 2 | 3 | 4 |
消耗Na2S2O3标准溶液(mL) | 25.00 | 25.02 | 26.20 | 24.98 |
此产品中CuSO4·5H2O的质量分数为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电讯器材元件材料MnCO3在空气中加热易转化为不同价态锰的氧化物,其固体残留率随温度变化如下图。下列说法不正确的是( )
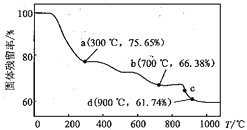
A. a 点剩余固体中n(Mn) : n(O) = 1 : 2
B. b 点对应固体的成分为Mn3O4
C. c 点发生的反应为2MnO2 △ 2MnO+O2↑
D. d 点对应固体的成分为MnO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求完成下列化学方程式或离子方程式。
(1)工业用电解饱和食盐水制氯气的化学方程式为____________________。
(2)向新制的Na2S 溶液中滴加新制的氯水的离子方程式为_______________。
(3)氯化铝与过量NaOH 溶液反应的离子方程式为____________________。
(4)乙醇催化氧化制乙醛的化学方程式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化钠是重要的化工原料,大多采用无水芒硝(Na2SO4)—炭粉还原法制备,原理为:Na2SO4+2CNa2S+2CO2↑。其主要流程如下:

(1) 上述流程中采用稀碱液比用热水更好,理由是________________________________________________________________________。
(2) 已知:I2+2S2O32-===2I-+S4O62-。所制得的Na2S·9H2O晶体中含有Na2S2O3·5H2O等杂质。为测定产品的成分,进行下列实验,步骤如下:
a. 取试样10.00 g配成500.00 mL溶液。
b. 取所配溶液25.00 mL于碘量瓶中,加入过量ZnCO3悬浊液除去Na2S后,过滤,向滤液中滴入2~3滴淀粉溶液,用0.050 00 mol·L-1 I2溶液滴定至终点,用去5.00 mL I2溶液。
c. 再取所配溶液25.00 mL于碘量瓶中,加入50.00 mL 0.050 00 mol·L-1的I2溶液,并滴入2~3滴淀粉溶液,振荡。用标准Na2S2O3溶液滴定多余的I2,用去15.00 mL 0.100 0 mol·L-1 Na2S2O3溶液。
①步骤b中用ZnCO3除去Na2S的离子方程式为____________。
②判断步骤c中滴定终点的方法为______________。
③计算试样中Na2S·9H2O和Na2S2O3·5H2O的质量分数,写出计算过程__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com