
����Ŀ����֪�����Ȼ�ѧ����ʽ����H2��g��+ ![]() O2��g���TH2O��l����H=��285.8kJmol��1
O2��g���TH2O��l����H=��285.8kJmol��1
��H2��g��+ ![]() O2��g���TH2O��g����H=��241.8kJmol��1
O2��g���TH2O��g����H=��241.8kJmol��1
��C��s��+ ![]() O2��g���TCO��g����H=��110.5kJmol��1
O2��g���TCO��g����H=��110.5kJmol��1
��C��s��+O2��g���TCO2��g����H=��393.5kJmol��1
�ش����и����⣺
��1��������Ӧ�����ڷ��ȷ�Ӧ���� ��
��2��H2��ȼ����Ϊ��C��ȼ����Ϊ ��
��3��ȼ��10g H2����Һ̬ˮ���ų�������Ϊ ��
��4��COȼ�յ��Ȼ�ѧ����ʽΪ����ȼ���ȡ�HΪ ��
���𰸡�
��1���٢ڢۢ�
��2��285.8 kJ?mol��1��393.5kJ?mol��1
��3��1429.0kJ
��4��CO��g��+O2��g���TCO2��g����H=��283.0 kJ?mol��1����283.0 kJ?mol��1
���������⣺��1�����ʵ�ȼ�վ�Ϊ���ȷ�Ӧ�����٢�Ϊ������ȼ�գ��ۢ�ΪC��ȼ�գ��ʢ٢ڢܾۢ�Ϊ���ȷ�Ӧ�����Դ��ǣ��٢ڢۢܣ���2��ȼ������ָ��101kPʱ��1mol��ȼ����ȫȼ�������ȶ���������ʱ���ų���������CԪ��ת��ΪCO2 �� HԪ��ת��ΪҺ̬ˮ���ʷ�Ӧ��Ϊ������ȼ���ȵ��Ȼ�ѧ����ʽ����������ȼ����Ϊ285.8kJmol��1����Ӧ��ΪC��ȼ���ȵ��Ȼ�ѧ����ʽ����C��ȼ����Ϊ393.5kJmol��1 �� ���Դ��ǣ�285.8 kJmol��1��393.5kJmol��1����3��10g���������ʵ���Ϊ5mol����1mol����ȼ������Һ̬ˮʱ�ų�285.8KJ����5mol����ȼ������Һ̬ˮʱ�ų�������Ϊ285.8kJmol��1��5mol=1429.0 kJ�����Դ��ǣ�1429.0kJ�� ��4�����ݸ�˹���ɿ�֪�����ܩ��ۿɵ�CO��ȼ�շ�ӦΪ��CO��g��+O2��g���TCO2��g����H=��283.0 kJmol��1 �� ��CO��ȼ���ȡ�HΪ��283.0 kJmol��1 �� ���Դ��ǣ�CO��g��+O2��g���TCO2��g����H=��283.0 kJmol��1����283.0 kJmol��1 ��
�����㾫����������Ĺؼ������������ȷ�Ӧ�ͷ��ȷ�Ӧ�����֪ʶ�����ջ�ѧ�ϰ����������Ļ�ѧ��Ӧ��Ϊ���ȷ�Ӧ����ѧ�ϰѷų������Ļ�ѧ��Ӧ��Ϊ���ȷ�Ӧ���Լ��Է�Ӧ�Ⱥ��ʱ�����⣬�˽��ڻ�ѧ��Ӧ�зų������յ�������ͨ���з�Ӧ�ȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CH4����һ����Ҫ����Դ��Ҳ��һ����Ҫ�Ļ���ԭ�ϡ�
(1)����ĽṹʽΪ________
(2)������·ֽ�����������̼�����ܱ������н��д˷�ӦʱҪͨ����������ʹ���ּ���ȼ�գ���Ŀ����_________��
(3)��CH4Ϊȼ�Ͽ���Ƴɽṹ������ת���ʸߡ��Ի�������Ⱦ��ȼ�ϵ�أ��乤��ԭ����ͼ��ʾ����ͨ��a����ĵ缫����Ϊ_____,ͨ��b����ĵ缫��Ӧʽ_______.(���ӽ���Ĥֻ����H+ͨ��)

(4)��һ���¶Ⱥʹ��������£�CH4��CO2��ֱ��ת�������ᣬ����ʵ�֡����š���һ���о�����
���ڲ�ͬ�¶��£������Ĵ�Ч���������������������ͼ��ʾ����÷�Ӧ������¶�Ӧ������_________���ҡ�
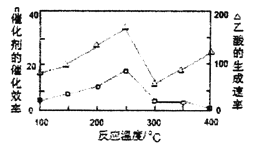
�ڸ÷�Ӧ��������Ч�ɷ�Ϊƫ������ͭ(CuAlO2,������)����CuAlO2�ܽ���ϡ���������������β��ų�NO���壬�����ӷ���ʽΪ_________
(5)CH4��ԭ���Ǵ���NOx�����һ�ַ�������֪һ��������CH4��NOx��Ӧת��ΪN2��CO2,����״����8.96LCH4�ɴ���22.4LNOx,��xֵΪ________.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ��101kPaʱ������������ȼ�������Ȼ�������������仯���������й�˵���в���ȷ���ǣ� �� 
A.1 molH2�еĻ�ѧ������ʱ��Ҫ����436 kJ����
B.2 molHCl�����еĻ�ѧ���γ�ʱҪ�ͷ�862 kJ����
C.�˷�Ӧ���Ȼ�ѧ����ʽΪ��H2��g��+Cl2��g���T2HCl��g����H=+183 kJ/mol
D.�˷�Ӧ���Ȼ�ѧ����ʽΪ�� ![]() H2��g��+
H2��g��+ ![]() Cl2��g���THCl��g����H=��91.5 kJ/mol
Cl2��g���THCl��g����H=��91.5 kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л��������ܽ⡢���ˡ������IJ����ﵽ����Ŀ�ĵ��ǣ� ��
A. ��������Ȼ��ƵĻ����
B. ʯ��ʯ����ɳ�Ļ����
C. ����ƾ��Ļ����
D. ��ɳ���Ȼ��ƵĻ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2016��IUPAC����117��Ԫ��ΪTs���������� ![]() ����ti��n����Ts��ԭ�Ӻ���������������7������˵������ȷ���ǣ�������
����ti��n����Ts��ԭ�Ӻ���������������7������˵������ȷ���ǣ�������
A. Ts�ǵ������ڵڢ�A��Ԫ�� B. Ts��ͬλ��ԭ�Ӿ�����ͬ�ĵ�����
C. Ts��ͬ��Ԫ���зǽ��������� D. ������Ϊ176��TS���ط����� ![]() Ts
Ts
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ�鷽���Ʊ����壬��������ʵ�õ���(����)
A.п����ϡ���ᷴӦ�Ʊ�H2
B.�����Ͱ�ˮ�μӵ����Ƶ���ʯ����NH3
C.����������ϡ���ᷴӦ�Ʊ�SO2
D.����ʯ��Ũ���ᷴӦ�Ʊ�CO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ʊ�����ķ������ټ���ϡ�����MnO2������������ϡH2SO4�ʹ���ʯ�Ʊ�������̼������ϡ�����п���Ʊ����������˲��õķ�����(����)
A.ֻ�Т�
B.ֻ�Тٺ͢�
C.ֻ�Т�
D.�٢ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������к���Ԫ�ء��Ӻ�������ȡ�������²��裺��ͨ������Cl2���ڽ��������ճɻҺ������ˮ���裻�ۼ�CCl4���ܹ��ˡ������IJ���˳����(����)
A.�٢ڢۢ�
B.�ڢ٢ۢ�
C.�٢ۢڢ�
D.�ڢܢ٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵ�飺
��1��ȷ��ȡ25.00mL���������Һ����ѡ�õ������� ��
��A��50mL��Ͳ ��B��10mL��Ͳ ��C��50mL��ʽ�ζ��� ��D��50mL��ʽ�ζ���
��2�������к͵ζ�ʱ�����Ȳ�Ӧ������ʢ��Һ��ϴ�������� ��
��A����ʽ�ζ��� ��B����ʽ�ζ��� ��C����ƿ ��D����Ͳ
��3��ij�ռ���Ʒ�к����������������õ����ʣ�Ϊ�˲ⶨ�䴿�ȣ��������µζ�������
��A����250mL������ƿ�ж�������250mL�ռ���Һ��
��B������Һ����ȡ25mL�ռ���Һ����ƿ�У������뼸�μ�����ָʾ����
��C����������ƽ��ȷ��ȡ�ռ���ƷWg�����ձ���������ˮ�ܽ⣻
��D�������ʵ���Ũ��ΪcmolL��1�ı�������Һװ������ϴ������ʽ�ζ����У�����Һ�沢������ʼ����ΪV1mL��
��E������ƿ�µ�һ�Ű�ֽ���ζ�����ɫΪֹ�����¶���ΪV2mL��
�ʹ�����������⣺
����ȷ���������ǣ��ñ����ĸ��գ�������D����
�ڹ۲�ζ�����Һ��ĸ߶�ʱӦע�⣺ ��
��E����IJ���������ƿ�µ�һ�Ű�ֽ�������� ��
��D����IJ�����Һ��Ӧ������ �� ���첿��Ӧ�� ��
��ijѧ��ʵ��ʱ����ƿ�ô����ռ���Һ��ϴ����ⶨ���ռ���Һ��Ũ��ƫ����ƫ����
���ռ���Ʒ���ȵļ��㹫ʽ�� ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com