
【题目】根据下列图示所得出的结论正确的是( )
A.图甲表示用0.100mol·L-1AgNO3滴定50.0mL0.0500mol·L-1Cl-溶液的滴定曲线,说明m点时溶液中c(Ag+)与c(Cl-)相等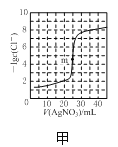
B.图乙表示室温下醋酸溶液中H+浓度与醋酸浓度的关系,说明醋酸浓度越大,醋酸的电离程度越大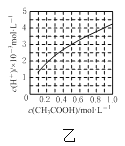
C.图丙是稀释相同体积、相同pH的HNO2和CH3COOH稀溶液时,溶液的pH随加水体积的变化,说明所含溶质的物质的量浓度x点大于y点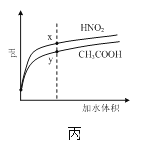
D.图丁是在恒压、NO和O2的起始浓度一定的条件下,催化反应相同时间,测得不同温度下NO转化为NO2的转化率随温度的变化,说明Z点时v(正)<v(逆)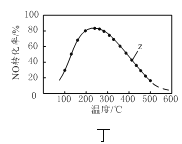
【答案】A
【解析】
A.图甲m点指的是:50.0mL0.0500mol·L-1Cl-溶液和25.0mL 0.100mol·L-1AgNO3二者恰好反应,则c(Ag+)与c(Cl-)相等,A项正确;
B. 图乙表示室温下醋酸溶液中H+浓度与醋酸浓度的关系,说明醋酸浓度越大,溶液酸性越强,但是醋酸的电离程度越小,B项错误;
C.稀释过程中HNO2的变化较大,酸性较强,等pH的二者溶液,HNO2的浓度较小,稀释相同的倍数,得到的HNO2的浓度较小,x点小于y点,C项错误;
D.恒压起始浓度不变,催化剂存在,反应相同时间,升温速率加快,有两种情况。一、温度升高到二百多度,反应达到平衡,继续升温平衡向吸热方向移动,该反应正向放热,故往逆向移动,此时Z点时v(正)<v(逆);二、温度升高,降低了催化剂的活性,速率减慢,还未达到平衡,Z点时v(正)>v(逆);D项错误;
答案选A。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】草酸(H2C2O4)是一种二元弱酸。常温下向H2C2O4溶液中滴加NaOH溶液,混合溶液里lgX [X表示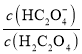 或
或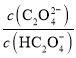 ]随pH的变化关系如图所示。下列说法不正确的是( )
]随pH的变化关系如图所示。下列说法不正确的是( )
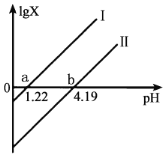
A.由图可知H2C2O4的K2的数量级是10-5
B.b点为恰好完全反应点
C.c(HC2O4-)>c(C2O42-)>c(H2C2O4)对应1.22<pH<4.19
D.c(Na+)= c(HC2O4-)+2c(C2O42-)对应pH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数值。下列有关叙述正确的是( )
A. 14 g乙烯和丙烯混合气体中的氢原子数为2NA
B. 1 mol N2与4 mol H2反应生成的NH3分子数为2NA
C. 1 mol Fe溶于过量硝酸,电子转移数为2NA
D. 标准状况下,2.24 L CCl4含有的共价键数为0.4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:KClO3+6HCl(浓)===KCl+3Cl2↑+3H2O。如图所示,将少量试剂分别放入培养皿中的相应位置,实验时将浓盐酸滴在KClO3晶体上,并用表面皿盖好。下表中由实验现象得出的结论完全正确的是

选项 | 实验现象 | 结论 |
A | 滴有KSCN的FeCl2溶液变红 | Cl2具有还原性 |
B | 滴有酚酞的NaOH溶液褪色 | Cl2具有酸性 |
C | 紫色石蕊溶液先变红后褪色 | Cl2具有漂白性 |
D | KI淀粉溶液变蓝色 | Cl2具有氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对溴苯乙烯与丙烯的共聚物是一种高分子阻燃剂,具有低毒、热稳定性好等优点。完成下列填空:
(1)写出该共聚物的结构简式________。
(2)实验室由乙苯制取对溴苯乙烯,需先经两步反应制得中间体![]() 。写出该两步反应所需的试剂及条件_______、__________。
。写出该两步反应所需的试剂及条件_______、__________。
(3)将![]() 与足量氢氧化钠溶液共热得到A,A在酸性条件下遇FeCl3溶液不显色。A的结构简式为_______。由上述反应可推知_________。由A生成对溴苯乙烯的反应条件为______。
与足量氢氧化钠溶液共热得到A,A在酸性条件下遇FeCl3溶液不显色。A的结构简式为_______。由上述反应可推知_________。由A生成对溴苯乙烯的反应条件为______。
(4)丙烯催化二聚得到2,3-二甲基-1-丁烯,B与2,3-二甲基-1-丁烯互为同分异构体,且所有碳原子处于同一平面,写出B的结构简式_______。设计一条由2,3-二甲基-1-丁烯制备B的合成路线_______。(合成路线常用的表示方式为:![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物Z是合成一种镇痛药的中间体,可通过如下反应制得。下列说法正确的是( )
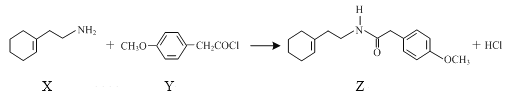
A.化合物X既能与盐酸反应,也能与NaOH溶液反应
B.化合物Y能使酸性KMnO4溶液褪色
C.化合物Z的分子式为C17H24O2N
D.化合物X与Br2加成所得产物分子中含有2个手性碳原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是第3周期11~17号元素某些性质变化趋势的柱形图,下列有关说法中正确的是( )

A. y轴表示的可能是第一电离能
B. y轴表示的可能是电负性
C. y轴表示的可能是原子半径
D. y轴表示的可能是原子形成简单离子转移的电子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数小于等于36的Q、W、X、Y、Z五种元素原子序数依次增大,其中Q是原子半径最小的元素,W和Y的基态原子2p能级所含成单电子数均为2,Z的基态原子核外含有13种运动状态不同的电子。回答下列问题(涉及元素时用对应的元素符号表示):
(1)X、Y、Z三种元素的第一电离能由大到小的顺序是___。
(2)1molQWX与1molWQ2Y所含σ键的比值为___。
(3)根据等电子体理论可以预测WXY-的空间构型为___。
(4)一种由X和Z两种元素形成化合物的晶胞如图所示,该晶胞的化学式为___。
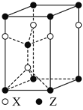
(5)实验室合成一种由W和X两种元素形成的化合物,该化合物具有空间网状结构,其中每个W原子与4个X原子形成共价键,每个X原子与3个W原子形成共价键。
①该化合物的化学式为___。
②该化合物所属晶体类型为___晶体,预测其熔点应___金刚石(填“高于”或“低于”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肼(H2NNH2)是一种高能燃料,有关化学反应的能量变化如下图所示。已知断裂1 mol化学键所需的能量(kJ):N≡N为942、O=O为500、N—N为154,则断裂1 mol N—H键所需的能量(kJ)是:

A. 194 B. 391 C. 516 D. 658
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com