
 )分别为?a、b、c(单位为mol/L),则下列判断正确的是
)分别为?a、b、c(单位为mol/L),则下列判断正确的是| A.a=b=c | B.c>a>b | C.b>a>c | D.a>c>b |
科目:高中化学 来源:不详 题型:单选题
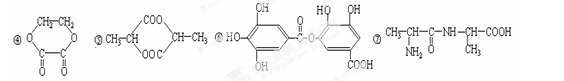
| A.①②⑤⑦ | B.②④⑤⑦ | C.②⑤⑥⑦ | D.①④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.Ⅱ、Ⅲ溶液分别与10g铝粉充分反应,生成H2的量Ⅲ一定更多 |
| B.Ⅰ与Ⅱ等体积混合后,溶液中的c(CH3COO-)为原溶液浓度的1/2 |
| C.将Ⅰ和Ⅲ等体积混合后,溶液pH一定小于7 |
| D.四种溶液各10mL分别加水稀释至100mL后,溶液的pH:Ⅲ>Ⅳ>Ⅰ>Ⅱ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.盐的电离平衡被破坏 | B.水的电离程度一定会增大 |
| C.溶液的pH一定会增大 | D.(H+)与c(OH-)的乘积一定会增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com