
【题目】2019年获诺贝尔化学奖的是约翰·班尼斯特·古迪纳夫(John B.Goodenough)、迈克尔·斯坦利·威廷汉(M.Stanley Whittlingham)和吉野彰( Akira Yoshino)三位科学家,他们在锂离子电池发展上做出了突出贡献。锂离子电池是将层状石墨加导电剂及黏合剂涂在铜箔基带上,将钴酸锂(LiCoO2)涂在铝箔上制作而成,利用锂离子在两极上的嵌入和脱嵌进行充、放电,其原理如图所示。下列说法错误的是

LiCoO2+6C=Li1-xCoO2+LixC6
A.石墨加导电剂及黏合剂涂在铜箔基带上作锂离子电池的负极
B.充电时Li+从石墨层状结构中脱嵌,进入电解质
C.放电时的正极反应为Li1-xCoO2+xLi++xe-=LiCoO2
D.锂离子电池常用非水液态有机电解质作电解液
【答案】B
【解析】
从图中可以看出,左侧为铝箔,右侧是石墨,放电过程中锂离子从石墨电极上脱嵌,铝箔电极上嵌入,充电过程中锂离子从铝箔电极上脱嵌,在石墨电极上嵌入。放电的方程式为LixC6+Li1-xCoO2=LiCoO2+6C,反之为充电的方程式。
A.从图中可以看出,右侧石墨电极中锂离子脱嵌,LixC6失去电子,做负极,A正确;
B.充电时锂离子从铝箔电极上脱嵌进入电解质,B错误;
C.放电时,正极为电解质中的Li+得电子与正极上的Li1-xCoO2结合生成LiCoO2,电极方程式为Li1-xCoO2+xLi++xe-=LiCoO2,C正确;
D.锂是活泼的金属,锂离子电池常用非水溶剂电解质作为电解液,当用水溶剂做电解质时,充电过程中易生成气体,影响使用安全和使用寿命,D正确;
故选B。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】2SO2(g)+O2(g)![]() 2SO3(g)是工业生产硫酸的重要步骤,T℃时该反应过程中的能量变化如图所示:
2SO3(g)是工业生产硫酸的重要步骤,T℃时该反应过程中的能量变化如图所示:
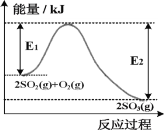
(1)2SO2(g)+O2(g)![]() 2SO3(g)ΔH=___________kJ·mol-1(
2SO3(g)ΔH=___________kJ·mol-1(![]() 含E1、E2的计算式表示)
含E1、E2的计算式表示)
(2)①下列措施不能使该反应速率加快的是___________。
A.升高温度 B.降低压强 C.使用催化剂
②若上述反应在恒容的密闭容器中进行,下列叙述中能说明该反应已达平衡状态的是___________。
A.SO3的浓度不再变化
B.SO2与SO3的物质的量相等
C.容器内气体的压强不再变化
D.单位时间内消耗1molO2,同时消耗2molSO2
(3)运用电化学原理可生产硫酸,总反应为2SO2+O2+2H2O=2H2SO4,装置如图所示。其中质子交换膜将该原电池分隔成氧化反应室和还原反应室,能阻止气体通过而允许H+通过。
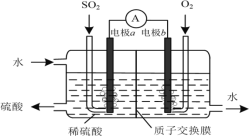
①该电池的负极是___________。(填“电极a”或“电极b”)
②H+通过质子交换膜时的移动方向是___________。
A.从左向右 B.从右向左
③通入O2的电极反应式是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知氯的非金属性比氮的强,某同学依据反应3Cl2+2NH3=6HCl+N2进行实验证,设计的实验装置如下:
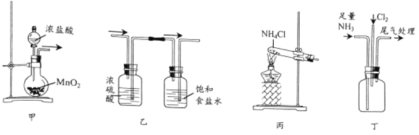
下列说法正确的是
A.可用图甲所示装置及药品制取Cl2B.可用图乙所示装置及气流方向净化Cl2
C.可用图丙所示装置及药品制取NH3D.可用图丁所示装置进行实验,瓶中有白烟产生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积不变的密闭容器中发生反应N2(g)+3H2(g)![]() 2NH3(g),下列叙述表示该反应处于化学平衡状态的是( )
2NH3(g),下列叙述表示该反应处于化学平衡状态的是( )
A.N2、H2、NH3的浓度之比为1∶3∶2
B.混合气体的密度不随时间变化
C.当有1molN≡N键断裂时,有6molN—H键断裂
D.单位时间内生成2amolNH3,同时消耗amolN2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家对一碳化学进行了广泛深入的研究并取得了一些重要成果。
(1)已知:CO(g)+2H2(g)![]() CH3OH(g) △H1=-90.1kJ/mol;
CH3OH(g) △H1=-90.1kJ/mol;
3CH3OH(g)![]() CH3CH=CH2(g)+3H2O(g) △H2=-31.0kJ/mol
CH3CH=CH2(g)+3H2O(g) △H2=-31.0kJ/mol
CO与H2合成CH3CH=CH2的热化学方程式为________。
(2)现向三个体积均为2L的恒容密闭容器I、II、Ⅲ中,均分别充入1molCO 和2mo1H2发生反应:CO(g)+2H2(g)![]() CH3OH(g) △H1=-90.1kJ/mol。三个容器的反应温度分别为Tl、T2、T3且恒定不变。当反应均进行到5min时H2的体积分数如图1所示,其中只有一个容器中的反应已经达到平衡状态。
CH3OH(g) △H1=-90.1kJ/mol。三个容器的反应温度分别为Tl、T2、T3且恒定不变。当反应均进行到5min时H2的体积分数如图1所示,其中只有一个容器中的反应已经达到平衡状态。
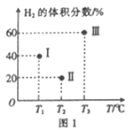
①5min时三个容器中的反应达到化学平衡状态的是容器_______(填序号)。
②0-5 min内容器I中用CH3OH表示的化学反应速率v(CH3OH)=_______。(保留两位有效数字)
(3)CO常用于工业冶炼金属,在不同温度下用CO 还原四种金属氧化物,达到平衡后气体中lgc(CO)/c(CO2)与温度(T)的关系如图2所示。下列说法正确的是_____(填字母)。
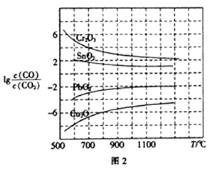
A.工业上可以通过增高反应装置来延长矿石和CO接触面积,减少尾气中CO的含量
B.CO用于工业冶炼金属铬(Cr)时,还原效率不高
C.工业冶炼金属铜(Cu) 时,600℃下CO的利用率比1000℃下CO的利用率更大
D.CO还原PbO2的反应△H>0
(4)一种甲醇燃料电池,使用的电解质溶液是2mol·L-1的KOH溶液。
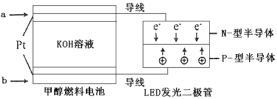
请写出加入(通入)a物质一极的电极反应式___________;每消耗6.4g甲醇转移的电子数为__________。
(5)一定条件下,用甲醇与一氧化碳反应合成乙酸可以消除一氧化碳污染。常温下,将a mol/L的醋酸与b mol/LBa(OH)2溶液等体积混合后,若溶液呈中性,用含a和b的代数式表示该混合溶液中醋酸的电离常数Ka为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三乙酸锰可作单电子氧化剂,用如下反应可以制取三乙酸锰:4Mn(NO3)2·6H2O+26(CH3CO)2O=4(CH3COO)3Mn +8HNO2+ 3O2↑+40CH3COOH。
(1)基态锰原子的价层电子排布式为__________。
(2) CH3COOH中碳原子的杂化形式为________。
(3) NO3-的空间构型是①______,与NO3-互为等电子体的分子的化学式为②______(任写一种)。
(4) CH3COOH能与H2O以任意比互溶的原因是____________________。
(5)某种镁铝合金可作为储钠材料,该合金晶胞结构如图所示,晶胞棱长为anm,该合金的化学式为①_______,晶体中每个镁原子周围距离最近的铝原子数目为②_______,该晶体的密度为③______g/cm3(阿伏伽德罗常数的数值用NA表示)。
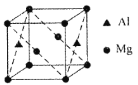
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温常压下,取下列四种有机物各1mol,分别在足量的氧气中燃烧,消耗氧气最多的是
A. C2H5OH B. CH4 C. C2H4O D. C3H8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】维拉帕米(又名异搏定)是治疗心绞痛和原发性高血压的药物,合成路线中某一步骤如图所示,下列说法中正确的是
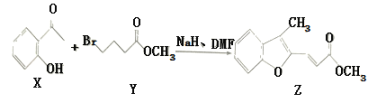
A. Y的分子式为C5H11O2 Br
B. 含苯环和羧基的ⅹ的同分异构体有4种
C. 可以用酸性高锰酸钾溶液鉴别X和Z
D. 1mol Z最多可与6mol H2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从化学成分上讲,油脂属于酯类化合物,对于油脂和酯类化合物认识正确的是( )
A. 油和脂肪都属于酯类化合物,所以油和脂肪的结构相似
B. 自然界中的油脂是混合物,以甘油三酯为主要成分
C. 酯类化合物是高分子化合物,自然界中的油脂是纯净物,以甘油三酯形式存在
D. 油脂属于酯类化合物,天然油脂是纯净物,没有固定熔、沸点
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com