
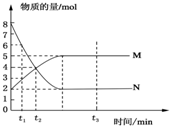
 在一定温度下,将两种气体M和N通入容积为2L的密闭容器中进行反应,M和N的物质的量与时间的关系如图所示,下列说法不正确的是( )
在一定温度下,将两种气体M和N通入容积为2L的密闭容器中进行反应,M和N的物质的量与时间的关系如图所示,下列说法不正确的是( )| A. | t2时刻M与N的物质的量浓度之比为1:1 | |
| B. | t2与t3时刻的混合气体的平均相对分子质量相等 | |
| C. | 反应物与生成物平衡时的物质的量浓度之比是2:5 | |
| D. | 0~t2内用M表示的平均反应速率是 1/t2mol/(L•min) |
分析 图象看出反应从开始到平衡,N的物质的量减小,应为反应物,物质的量变化值为8mol-2mol=6mol,M的物质的量增多,应为是生成物,物质的量的变化值为5mol-2mol=3mol,则有n(N):n(M)=6mol:3mol=2:1,可知反应的化学方程式为2N?M,结合反应的方程式可计算相关物质的反应速率以及物质的量浓度关系.
解答 解:由图象可知反应的化学方程式为2N?M,
A.t2时M与N的物质的量相等,则浓度相等,浓度之比为1:1,故A正确;
B.t2与t3时刻的混合气体的总物质的量不同,分别为8mol和7mol,则平均相对分子质量不等,故B错误;
C.反应物与生成物平衡时的物质的量分别为2mol、5mol,则平衡时的物质的量浓度之比是2:5,故C正确;
D.0~t2内用M表示的平均反应速率是$\frac{\frac{4mol-2mol}{2L}}{{t}_{2}min}$=$\frac{1}{{t}_{2}}$mol/(L•min),故D正确.
故选B.
点评 本题考查化学反应速率的影响因素以及平衡图象题目,题目难度不大,注意把握图象中曲线的变化特点.


科目:高中化学 来源: 题型:选择题
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.089 | 0.102 | 0.074 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A. | 氢化物的沸点为H2T<H2R | B. | 单质与稀盐酸反应的速率为L<Q | ||
| C. | M与T形成的化合物具有两性 | D. | L2+与R2-的核外电子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | B、C、D、E四种元素原子半径由大到小的顺序是:C>E>D>B | |
| B. | C和D两元素的最高价氧化物对应水化物的碱性:C>D | |
| C. | B和E两元素的气态氢化物热稳定性:B>E | |
| D. | A元素的气态氢化物与其最高价氧化物对应的水化物反应后产物中既含有离子键又含有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素 | X | Y | Z | W |
| 原子半径(nm) | 0.077 | 0.075 | 0.102 | 0.099 |
| 最高正价或最低负价 | +4 | +5 | -2 | -1 |
| A. | 1mol W的单质参加氧化还原反应时转移的电子数为2mol | |
| B. | X与W形成XW4时,各原子最外层均满足8电子稳定结构 | |
| C. | 0.3mol Cu分别与足量HYO3和H2ZO4的稀溶液反应均产生0.2mol气体 | |
| D. | Y的氢化物与W的氢化物反应的产物只含有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 密度相等,等体积的NO和 C2H6 (g) | B. | 常温常压下,等体积的NO和 C2H6 (g) | ||
| C. | 等温条件下,等体积的NO和 C2H6 (g) | D. | 常温常压下,等质量的NO和 C2H6 (g) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
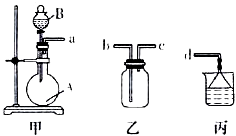 熟悉和使用中学化学实验中常见仪器及用品,是化学学习的基本要求.试回答以下问题:
熟悉和使用中学化学实验中常见仪器及用品,是化学学习的基本要求.试回答以下问题: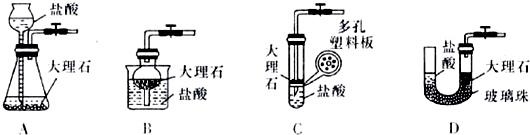
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl | B. | CH2═CH2+HCl→CH3CH2Cl | ||
| C. | 2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O | D. |  +HO-NO2$→_{60℃}^{浓硫酸}$ +HO-NO2$→_{60℃}^{浓硫酸}$ +H2O +H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com