
【题目】已知A、B、C为中学化学中常见的单质。室温下,A为固体,B和C均为气体。在适宜的条件下,它们可以按下面框图进行反应。
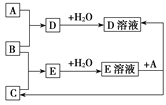
回答下列问题:
(1)A、B、C三种元素中的任意两种元素形成的化合物所属物质类别一定不是________。
①氢化物 ②酸 ③碱 ④盐 ⑤氧化物
(2)A、B、C三种元素中有一种是金属,则这种元素是A、B、C中的________,理由是__________。
(3)如果E溶液是一种强酸,则E的化学式为_________;
①A能否是铁:________,理由是____________;
②A能否是铜:________,理由是____________;
③A可能是________(任写两种)。
【答案】 ③⑤ A 常温下金属单质都不是气体 HCl 不能 若E为HCl,A为Fe,则D为FeCl3,盐酸与Fe不能生成FeCl3 不能 Cu与盐酸不反应 Al、Zn
【解析】A、B、C为中学化学中常见的单质。室温下,A为固体,常见为碳、钠、镁、铝、铁等,B、C为气体单质,常见有氯气、氧气、氢气、氮气等,固体A和气体B反应生成D,D能溶于水;B与C反应生成的E能溶于水,E溶液能与A反应,生成C和D,则E应为酸,C应为氢气,B为Cl2,E为HCl,D为金属和盐酸反应生成的氯化物盐,此盐可以直接由A和Cl2反应得到,说明A一定不是变价金属铁;A可能是金属钠、镁、铝等。(1)A为金属、B为氯气、C为氢气,由于不含氧元素,三种元素中的任意两种形成的化合物所属物质类别可以为酸、盐、氢化物,一定不是碱、氧化物,答案选③⑤;(2)A、B、C三种元素中有一种是金属,则三种元素中可能是金属的是A,因金属单质在室温下不是气态物质;(3)E溶液是一种强酸,应为盐酸,①若E为HCl,A为Fe,则D为FeCl3,盐酸与Fe反应不能生成FeCl3,所以A不能是铁:②Cu与盐酸不反应,因此A不可能是铜;③根据以上分析可知A可能是Al、Zn等。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列关于化学实验的说法中,符合实验安全要求的是( )
A. 制备氯气时严格检查装置的气密性,并设置尾气吸收装置
B. 用点燃的火柴在液化气钢瓶口检验是否漏气
C. 为防止药品污染,实验结束后,用剩的浓硝酸可倒入垃圾箱
D. 进入地下矿井中可用火把照明
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】材料是人类赖以生存和发展的重要物质基础.有机高分子材料的出现是材料发展史上的一次重大突破.下更物质中含有有机高分子材料的是( )
A.普通水泥
B.普通玻璃
C.汽车轮胎
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某物质的球棍模型如图所示,关于该物质的说法正确的是( ) 
A.该物质的结构简式为 
B.该物质可以发生加成反应
C.该物质既可以与强酸反应,但不可以与强碱反应
D.该物质不可以聚合成高分子物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自然界中,金属元素大多以化合态存在,通过金属冶炼得到金属单质.工业上生产Na、Ca、Mg都用电解其熔融的氯化物,但生产钾是用金属钠和熔化的KCl在一定的条件下反应制取:KCl+NaNaCl+K+Q (Q<0) 有关数据如表:
熔点℃ | 沸点℃ | 密度 (g/cm3) | |
Na | 97.8 | 882.9 | 0.97 |
K | 63.7 | 774 | 0.86 |
NaCl | 801 | 1413 | 2.165 |
KCl | 770 | 1500 | 1.984 |
(1)请结合平衡移动理论分析,为什么能用该反应制备金属钾. .
(2)在常压下金属钾转为气态从反应混合物中分离的最低温度约为℃,而反应的最高温度应低于℃.
(3)在制取金属钾的过程中,为了提高原料的转化率可采取的措施有 . (任写两点)
(4)相比于电解熔融氯化钾,此方法的优点有
(5)常压下,当反应温度升高到900℃时,该反应的平衡常数可表示为k=
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将足量的CO2不断通入NaOH、Ca (OH)2、NaAlO2的混合溶液中,则生成沉淀的物质的量与通入CO2的体积的关系可表示为

A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是制备和研究乙炔性质的实验装置图,有关说法不正确的是( ) 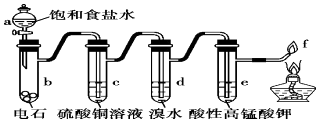
A.用蒸馏水替代a中饱和食盐水产生的乙炔更为纯净
B.c(过量)的作用是除去影响后续实验的杂质
C.d、e中溶液褪色的原理不同
D.f处产生明亮、伴有浓烟的火焰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组对过量炭粉与氧化铁反应的气体产物成分进行研究. 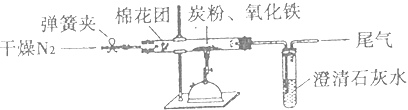
(1)提出假设 ①该反应的气体产物是CO2 .
②该反应的气体产物是CO.
③该反应的气体产物是 .
(2)设计方案 如图所示,将一定量的氧化铁在隔绝空气的条件下与过量炭粉完全反应,测定参加反应的碳元素与氧元素的质量比.
查阅资料
氮气不与碳、氧化铁发生反应.实验室可以用氯化铵饱和溶液和亚硝酸钠(NaNO2)饱和溶液混合加热反应制得氮气.请写出该反应的离子方程式: .
(3)实验步骤 ①按如图连接装置,并检查装置的气密性,称取3.20g氧化铁、2.00g碳粉混合均匀,放入10.38g的硬质玻璃管中;
②加热前,先通一段时间纯净干燥的氮气;
③停止通入N2后,夹紧弹簧夹,加热一段时间,澄清石灰水(足量)变浑浊;
④待反应结束,再缓缓通入一段时间的氮气.冷却至室温,称得硬质玻璃管和固体总质量为53.02g;
⑤过滤出石灰水中的沉淀,洗涤、烘干后称得质量为1g.步骤②、④中都分别通入N2 , 其作用分别为 .
(4)数据处理 试根据实验数据分析,写出该实验中氧化铁与碳发生反应的化学方程式: .
(5)实验优化 学习小组有同学认为应对实验装置进一步完善.
①甲同学认为:应将澄清石灰水换成Ba(OH)2溶液,其理由是 .
②从环境保护的角度,请你再提出一个优化方案: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com