
【题目】如图是制备和研究乙炔性质的实验装置图,有关说法不正确的是( ) 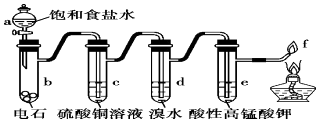
A.用蒸馏水替代a中饱和食盐水产生的乙炔更为纯净
B.c(过量)的作用是除去影响后续实验的杂质
C.d、e中溶液褪色的原理不同
D.f处产生明亮、伴有浓烟的火焰
科目:高中化学 来源: 题型:
【题目】下列实验设计中能达到预期目的的是( )
A. 用酒精萃取碘水中的碘,将碘的酒精溶液从分液漏斗的上口倒出
B. 在沸水中逐滴加入FeCl3溶液,继续煮沸至溶液呈红褐色即可得到Fe(OH)3胶体。
C. 将氢气和氧气的混合气体通过灼热的氧化铜除去氢气
D. 氯酸钾和二氧化锰的混合物充分加热后可用溶解、过滤、蒸发的方法分离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C为中学化学中常见的单质。室温下,A为固体,B和C均为气体。在适宜的条件下,它们可以按下面框图进行反应。
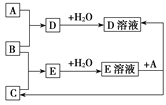
回答下列问题:
(1)A、B、C三种元素中的任意两种元素形成的化合物所属物质类别一定不是________。
①氢化物 ②酸 ③碱 ④盐 ⑤氧化物
(2)A、B、C三种元素中有一种是金属,则这种元素是A、B、C中的________,理由是__________。
(3)如果E溶液是一种强酸,则E的化学式为_________;
①A能否是铁:________,理由是____________;
②A能否是铜:________,理由是____________;
③A可能是________(任写两种)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今有化合物: 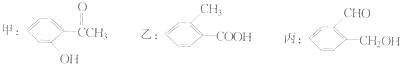
(1)请写出丙中含氧官能团的名称:;
(2)请判别上述哪些化合物互为同分异构体:;
(3)请分别写出鉴别甲、乙、丙化合物的方法.(指明所选试剂及主要现象即可) 鉴别甲的试剂:;现象:;
鉴别乙的试剂:;现象:;
鉴别丙的试剂:;现象: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,将10mL质量分数为50%(密度1.4g/mL)的硫酸稀释成100mL,下列说法正确的是( )
A.纯硫酸的摩尔质量为98
B.上述100mL稀硫酸中含溶质14g
C.上述稀释过程所需要的蒸馏水为90mL
D.质量分数为50%的硫酸物质的量浓度为7.14mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化过程中,属于氧化反应的是 ( )
A. CO32-→CO2 B. Zn→Zn2+ C. MnO2→Mn2+ D. FeCl3→FeCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组从海水晒盐后的苦卤(Br-, Mg2+含量较大)中提取溴,设计的实验方案如下:

(1)“氯气氧化”过程中发生反应的离子方程式________________________________;多余的Cl2用NaOH溶液吸收,写出反应的离子方程式_____________________________ 。
(2)萃取、分液操作的主要仪器是___________________;若用四氯化碳萃取溴水混合物中的溴,分液时有机层从仪器____________端放出。若从苦卤中提取金属镁,写出提取过程中发生氧化还原反应的化学方程式__________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com