
【题目】(氧氮杂 ![]() 是新药研制过程中发现的一类重要活性物质,具有抗惊厥、抗肿瘤、改善脑缺血等性质.下面是某研究小组提出的一种氧氮杂
是新药研制过程中发现的一类重要活性物质,具有抗惊厥、抗肿瘤、改善脑缺血等性质.下面是某研究小组提出的一种氧氮杂 ![]() 类化合物H的合成路线:
类化合物H的合成路线: 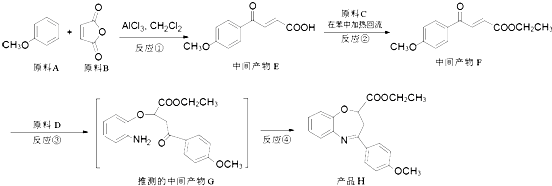
(1)原料A的同分异构体中,含有苯环、且核磁共振氢谱中有4个峰的是(写出其结构简式).
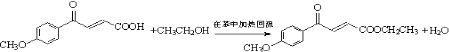
(2)反应②的化学方程式是 .
(3)③的反应类型是 . 原料D中含有的官能团名称是、 .
(4)原料B俗名“马莱酐”,它是马莱酸(顺丁烯二酸: ![]() )的酸酐,它可以经下列变化分别得到苹果酸(
)的酸酐,它可以经下列变化分别得到苹果酸( ![]() )和聚合物Q:
)和聚合物Q: 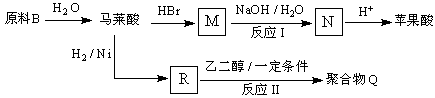
写出反应Ⅰ和反应Ⅱ的化学方程式:、 .
(5)符合下列条件的中间产物F的同分异构体数目是(不考虑手性异构),写出其中任意一种的结构简式 . (i)能发生银镜反应;
(ii)分子中含有三取代的苯环结构,其中两个取代基是:﹣COOCH3和 ![]() ,且二者处于对位.
,且二者处于对位.
【答案】
(1)![]()
(2)
(3)加成反应;氨基;酚羟基
(4)![]() ;
;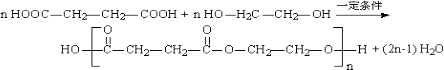
(5)4;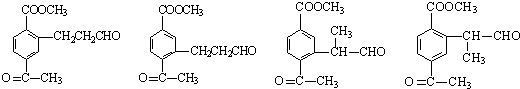 (任意写一种)
(任意写一种)
【解析】解:(1)原料A的同分异构体中,含有苯环,为甲基苯酚,核磁共振氢谱中有4个峰,应为对甲基苯酚,其结构简式为 ![]() , 所以答案是:
, 所以答案是: ![]() ;(2)由E、F的结构可知,反应②为E与乙醇发生酯化反应,该反应为
;(2)由E、F的结构可知,反应②为E与乙醇发生酯化反应,该反应为 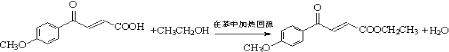 ,
,
所以答案是:  ;(3)由F、G的结构可知,为E中C=C键的加成反应,由G的结构可知,原料D中含氨基、酚﹣OH,所以答案是:加成反应;氨基、酚羟基;(4)由信息和流程可知,M为HOOCCH2CHBrCOOH,反应Ⅰ为﹣Br的水解反应,该反应为
;(3)由F、G的结构可知,为E中C=C键的加成反应,由G的结构可知,原料D中含氨基、酚﹣OH,所以答案是:加成反应;氨基、酚羟基;(4)由信息和流程可知,M为HOOCCH2CHBrCOOH,反应Ⅰ为﹣Br的水解反应,该反应为 ![]() ,
,
R为HOOCCH2CH2COOH,反应Ⅱ丁二酸与乙二醇的缩聚反应,该反应为  ,所以答案是:
,所以答案是: ![]() ;
;  ;(5)F的同分异构体符合:(i) 能发生银镜反应,含﹣CHO;(ii) 分子中含有三取代的苯环结构,其中两个取代基是:﹣COOCH3和
;(5)F的同分异构体符合:(i) 能发生银镜反应,含﹣CHO;(ii) 分子中含有三取代的苯环结构,其中两个取代基是:﹣COOCH3和 ![]() ,且二者处于对位,符合条件的同分异构体为
,且二者处于对位,符合条件的同分异构体为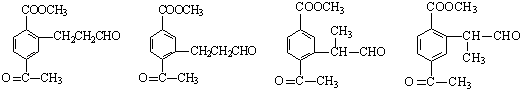 ,共4种,所以答案是:4;
,共4种,所以答案是:4; 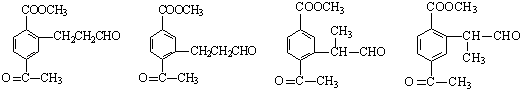 (任意写一种).
(任意写一种).


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列分离方法正确的是
A. 分离汽油和水可以用结晶的方法
B. 除去氯化钠溶液中的泥沙用分液的方法
C. 分离醋酸(沸点118℃)与乙酸乙酯(沸点77.1℃)用蒸馏的方法
D. 从含有少量氯化钠的硝酸钾溶液中提取硝酸钾用过滤的方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识回答下列问题:
(1)二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂,而且与Cl2相比不会产生对人体有潜在危害的有机氯代物。制备ClO2有下列两种方法:
方法一:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
方法二:2NaClO3+H2O2+H2SO4 =2ClO2↑+O2↑+2Na2SO4+2H2O
①方法一的离子方程式为____________________________________.
②方法二中被氧化的物质是___________,若反应中有0.1mol电子转移,则产生的ClO2气体在标准状况下的体积为___________L,在下面的化学方程式上用双线桥标出电子转移的方向和数目
2NaClO3+H2O2+H2SO4 =2ClO2↑+O2↑+2Na2SO4+2H2O___________
③某温度下,将Cl2通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合液,经测定ClO-与ClO3- 的浓度之比为1:1,则Cl2与NaOH溶液反应时被还原的氯元素与被氧化的氯元素的物质的量之比为____________;
(2)现用98%的浓H2SO4(密度为1.84g/cm3)来配制480mL 0.2mol/L的稀H2SO4。
有关操作为:①计算所需浓硫酸的体积 ②量取一定体积的浓硫酸 ③稀释、冷却 ④转移、洗涤 ⑤定容 ⑥摇匀。回答下列问题
①应量取的浓硫酸体积是__________,实验中所用的玻璃仪器除烧杯、玻璃棒、量筒、胶头滴管外还有_________________;
②将所配制的稀H2SO4进行测定,发现实际浓度大于0.2mol/L。请你分析下列哪些操作会引起所配浓度偏大(填写字母)_________________________。
A. 用量筒量取浓硫酸时,仰视量筒的刻度
B. 容量瓶未干燥即用来配制溶液
C. 浓硫酸在烧杯中稀释后,未冷却就立即转移到容量瓶中,并进行定容
D. 往容量瓶转移时,有少量液体溅出
E. 烧杯未进行洗涤
F. 在容量瓶中定容时俯视容量瓶刻度线
G. 定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关阿伏加德罗常数(NA)的说法错误的是( )
A. 32g O2所含的原子数目为NA
B. 0.5mol H2O含有的原子数目为1.5NA
C. 1mol H2O含有的H2O分子数目为NA
D. 0.5NA个氯气分子的物质的量是0.5mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用价层电子对互斥理论预测H2S和BF3的立体结构,两个结论都正确的是( )
A.直线形;三角锥形
B.V形;三角锥形
C.直线形;平面三角形
D.V形;平面三角形
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是某儿童微量元素体检报告单的部分数据:
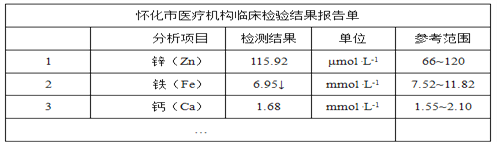
根据上表的数据,回答下列问题:
(1)该儿童__元素含量偏低。
(2)报告单中“μmol·L-1”是__(填“质量” “体积”或“浓度”)的单位。
(3)服用维生素C可使食物中的Fe3+转化为Fe2+。在这个过程中维生素C表现出__________(填“氧化性”或“还原性”)。
(4)硫酸亚铁晶体(FeSO47H2O)在医疗上可作补血剂。某课外小组测定该补血剂(每片b克)中铁元素的含量。实验步骤如图:
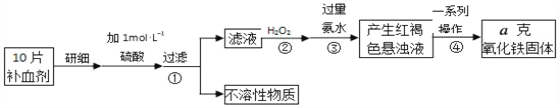
请回答下列问题:
a.②中H2O2的作用是__。
b.④中一系列处理的操作步骤为过滤、______、灼烧、冷却、称量。
c. 下列操作会导致所测定的铁元素含量偏高的是__。
A.步骤③所加氨水量不足 B.步骤④洗涤不充分 C.步骤④灼烧不充分
d. 写出步骤③中发生的离子方程式_____________________________________
e、简述滤液中存在Fe3+的检验方法是:_______________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,说明氨有还原性和碱性的是( )
A.2NH3+3CuO ![]() 3Cu+N2↑+3H2O
3Cu+N2↑+3H2O
B.8NH3+3Cl2═6NH4Cl+N2
C.4NH3+6NO ![]() 5N2+6H2O
5N2+6H2O
D.NH3+HCl═NH4Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、Q、E五种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,Q的核电荷数是X与Z的核电荷数之和,E在元素周期表的各元素中电负性最大.请回答下列问题:
(1)X的原子结构示意图为;Y的价电子轨道表示式为 .
(2)XZ2与YZ2分子的立体结构分别是和 , 相同条件下两者在水中的溶解度较大的是(写分子式),理由是 .
(3)Q的元素符号是 , 它属于第周期族,它的核外电子排布式为 , 在形成化合物时它的最高化合价为
(4)用氢键表示式写出E的氢化物水溶液中存在的所有氢键 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知4NH3+5O2═4NO+6H2O,同一反应速率若分别用v(NH3)、v(O2)、v(H2O)、v(NO)(molL﹣1min﹣1)来表示,则正确关系是( )
A.![]() v(NH3)=v(O2)
v(NH3)=v(O2)
B.![]() v(O2)=v(H2O)??
v(O2)=v(H2O)??
C.![]() v(NH3)=v(H2O)
v(NH3)=v(H2O)
D.![]() v(O2)=v(NO)
v(O2)=v(NO)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com