
设NA表示阿伏加德罗常数的值,下列叙述中正确的是
A.常温下,1 mol Cl2与足量NaOH溶液完全反应,转移的电子数2NA
B.常温常压下,11.2 L CO2中含有的分子数是0.5NA
C.标准状况下,22.4 L水所含原子数为3NA
D.常温常压下,48 g O3和O2的混合气体中氧原子数为3NA
 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源:2015届江西省赣州市六校高二上学期期末联考化学试卷(解析版) 题型:选择题
用惰性电极电解硫酸铜溶液,整个过程转移电子的物质的量与产生气体总体积的关系如图所示(气体体积均在相同状况下测定)。欲使溶液恢复到起始状态,可向溶液中加入( )
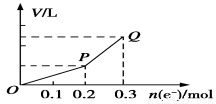
A.0.15 mol CuO B.0.1 mol CuCO3
C.0.075mol Cu(OH)2 D.0.05 mol Cu2(OH)2CO3
查看答案和解析>>
科目:高中化学 来源:2015届江苏省教学协作体高二上学期期末化学试卷(解析版) 题型:选择题
下物质间的转化通过一步化学反应不能实现的是
A.HCl → C12 B.Na → Na2O C.CuO → Cu(OH)2 D.Fe → Fe3O4
查看答案和解析>>
科目:高中化学 来源:2015届江苏省教学协作体高二上学期期末化学试卷(解析版) 题型:选择题
工业用洗净的废铜作原料来制备硝酸铜。为了节约原料和防止污染,宜采取的方法是
A.Cu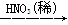 Cu(NO3)2
Cu(NO3)2
B.Cu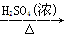 CuSO4
CuSO4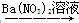 Cu(NO3)2
Cu(NO3)2
C.Cu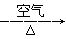 CuO
CuO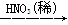 Cu(NO3)2
Cu(NO3)2
D.Cu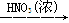 Cu(NO3)2
Cu(NO3)2
查看答案和解析>>
科目:高中化学 来源:2015届江苏省扬州市高二下学期学业水平模拟化学试卷(二)(解析版) 题型:填空题
双酚A (也称BPA)常用来生产防碎塑料聚碳酸酯。BPA的结构简式如图所示。
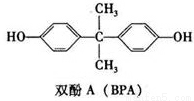
(1)双酚A中的含氧官能团为 (填名称)。
(2)下列关于双酚A的叙述中,不正确的是 (填标号)。
A.遇FeCl3溶液变色
B.可以发生还原反应
C.1 mol双酚A最多可与2 mol Br2反应
D.可与NaOH溶液反应
(3)双酚A的一种合成路线如下图所示:
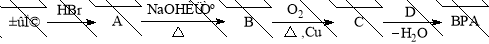
①丙烯→A的反应类型是 。
②B→C的化学方程式是 。
Ⅱ(7分)甲苯和溴乙烷混合物可通过如下流程进行分离。

请填写下列空白:
(1)X的结构简式为 ;
(2)操作①能否用分液 ,理由是 。
(3)写出甲苯与溴乙烷的混合物中加入试剂A时发生反应的化学方程式: 。
(4)如果Y为乙烯,则试剂B为 ,“一定条件”是指 。
查看答案和解析>>
科目:高中化学 来源:2015届江苏省扬州市高二下学期学业水平模拟化学试卷(二)(解析版) 题型:选择题
下列各组离子在溶液中能大量共存的是
A.Cu2+、Mg2+、SO42-、NO3- B.H+、Mg2+、SO42-、ClO-
C.Ag+、Na+、NO3-、Cl- D.NH4+、Ba2+、NO3-、OH-
查看答案和解析>>
科目:高中化学 来源:2015届江苏省扬州市高二下学期学业水平模拟化学试卷(二)(解析版) 题型:选择题
下列气体中,不能用排空气法收集的是
A.CO2 B.O2 C.NO D.NH3
查看答案和解析>>
科目:高中化学 来源:2015届江苏省扬州市高二上学期期末考试化学试卷(选修)(解析版) 题型:选择题
如图所示,a、b、c均为石墨电极,d为碳钢电极,通电电解一段时间。假设在电解过程中产生的气体全部逸出,下列说法正确的是
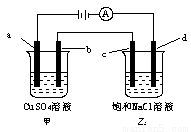
A.甲、乙两烧杯中溶液的pH均保持不变
B.甲烧杯中a电极反应式为:4OH――4e-= O2↑+2H2O
C.当电解一段时间后,将甲、乙两溶液混合,一定会产生蓝色沉淀
D.当b极增重3.2 g时,d极产生的气体为0.56 L(标准状况)
查看答案和解析>>
科目:高中化学 来源:2015届山西省大同市高二上学期期末考试化学试卷(解析版) 题型:填空题
(1)有甲、乙、丙、丁四种金属,把甲、丙浸入稀硫酸中,用导线连接时丙为负极;把乙、丁分别浸入稀硫酸中,丁产生气泡的速率更大;把甲、乙用导线连接浸入稀硫酸中,甲上有气泡冒出;把丙浸入丁的硝酸盐溶液中,丙的表面有丁析出。这四种金属的活动性由强到弱的顺序是 。
(2)向5mLNaCl溶液中滴入一滴AgNO3溶液,出现白色沉淀,继续滴加一滴KI溶液并振荡,沉淀变为黄色,再滴入一滴Na2S溶液并振荡,沉淀又变成黑色,根据上述变化过程,分析此三种沉淀物的溶解度大小关系为_______________。
(3) 现将足量的AgCl分别放入下列物质中,AgCl的溶解度由大到小的排列顺序是_______________
①20 mL 0.01 mol·L-1KCl溶液
②30 mL 0.02 mol·L-1CaCl2溶液
③40 mL 0.03 mol·L-1HCl溶液
④10 mL蒸馏水
⑤50 mL 0.05 mol·L-1 AgNO3溶液
(4)某种甲醇燃料电池是采用铂或碳化钨作为电极催化剂,在稀硫酸电解液中直接加入纯化后的甲醇,同时向一个电极通入空气。此电池的负极发生的电极反应式是_______________ ;
(5)某酸H2B在水溶液中有如下变化:H2B H++HB-;HB-
H++HB-;HB- H++B2-;现有溶液 0.10mol/L、100ml,试回答以下问题:
H++B2-;现有溶液 0.10mol/L、100ml,试回答以下问题:
①溶液中的H+物质的量取值范围是:
②已知0.1mol·L-1NaHB溶液的pH=2,则0.1mol·L-1 H2B溶液中氢离子的物质的量浓度可能是 0.11 mol·L-1(填“<”,“>”,或“=”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com