
����Ŀ����ҵ��NaCl��NH3��CO2��Ϊԭ�����Ƶ�NaHCO3����������������йط�Ӧ�Ļ�ѧ����ʽΪ��
NH3��CO2��H2O===NH4HCO3
NH4HCO3��NaCl===NaHCO3����NH4Cl
2NaHCO3![]() Na2CO3��CO2����H2O
Na2CO3��CO2����H2O
(1)̼������뱥��ʳ��ˮ��Ӧ��������̼�����ƾ����ԭ����__________(����ĸ���)��
a��̼������������ˮ
b��̼�����������ֽ�
c��̼�����Ƶ��ܽ����Խ�С����������Һ�����Ƚᾧ����
d��̼�����Ƶ��ȶ��Դ���̼����
(2)ij�С����������Ƽ�ԭ��������̼�����Ƶ��Ʊ�ʵ�顣
��һλͬѧ��������̼����ͨ�뺬���ı���ʳ��ˮ���Ʊ�̼�����ƣ�ʵ��װ������ͼ��ʾ(ͼ�мг֡��̶��õ�����δ����)��


�Իش������й����⣺
(��)��װ���е��Լ���____________����������____________________________��
(��)��װ����ϡ�����������_______________________��
(��)ʵ����������NaHCO3 ����IJ�����__________(��������������)���ò�������Ҫ�IJ���������__________________________��
����һλͬѧ��ͼ����װ��(����װ��δ����)����ʵ�顣
(��)ʵ��ʱ�����ȴ�a��ͨ��________���壬˵��ԭ��______________________��
(��)��ͬѧ��������װ�õ�b���¶����Ӽ�װ�ã�������____________________��
(3)̼�������������ù���12.28 g��������ʯ��ˮ��ַ�Ӧ�����ó�����ϴ�ӡ���������Ϊ12.00 g�������ù�����̼���Ƶ���������Ϊ__________________��
���𰸡�(1)c
(2)��(��)����̼��������Һ ��ȥCO2�е�HCl����
(��)����δ��Ӧ���NH3
(��)���� ��������©�����ձ�
��(��)NH3 ���������ܽ���ˮ�����γɽϴ�Ũ�ȵ���Һ�������ڶ�����̼���գ����ɸ����̼����� (��)������������Һ�Ӵ���������CO2��������
(3)86.3%(��0.863)
��������(1)̼������뱥��ʳ��ˮ��Ӧ��������̼�����ƾ����ԭ����̼�����Ƶ��ܽ����Խ�С����������Һ�����Ƚᾧ������ѡc��(2)��(��)��װ��������ȥ������̼�е��Ȼ������ʣ���ʢ�Լ��DZ���̼��������Һ��(��)ע�������Ƕ�װ����ϡ��������ã��������ʶ��е���ĩ�����ӵ���©�������ã����Դ�����δ��Ӧ���NH3��(��)ʵ�������NaHCO3 �������Һ�������������ù��˷����룻���˲����õ����ֲ�����������������©�����ձ�����(��)ʵ��ʱ�����ȴ�a��ͨ�백�������������ܽ���ˮ�����γɽϴ�Ũ�ȵ���Һ�������ڶ�����̼���գ����ɸ����̼����李�(��)����װ�õ�b���¶����Ӽ�װ�ã���������������Һ�Ӵ���������CO2�������ʡ�(3)��̼�������������ù�����̼���Ƶ����ʵ�����x mol��̼�����Ƶ����ʵ�����y mol����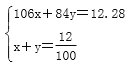 ��ã�x��0.1��y��0.02������̼���Ƶ���������Ϊ
��ã�x��0.1��y��0.02������̼���Ƶ���������Ϊ![]() ��100%��86.3%��
��100%��86.3%��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����֪���ظ����������Cr2O72����������������CrO42-������Һ���ܻ���ת�����ظ��������ˮ���������ӷ�Ӧ����ʽ��Cr2O72-����ɫ��+H2O2CrO42-����ɫ��+2H+ ��H��0����ҺΪ�Ȼ�ɫ������Һ�еμ�����6 mol/L�����ᣬ��Һ��________ɫ��ԭ���� _��
��2����NO2��N2O4����������ں����ܱ������У�������ϵ������100oC����ʱ��������________________��ԭ���� ��
��3�������������Һ��ϡ���ᷴӦ�ɳ��ֻ��ǣ��±���ijͬѧ�ø÷�Ӧ̽����ѧ��Ӧ���ʵ�ʵ���¼����ش��������⣺
ʵ����� | ��Ӧ�¶�/�� | Na2S2O3��Һ | ϡH2SO4 | H2O | ||
V/mL | c/��mol��L-1�� | V/mL | c/��mol��L-1�� | V/mL | ||
A | 25 | 5 | 0.1 | 5 | 0.1 | 10 |
B | 25 | 5 | 0.1 | 5 | 0.2 | 10 |
C | 35 | 5 | 0.1 | 10 | 0.1 | 5 |
D | 35 | 5 | 0.2 | 5 | 0.2 | V1 |
���÷�Ӧ�Ļ�ѧ����ʽ��
��V1=_________mL��
�����ֻ����ɿ쵽����˳��������ʵ�������__________________��
��4���������ʹ���Ը��������ɫ������д�˹��̵����ӷ�Ӧ����ʽ�� ����ͼΪ���������Ը�����ط�Ӧ��V-tͼ��������ͼ��AB���γɵĿ���ԭ��__________��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ס������ձ��и�ʢ��100 mL 3 mol��L��1�������NaOH��Һ�������ձ��зֱ��������������ۣ���Ӧ����������ɵ����������ΪV(��)��V(��)��1:2����������۵�����Ϊ( )
A. 1.8 g B. 2.7 g C. 3.6 g D. 5.4 g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л������У�����ͨ������֮��ķ�Ӧֱ����ȡ���ǣ� ��
A.Fe3O4
B.FeCl3
C.FeCl2
D.CuCl2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�ס��ҡ�����X��4����ѧ��ѧ�г��������ʣ���ת����ϵ������ͼ�����X(Ҫ���X�ܻ���)��������( )
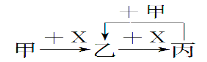
A��C��O2 B��CO2��NaOH��Һ
C��Cl2��Fe D��AlCl3��Һ��NaOH��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ס���������������ͬ�������壬�ڿ�����ȼ�յõ��������������������P4O6����������ʱ����P4O10��
��1����֪298 Kʱ���ס�������ȫȼ�յ��Ȼ�ѧ����ʽ�ֱ�Ϊ
P4��s����������5O2��g��=P4O10��s�� ��H1����2 983.2 kJ��mol��1
P��s����������![]() O2��g��=
O2��g��=![]() P4O10��s�� ��H2����738.5 kJ��mol��1
P4O10��s�� ��H2����738.5 kJ��mol��1
����¶��°���ת��Ϊ�����Ȼ�ѧ����ʽΪ ��
��2����֪298 Kʱ���ײ���ȫȼ�յ��Ȼ�ѧ����ʽΪP4��s����������3O2��g��===P4O6��s�� ��H����1638 kJ��mol��1����ij�ܱ������м���62 g����50.4 L��������״��������������ʹ֮ǡ����ȫ��Ӧ�������õ���P4O10��P4O6�����ʵ���֮��Ϊ ����Ӧ�����зų�������Ϊ ��
��3����֪����PCl3�ķ��ӽṹ��ͼ�����ṩ���»�ѧ���ļ�����kJ��mol��1����P��P 198��Cl��Cl 243��P��Cl 331��
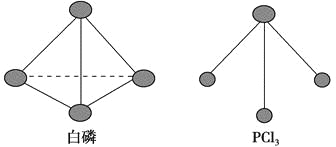
��ӦP4��s����������6Cl2��g��==4PCl3��s���ķ�Ӧ����H�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������Ԫ�أ�ȱ�ƻ���ɹ��������ݴ���������ʳ���в����Եõ���������ĸ�ʱ����Ҫ�ú��Ƶ�ҩƷ���������������������У�������Ϊ����ҩƷ����
A��CaCO3 B��CaO C��Ca(OH)2 D��Ca
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ԭ��һ����Ҫ�ķ�Ӧ��
��1����֪��ӦCu��2Fe3+=Cu2+��2Fe2+����Ӧ�л�ԭ���� ��������Fe3+ Cu2+(���� �� ������ �� ��) ��
��2����2Na2O2+2CO2��2Na2CO3+O2��Ӧ�У���ת��3mol���ӣ����������������ڱ�״���µ����Ϊ L��
��3����xR2++yH++O2�TmR3++nH2O�����ӷ���ʽ�У���ϵ��m��R2+��R3+�ж���ȷ���� ��
A��m=y��R3+�ǻ�ԭ�� B��m=2y��R2+������
C��m=2��R3+�������� D��m=4��R2+�ǻ�ԭ��
��4����˫���ű����Ӧ2KMnO4+16HCl��Ũ���T2KCl+2MnCl2+5Cl2��+8H2O�е���ת�Ƶķ������Ŀ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ۺ����ü������ڽ�Լ��Դ���������ڱ���������ʵ�������÷Ͼɻ�ͭ(Cu��Zn�Ͻ𣬺���������Fe)�Ʊ���������(CuSO4��5H2O)��������ZnO���Ʊ�����ͼ���£�
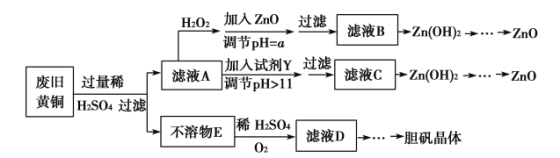
��֪��Zn���������������Al����������������ƣ�pH��11ʱZn(OH)2������NaOH��Һ����[Zn(OH)4]2�����±��г��˼������������������������pH(��ʼ������pH����������Ũ��Ϊ1.0 mol��L��1����)��
Fe3�� | Fe2�� | Zn2�� | |
��ʼ������pH | 1.1 | 5.8 | 5.9 |
������ȫ��pH | 3.0 | 8.8 | 8.9 |
��ش��������⣺
(1)����ZnO����pH��a��Ŀ����______________________��a�ķ�Χ________________________��
(2)�ɲ�����E������ҺD�Ļ�ѧ����ʽΪ____________________________��
(3)��ҺA�м���H2O2��Ӧ�����ӷ���ʽΪ________________________________________��
(4)����ҺD�Ƶ��������������Ҫ����������__________________________
(5)�����Լ�����ΪY�Լ�����____________��
A��ZnO B��NaOH C��Na2CO3 D��ZnSO4
������ҺC����μ�������ֱ���������������������______________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com