
【题目】某同学设计如图装置制取少量溴苯,请回答下列问题:

(1)写出实验室制取溴苯的化学方程式__________。
(2)上述反应发生后,在锥形瓶中加入硝酸银溶液观察到的现象是________,你认为这一现象能否说明溴和苯发生了取代反应(填“能”或“不能”)____________,理由是______________________。
(3)该装置中长直导管a的作用________,锥形瓶中的导管为什么不插入液面下?________。
(4)反应后得到的溴苯中溶有少量苯、溴、二溴苯、溴化铁和溴化氢等杂质,欲除去上述杂质得到比较纯净的溴苯,合理的操作步骤是___________。
【答案】![]() 浅黄色沉淀 不能 溴易挥发会进入锥形瓶,溴与硝酸银溶液也可发生反应,生成溴化银沉淀 冷凝回流并导气 防止水倒吸入烧瓶中 先用大量水洗后分液取下层液体,再加入稀的NaOH溶液充分反应后再分液取下层液体,再水洗分液取下层液体加入干燥剂并蒸馏可得到比较纯净的溴苯
浅黄色沉淀 不能 溴易挥发会进入锥形瓶,溴与硝酸银溶液也可发生反应,生成溴化银沉淀 冷凝回流并导气 防止水倒吸入烧瓶中 先用大量水洗后分液取下层液体,再加入稀的NaOH溶液充分反应后再分液取下层液体,再水洗分液取下层液体加入干燥剂并蒸馏可得到比较纯净的溴苯
【解析】
苯和液溴在溴化铁作催化剂的条件下,发生取代反应,生成溴苯和HBr,该反应为放热反应,苯和液溴均易挥发。
(1)苯和液溴在溴化铁作催化剂的条件下,发生取代反应,生成溴苯,化学方程式为![]() ;
;
(2)反应还生成了HBr,被锥形瓶中的水吸收,加入硝酸银溶液,生成溴化银淡黄色沉淀。由于反应放热,液溴易挥发,液溴也会挥发出被锥形瓶中的水吸收,加入溴化银也会生成淡化的溴化银,不一定是由于有HBr生成。答案为浅黄色沉淀 不能 溴易挥发会进入锥形瓶,溴与硝酸银溶液也可发生反应,生成溴化银沉淀;
(3)该反应为放热反应,苯和液溴均易挥发,长导管起到冷凝的作用,使挥发出去的苯等原料冷凝回流至圆底烧瓶,而长导管最基本的用途为导气。所以长导管的作用为冷凝回流并导气;HBr极易溶于水,若将导入插入液面以下,会引发倒吸,所以导管不能插入液体重是由于防止水倒吸入烧瓶中;
(4)溴苯中溶有少量苯、溴、二溴苯、溴化铁和溴化氢等杂质,首先无机物和有机物需要进行分离,溴单质不易溶于水,要转化为易溶于水的盐,,故先用大量的水洗,然后再NaOH溶液洗涤,将溴单质和HBr从有机相中分离,再用水洗,洗去NaOH溶液。分液得到含有少量水的有机相,经干燥后,有机相主要成分为溴苯,并含有苯和二溴苯等杂质,为液体混合物,利用各组分的沸点不同蒸馏得到较纯的溴苯。答案为:先用大量水洗后分液取下层液体,再加入稀的NaOH溶液充分反应后再分液取下层液体,再水洗分液取下层液体加入干燥剂并蒸馏可得到比较纯净的溴苯。


 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:
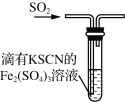
【题目】下列关于硫及其化合物的说法正确的是
A. 浓硫酸具有脱水性,可用于干燥氨气
B. 二氧化硫能使溴水、酸性高锰酸钾溶液褪色,因其有漂白性
C. 加氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42-
D. 如图装置中血红色褪去,可以验证SO2的还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列根据实验操作和实验现象所得出的结论不正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 将FeCl2样品溶于盐酸后,滴加KSCN溶液 | 溶液变成红色 | 原FeCl2样品已变质 |
B | 将Na2SO3样品溶于水,滴加入稀盐酸酸化的Ba(NO3)2溶液 | 产生白色沉淀 | 原Na2SO3样品已变质 |
C | 向淀粉KI溶液中滴入3滴稀硫酸,再加入10%的H2O2溶液 | 滴入稀硫酸未见溶液变蓝;加入H2O2溶液后,溶液立即变蓝 | 酸性条件下,H2O2氧化性强于I2 |
D | 向5mL0.5mol/LNaHCO3溶液中滴入2mL1mol/LBaCl2溶液 | 产生白色沉淀,且有无色气体生成 | 反应的化学方程式为NaHCO3 + BaCl2 BaCO3↓+ NaCl+ CO2↑+H2O |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应进行的方向和限度是化学反应原理所要研究的两个重要问题,下列有关化学反
应进行的方向和限度的说法中正确的是( )
A. mA(g)+nB(g)![]() pC(g),平衡时A的浓度等于0.5 mol/L,将容器体积扩大一倍,达到新的平衡后A的浓度变为0.3mol/L,则计量数m+n<p
pC(g),平衡时A的浓度等于0.5 mol/L,将容器体积扩大一倍,达到新的平衡后A的浓度变为0.3mol/L,则计量数m+n<p
B. 将一定量纯净的氨基甲酸铵置于密闭真空恒容容器中,在恒定温度下使其达到分解平衡:NH2COONH4(s)![]() 2NH3(g)+CO2(g),则CO2的体积分数不变能作为平衡判断的依据
2NH3(g)+CO2(g),则CO2的体积分数不变能作为平衡判断的依据
C. 对于反应A(g)+B(g)![]() 2C(g),起始充入等物质的量的A和B,达到平衡时A的体积分数为n%,此时若给体系加压则A的体积分数不变
2C(g),起始充入等物质的量的A和B,达到平衡时A的体积分数为n%,此时若给体系加压则A的体积分数不变
D. 2NO(g)+2CO(g)=N2(g)+2CO2(g)在常温下能自发进行,则该反应的ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各原子或离子的电子排布式错误的是( )
A.Al 1s22s22p63s23p1B.O2- 1s22s22p6
C.Na+ 1s22s22p6D.Si 1s22s22p2
查看答案和解析>>
科目:高中化学 来源: 题型:
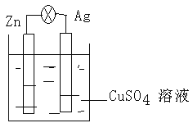
【题目】在银锌原电池中,以硫酸铜为电解质溶液,锌为____极,电极上发生的是____反应(“氧化”或“还原”)。电极反应式为________,银为______极,电极上发生的是_____反应(“氧化”或“还原”),电极反应式是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的数值,下列说法正确的是( )
A. 7.2 g CaO2晶体中阴离子和阳离子总数为0.3 NA
B. 0.1 mol/L NH4Cl溶液中Cl-离子数目为0.1 NA
C. 反应3H2(g)+N2(g)![]() 2NH3(g) ΔH=-92 kJ/mol,放出热量9.2 kJ时,转移电子0.6 NA
2NH3(g) ΔH=-92 kJ/mol,放出热量9.2 kJ时,转移电子0.6 NA
D. 0.1 mol H2O2分子中含极性共价键数目为0.3 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A.用植物油可萃取溴水中的溴
B.苯酚具有弱酸性,俗称石炭酸
C.淀粉和纤维素互为同分异构体
D.可以用银镜反应检验淀粉是否水解完全
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com