
����Ŀ�����������������ʣ�![]() ��
��![]() ��CaO��MgO��
��CaO��MgO��![]() ��
��![]() ��
��
��1�����ղ�ͬ�ķ��������������һ���������������������ԵIJ�ͬ�����ҳ��������ʣ���д����������ݣ��� ______��______��
��2���ӷ�Ӧ���������Ӳμӣ����Խ���ѧ��Ӧ��Ϊ���ӷ�Ӧ�ͷ����ӷ�Ӧ��![]() ��ˮ��Ӧ�����ӷ���ʽ��______��
��ˮ��Ӧ�����ӷ���ʽ��______��
��3���������������зֱ��ҳ����������Ӧ�����ʣ�д��һ����������ԭ��Ӧ�ķ���ʽ��һ��������ԭ��Ӧ�ķ���ʽ��______��
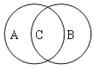
��4����Ȼ����ķ�����ͬ�������ӷ�Ӧ��������ԭ��Ӧ֮�������һ���Ĺ�ϵ�����ü�ͼʾ������ʾ����֮��Ĺ�ϵ��______��
���𰸡�![]() ���������ʵ������ǻ���������Ԫ�صĻ��ϼ�
���������ʵ������ǻ���������Ԫ�صĻ��ϼ� ![]() �����������ڳ����µ�״̬
�����������ڳ����µ�״̬ ![]()
![]() ��
��![]()
��������
(1)�ٸ�����Ԫ�ػ��ϼ۷��࣬�ڸ��ݳ����µ�״̬���ࣻ
(2) ![]() ��ˮ��Ӧ�����������ƺ�������
��ˮ��Ӧ�����������ƺ�������
(3) ��������������Ʒ�Ӧ���ɹ���ƣ����ϼ۱仯�����ڷ�������ԭ��Ӧ����������������Ʒ�Ӧ���������ƣ���Ԫ�ػ��ϼ۱仯������������ԭ��Ӧ��
(4)���ӷ�Ӧ��������ԭ��Ӧ֮���ǽ����ϵ��
(1)��![]() ����Ԫ�ػ��ϼ�Ϊ-1��
����Ԫ�ػ��ϼ�Ϊ-1��![]() ��
��![]() ��CaO��MgO��
��CaO��MgO��![]() ����Ԫ�ػ��ϼ۶�Ϊ-2��������Ԫ�ػ��ϼۣ���ͬ�����
����Ԫ�ػ��ϼ۶�Ϊ-2��������Ԫ�ػ��ϼۣ���ͬ�����![]() ����
����![]() �����³���̬��
�����³���̬��![]() ��CaO��MgO��
��CaO��MgO��![]() ��
��![]() �����³ʹ�̬�����ݳ����µ�״̬����ͬ�����
�����³ʹ�̬�����ݳ����µ�״̬����ͬ�����![]() ��
��
(2) ![]() ��ˮ��Ӧ�����������ƺ���������Ӧ�����ӷ���ʽ��
��ˮ��Ӧ�����������ƺ���������Ӧ�����ӷ���ʽ��![]() ��
��
(3)��������������Ʒ�Ӧ���ɹ���ƣ���Ԫ�ػ��ϼ۱仯�����ڷ�������ԭ��Ӧ����������������Ʒ�Ӧ���������ƣ���Ԫ�ػ��ϼ۱仯������������ԭ��Ӧ����Ӧ����ʽ�ֱ���![]() ��
��![]() ��
��
(4)���ӷ�Ӧ��������ԭ��Ӧ֮���ǽ����ϵ����A��ʾ���ӷ�Ӧ����B��ʾ������ԭ��Ӧ������֮��Ĺ�ϵΪ ��
��


 ��ǰ�κ�ͬ����ϰϵ�д�
��ǰ�κ�ͬ����ϰϵ�д� ����С��ҵϵ�д�
����С��ҵϵ�д� �Ƹ�С״Ԫ����������ϰ��ϵ�д�
�Ƹ�С״Ԫ����������ϰ��ϵ�д� �ɹ�ѵ���ƻ�ϵ�д�
�ɹ�ѵ���ƻ�ϵ�д� ����ѵ����ֱͨ�п�����ϵ�д�
����ѵ����ֱͨ�п�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˲ⶨʵ���ҳ��ڴ�ŵ�Na2SO3����Ĵ��ȣ�ȷ��ȡM g������Ʒ�����250 mL��Һ���������������ʵ�鷽����
����I��ȡ50.00 mL������Һ�����������������ữ��BaCl2��Һ������I��ϴ�ӡ���������������õ�����������Ϊm1 g
������ȡ50.00 mL������Һ����a mol/L ������KMnO4��Һ���еζ���
ʵ��������¼���������±���
�ζ����� ʵ������ | 1 | 2 | 3 | 4 |
������Һ���/mL | 50.00 | 50.00 | 50.00 | 50.00 |
�ζ��ܳ�����/mL | 0.00 | 0.20 | 0.10 | 0.15 |
�ζ���ĩ����/mL | 20.95 | 21.20 | 20.15 | 21.20 |
(1)����250 mL Na2SO3��Һʱ�������õ���ʵ�������У��ձ����������ιܡ�ҩ��_______��________��
(2)����IΪ______________��������Ϊ______________��
(3)�ڷ������еζ��յ���жϷ�����_______________________________��
(4)�ڷ������з��������ӷ�Ӧ����ʽΪ____________________________��
(5)���ݷ��������ṩ�����ݣ�����Na2SO3�Ĵ���Ϊ___________����д�ɷ�����ʽ��
(6)��������������ԭ�ζ������У����´���ҺNa2SO3Ũ�ȱ�С����_____������ţ���
a���ü�ʽ�ζ�����ȡ50mL����Һ����ʱ����ʼ���ӣ��ζ�����ʱ����
b���ü�ʽ�ζ�����ȡ50mL����Һ����ʱ��һ��ʼ�����ݣ��ζ�������û����
c����ʽ�ζ���������ˮ��ϴ��û��������KMnO4��Һ�����ϴ
d����ƿ������ˮ��ϴ��ֱ��װ50.00mL�Ĵ���Һ
e���ζ�����ʱ����ʼʱƽ�ӣ��ζ�����ʱ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й��������ʵ������������
A. ����������ͨ��CuSO4��Һ�пɵ�����ɫ��Һ
B. ����������ˮ���÷�ɢϵ�ɲ��������ЧӦ
C. ��������Һ��ϡ���ᷴӦ�����ɹ��ὺ��
D. ����������������ȼ�տ������Ȼ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������![]() ��
��![]() ��
��![]() ��
��![]() ��
��![]() ��
��![]() ��
��![]() ���һ����ѧ����ʽ����֪
���һ����ѧ����ʽ����֪![]() ����������Ϊ��Ӧ�
����������Ϊ��Ӧ�![]() ������ˮ�������ж���ȷ����
������ˮ�������ж���ȷ����![]()
A.![]() �Ƿ�Ӧ�
�Ƿ�Ӧ�![]() ��������
��������
B.![]() �Ƿ�Ӧ�
�Ƿ�Ӧ�![]() ��������
��������
C.![]() �Ƿ�Ӧ�
�Ƿ�Ӧ�![]() ��������
��������
D.![]() �Ƿ�Ӧ�
�Ƿ�Ӧ�![]() ��������
��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ָ����Ӧ�����ӷ���ʽ��ȷ����
A.MgͶ��ϡHNO3�У�Mg��2H+��Mg2+��H2��
B.MnO2��Ũ�����ϼ�����Cl2��MnO2��4H+��4Cl��![]() MnCl2��Cl2����2H2O
MnCl2��Cl2����2H2O
C.��ϡH2SO4��H2O2�Ļ��Һ�м���Cu�ۣ�2H+��H2O2��Cu��Cu2+��2H2O
D.��AlCl3��Һ�м��������ˮ��Al3+��4NH3��H2O��AlO![]() ��2H2O��4NH
��2H2O��4NH![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ�о�С��̽����������Ի�ѧ��ӦmA(g)+nB(g) pC(g)�����ʺ�ƽ���Ӱ��ͼ�����£������ж���ȷ����

A.��ͼ1��֪��![]() ���÷�Ӧ����ӦΪ���ȷ�Ӧ
���÷�Ӧ����ӦΪ���ȷ�Ӧ
B.��ͼ2��֪���÷�Ӧ![]()
C.ͼ3�У���3�ķ�Ӧ����:v��>v��
D.ͼ4�У���![]() ����a����һ��ʹ���˴���
����a����һ��ʹ���˴���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Y����һ�ֿ�����ʧ��ҩ�ĺϳɣ����ɻ�����X��һ���������Ƶá������йػ�����X��Y��˵����ȷ����

A.X����������ԭ�ӿ�����ͬһƽ����
B.1 mol Y�������4 mol H2�����ӳɷ�Ӧ
C.X��Y�ķ�Ӧ����Ϊ�ӳɷ�Ӧ
D.��FeCl3��Һ�ɼ���Y���Ƿ���X
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ϳɰ���ҵ�漰����ȼ�ϵ���������Ҫ�о�CO2��CO֮���ת����Ϊ��Ū������ɣ���һ������CO2������̼������ɱ���ܱ������з�Ӧ��C(s)��CO2(g) ![]() 2CO(g) H�����ѹǿ���¶ȶ�CO��CO2��ƽ����ɵ�Ӱ����ͼ��ʾ���ش��������⣺
2CO(g) H�����ѹǿ���¶ȶ�CO��CO2��ƽ����ɵ�Ӱ����ͼ��ʾ���ش��������⣺

��1��p1��p2��p3�Ĵ�С��ϵ��________��ͼ��a��b��c�����Ӧ��ƽ�ⳣ����С��ϵ��______________________��
��2��һ�������£���CO2������̼��Ӧ����ƽ����ϵ�м���H2���ʵ������������з�Ӧ��������Ӧ1��CO(g)��3H2(g) ![]() CH4(g)��H2O(g) H1= a kJ/mol
CH4(g)��H2O(g) H1= a kJ/mol
��Ӧ2��CO(g)��H2O(g) ![]() CO2(g)��H2(g) H2= b kJ/mol
CO2(g)��H2(g) H2= b kJ/mol
�� �������̼��������Ӧת��Ϊ�����ˮ�������Ȼ�ѧ����ʽ��____________��
�� ��֪298 Kʱ��ػ�ѧ����������Ϊ��
��ѧ�� | H��H | O��H | C��H |
|
E/��kJ��mol-1�� | 436 | 465 | 413 | 1076 |
����ݼ��ܼ��㣬H1=________________����Ӧ1�Է����е�������___________���������ϸ��¶��������ϵ��¶������������¶�����
��3��һ�������£�CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ��H3����̶��ݻ�Ϊ1 L���ܱ������г���2 mol CO2��6 mol H2��һ��ʱ���ﵽƽ��״̬�����CH3OH(g)�����ʵ���Ϊ1mol����������¸÷�Ӧ�Ļ�ѧƽ�ⳣ��K =_________���÷�����ʾ��������ʼʱ����2 mol CH3OH(g) ��2 mol H2O(g)�ﵽ��ͬƽ��״̬ʱ��CH3OH��ת����Ϊ_______����ƽ����ٳ���4 mol��N2����c(CO2)��ԭƽ��Ƚ���_________��������������������С��������������
CH3OH(g)+H2O(g) ��H3����̶��ݻ�Ϊ1 L���ܱ������г���2 mol CO2��6 mol H2��һ��ʱ���ﵽƽ��״̬�����CH3OH(g)�����ʵ���Ϊ1mol����������¸÷�Ӧ�Ļ�ѧƽ�ⳣ��K =_________���÷�����ʾ��������ʼʱ����2 mol CH3OH(g) ��2 mol H2O(g)�ﵽ��ͬƽ��״̬ʱ��CH3OH��ת����Ϊ_______����ƽ����ٳ���4 mol��N2����c(CO2)��ԭƽ��Ƚ���_________��������������������С��������������
��4����ͼ�Ǽ״�ȼ�ϵ�ع�����ʾ��ͼ������A��B��D��Ϊʯī�缫��CΪͭ�缫������һ��ʱ��Ͽ�K����ʱA��B�����ϲ��������������ͬ��

�����и����ĵ缫��ʽΪ_______________������C���ĵ缫��ӦʽΪ___________��
�� ����A�������������ڱ�״���µ����Ϊ__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���ѧϰС������H2C2O4��Һ������KMnO4��Һ֮��ķ�Ӧ��̽������������ı�Ի�ѧ��Ӧ���ʵ�Ӱ������ʵ�����£�����˵��������ǣ� ��
ʵ�� ��� | ʵ���¶�T/K | �μӷ�Ӧ������ | ��Һ��ɫ������ɫʱ����ʱ��t/s | ||||
KMnO4��Һ�������ᣩ | H2C2O4��Һ | H2O | |||||
V/mL | c/mol��L-1 | V/mL | c/mol��L-1 | V/mL | |||
A | 293 | 4 | 0.02 | 6 | 0.1 | 0 | 6 |
B | 293 | 4 | 0.02 | 4 | 0.1 | V1 | 8 |
C | T1 | 4 | 0.02 | 6 | 0.1 | 0 | 5 |
A.ʱ��t�������ǣ�����Һ��ϵ� B.ʵ��C�� C.ʵ��A��B��̽�� D.ʵ��A��C��̽���¶ȶԷ�Ӧ���ʵ�Ӱ�죬��![]() ��ɫ��ȥ��ʱ��
��ɫ��ȥ��ʱ��![]()
![]() Ũ�ȶԷ�Ӧ���ʵ�Ӱ�죬��
Ũ�ȶԷ�Ӧ���ʵ�Ӱ�죬��![]()
![]()
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com