
【题目】碳酸亚乙烯酯是锂离子电池低温电解液的重要添加剂,其结构如图.下列有关该物质的说法正确的是( ) ![]()
A.1mol该物质最多可与2molH2加成
B.分子式为C3H2O3
C.分子中只有极性键
D.8.6g该物质完全燃烧得到6.72LCO2
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】关于下列各装置图的叙述中,正确的是

A. 若采用装置①铝件镀银,则c极为铝件,d极为纯银,电解质溶液为AgNO3溶液
B. 装置②是原电池,能将化学能转化为电能,SO42-移向锌电极
C. 装置③中X若为四氯化碳,用于吸收氨气或氯化氢,会引起倒吸
D. 装置④可用于收集氨气,并吸收多余的氨气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列判断正确的是
A. 0.1 mol Na2O2含有的离子总数为0.4NA
B. 常温常压下,18g H2O 所含的中子数为8NA
C. 5.6 g铁与足量盐酸反应转移的电子数为0.3NA
D. 将含0.l mol FeCl3的饱和溶液制成胶体后,生成的Fe(OH)3胶粒数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NOx、SO2是主要的大气污染物,能引发雾霾、光化学烟雾及酸雨。
(1)NO2会产生硝酸型酸雨,硝酸型酸雨中主要溶质的化学式为_______________。
(2)目前新出厂的汽车均加装尿素[CO(NH2)2]箱,尾气中NO、NO2及尿素以物质的量之比1:1:1加热催化生成无害气体的化学方程式为_____________________________。
(3)氨化法同时脱硫脱硝的原理如下(已知NH4NO2在浓度较大时会分解)

①“催化氧化”的目的是________________。
②最终得到副产品的主要成分为____________(填化学式)。
③相同条件下用氨水作吸收剂,NOx的脱除率与pH及![]() 的关系如图所示。
的关系如图所示。

pH及其他条件相同时, ![]() 的比值越大,NOx的拖出率也越大,其主要原因是_________________。
的比值越大,NOx的拖出率也越大,其主要原因是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作错误的是( )
A.蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口
B.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
C.萃取,分液前需对分液漏斗检漏
D.用酒精萃取碘水中的碘
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中要配制2mol/L的NaCl溶液980 ml,配制时应选用的容量瓶的规格和称取的NaCl的质量分别是( )
A. 980 mL,114.7g B. 500mL, 58.5g
C. 1000 mL, 117 g D. 1000mL,117.0g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的量的说法中正确的是( )
A.物质的量就是物质的质量B.摩尔是国际单位制中的基本单位
C.某容器中含有1mol氯D.阿伏加德罗常数是6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】全钒氧化还原电池是一种新型可充电池,不同价态的含钒离子作为正极和负极的活性物质,分别储存在各自的酸性电解液储罐中。其结构原理如图所示,该电池放电时,右槽中的电极反应为:V2+-e-=V3+,下列说法正确的是
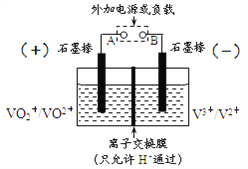
A. 放电时,右槽发生还原反应
B. 放电时,左槽的电极反应式:VO2++2H++e-=VO2++H2O
C. 充电时,每转移1mol电子,n(H+)的变化量为1mol
D. 充电时,阴极电解液pH升高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com