


 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:高中化学 来源: 题型:
| A、烧瓶内气体的颜色不再加深 |
| B、HI的消耗速率与H2的消耗速率之比为2:1 |
| C、I2的生成速率与I2的消耗速率相等 |
| D、烧瓶内气体的质量不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定存在的离子有CO32-、AlO2-、Na+ |
| B、一定不存在的离子有Ag+、Ba2+、Al3+ |
| C、可能存在的离子是SO42- |
| D、白色沉淀乙只能是BaCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C2H4>CO>N2 |
| B、C2H4=CO=N2 |
| C、CO>C2H4>N2 |
| D、N2>C2H4>CO |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、步骤①中的白色沉淀为2种钡盐 |
| B、溶液中难以确定Cl-的存在与否 |
| C、原溶液中所含的离子有5种 |
| D、步骤③中可以确定Fe2+、NO3-的存在,不能确定其它离子是否存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、石油主要是由各种烷烃、环烷烃、芳香烃组成的混合物,没有固定的熔点 |
B、聚乙烯是由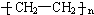 分子组成的化合物,加热至某一温度,则可全部熔化 分子组成的化合物,加热至某一温度,则可全部熔化 |
| C、同质量的乙烯和聚乙烯燃烧后生成的CO2质量相等 |
| D、油脂不是天然高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、苯、油脂均不能使酸性KMnO4溶液褪色 |
| B、向皂化反应后的混合溶液中加入食盐,静置,分层,下层为高级脂肪酸钠 |
| C、淀粉和纤维素的分子式均为(C6H10O5)n,二者互为同分异构体 |
| D、向鸡蛋清溶液中加硫酸铵饱和溶液,有沉淀析出,再加水沉淀溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
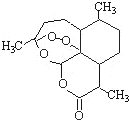 被誉为中国“新四大发明”的复方蒿甲醚是第一个由中国发现的全新化学结构的药品,也是目前在国际上获得广泛认可的中国原创药品.至今已被多个亚非国家指定为疟疾治疗一线用药,它在疟疾这一高传染性疾病治疗史上具有里程碑意义.其主要成分是青蒿素(是一种由青蒿中分离得到的具有新型化学结构的抗疟药),结构如图所示.有关该化合物的叙述正确的是( )
被誉为中国“新四大发明”的复方蒿甲醚是第一个由中国发现的全新化学结构的药品,也是目前在国际上获得广泛认可的中国原创药品.至今已被多个亚非国家指定为疟疾治疗一线用药,它在疟疾这一高传染性疾病治疗史上具有里程碑意义.其主要成分是青蒿素(是一种由青蒿中分离得到的具有新型化学结构的抗疟药),结构如图所示.有关该化合物的叙述正确的是( )| A、分子式为:C15H24O5 |
| B、该化合物在一定条件下不能与NaOH溶液反应 |
| C、该化合物中含有过氧键,一定条件下有氧化性 |
| D、青蒿素与维生素一样是水溶性的 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com