
����Ŀ��̽����Ƭ��Na2CO3��Һ�ķ�Ӧ��
|
| |
���������� | ��Ƭ�������ϸС���� | ���ְ�ɫ���ǣ������������ݣ�������ΪH2��CO2�� |
����˵������ȷ����
A.�ԱȢ�˵��Na2CO3��Һ���ƻ�������ı���Ĥ
B.�Ʋ���ְ�ɫ���ǵ�ԭ��AlO2- + HCO3- + H2O = Al��OH��3��+ CO32-
C.���Ⱥ�H2�ݳ���CO32- ˮ��ƽ���ƶ������Ӱ�����෴��
D.Na2CO3��Һ�д���ˮ��ƽ�⣺CO32- + H2O HCO3- + OH-
���𰸡�C
��������
Aѡ�I��Al����û�����ݣ�˵������������Ĥ��III��Al�����ݣ�˵����������Ĥ���ƻ�����A��ȷ��
Bѡ�̼������Һ�Լ��ԣ������������Ĥ�ͼӦ����ƫ�������ȥ������Ĥ�����ͼӦ����ƫ�������̼���ˮ������̼�������̼��������Ӻ�ƫ��������ӷ�Ӧ�� AlO2�� + HCO3�� + H2O = Al(OH)3��+ CO32������B��ȷ��
Cѡ�����ˮ�������ȷ�Ӧ�����ȴٽ�����ˮ�⣬�����ݳ��������������������ӵķ�Ӧ��̼���ˮ������̼����������������ӣ����������������ӣ��ٽ�̼�������ˮ�⣬���Լ��Ⱥ�H2�ݳ���CO32- ˮ��ƽ���ƶ������ٽ����ã���C����
Dѡ�Na2CO3��Һ�д���ˮ��ƽ�⣺CO32�� + H2O ![]() HCO3�� + OH������D��ȷ��
HCO3�� + OH������D��ȷ��
������������ΪC��


 ���Ͱ�ͨ�������Сѧ��ʱͬ�����ϵ�д�
���Ͱ�ͨ�������Сѧ��ʱͬ�����ϵ�д� ���Ͱ�ͨ������ϵ�д�
���Ͱ�ͨ������ϵ�д� �ٷ�ѧ����ҵ��������ϵ�д�
�ٷ�ѧ����ҵ��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ԫ������Ȼ������Ҫ��������������Ҫ�ɷ�ΪAl2O3��������Fe2O3��FeO��SiO2���С���ҵ�����������Ʊ�����ij�ֻ�����Ĺ����������¡�

��1������ҺA�м���Ư��Һ��Ŀ��������������������ҺB�����ԡ�
�ٸù������漰ij������ԭ��Ӧ���£�����ɣ�__Fe2+___ClO��+�� ��___=____Fe��OH��3��+__C1��+�� ����
�ڼ�����ҺB���Ƿ�����Ԫ�صķ���Ϊ��________��ע���Լ�������
�۽���ҺB�е���Ԫ���Գ�����ʽ��������ѡ�õ�����Լ�Ϊ___������ţ���
a������������Һ b��������Һ c����ˮ d��������̼
������ҺB�Ʊ��Ȼ��������漰�IJ���Ϊ���ߵμ�Ũ���������Ũ������ȴ�ᾧ��____����������ƣ���ϴ�ӡ�
��2��SiO2��NaOH�����Ʊ������ƣ��ɲ��õ�װ��Ϊ___������ţ���

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
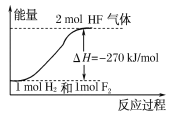
����Ŀ����֪��H2(g)��F2(g)===2HF(g) ��H����270 kJ/mol������˵����ȷ����( )
A������������ֽ����������ͷ����ķ�Ӧ�Ƿ��ȷ�Ӧ
B��1 mol H2��1 mol F2��Ӧ����2 molҺ̬HF�ų�������С��270 kJ
C������ͬ�����£�1 mol H2��1 mol F2�������ܺʹ���2 mol HF���������
D���÷�Ӧ�е������仯������ͼ����ʾ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ܱ������зֱ����N2��H2��O2�������壬���¸��������������ȷ���ǣ� ��
A. �����ǵ��¶Ⱥ�ѹǿ����ͬʱ������������ܶȣ�����H2��������N2��������O2��
B. �����ǵ��¶Ⱥ��ܶȶ���ͬʱ�����������ѹǿ��p��H2����p��N2����p��O2��
C. �����ǵ��������¶ȡ�ѹǿ����ͬʱ����������������V��O2����V��N2����V��H2��
D. �����ǵ�ѹǿ��������¶Ⱦ���ͬʱ�����������������m��H2����m��N2����m��O2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������нϹ㷺�Ŀ������ã���ṹ��ʽ����ͼ��ʾ��

���ڿ������������������ȷ����(����)
A������ʽΪC16H13O9
B��1 mol����������뺬8 mol NaOH����Һ��Ӧ
C����ʹ����KMnO4��Һ��ɫ��˵�����ӽṹ�к���̼̼˫��
D����Ũ��ˮ�ܷ����������͵ķ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������25 mL 2 mol��L��1Na2CO3��75 mL 1 mol��L��1��ϡ�������Na2CO3��Һ�����ε�ϡ������ ����ϡ���Ỻ���ε�Na2CO3��Һ�У��ڱ�״���²��������������( )
A.��Ϊ0.84 L
B.��Ϊ0.56 L
C.������
D.������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NaCl�����������бز����ٵ����ʡ���NaCl����ˮ���1 mol��L-1����Һ���ܽ������ͼ��ʾ������˵����ȷ����
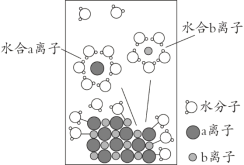
A. a����ΪNa+
B. ��Һ�к���NA��Na+
C. ˮ��b���ӵ�ͼʾ����ѧ
D. �����²ⶨ��NaCl��Һ��pHС��7��������Cl-ˮ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����300 Kʱ��A(g)��B(g) ![]() 2C(g)��D(s)�Ļ�ѧƽ�ⳣ��K��4���ڸ��¶��£���1 L�����м���1 mol A��1 mol B������Ӧ����������������Ϊ�÷�Ӧ�ﵽƽ��״̬�ı�־����
2C(g)��D(s)�Ļ�ѧƽ�ⳣ��K��4���ڸ��¶��£���1 L�����м���1 mol A��1 mol B������Ӧ����������������Ϊ�÷�Ӧ�ﵽƽ��״̬�ı�־����
��C������������C������������� �ڵ�λʱ��������a mol A��ͬʱ����2a mol C ��A��B��C��Ũ�Ȳ��ٱ仯 ����C�����ʵ������ٱ仯 �ݻ���������ѹǿ���ٱ仯 ���������ܶȲ��ٱ仯 ��A��B��C�ķ�����֮��Ϊ1��1��2
A. �ڢ� B. �ܢ� C. �ڢ� D. �ܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Fe(NO3)3��Cu(NO3)2��HNO3��ij��ϡ��Һ���������ۣ�c(Fe2+)�ı仯��ͼ��ʾ������˵���������(����)
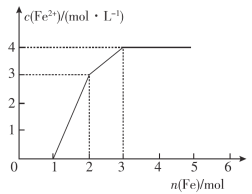
A.����0��1��Fe+NO![]() +4H+==Fe3++NO��+2H2O
+4H+==Fe3++NO��+2H2O
B.����1��2��Fe+2Fe3+=3Fe2+
C.����2��3��Fe+Cu2+=Fe2++Cu
D.ԭ��Һ����������Ũ�����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com