
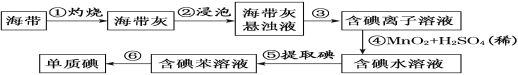
【题目】海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验(苯,一种不溶于水,密度比水小的液体):
请回答下列问题:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是________(填标号)。
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器
(2)步骤③的实验操作名称是________;步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是________。
(3)步骤⑤是萃取、分液,某学生选择用苯来提取碘的理由是___________________。
在分液操作中,应充分振荡,然后静置,待分层后________(填标号)。
A.直接将含碘苯溶液从分液漏斗上口倒出
B.直接将含碘苯溶液从分液漏斗下口放出
C.先将水层从分液漏斗的下口放出,再将含碘苯溶液从下口放出
D.先将水层从分液漏斗的下口放出,再将含碘苯溶液从上口倒出
(4)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法:________
【答案】BDE 过滤 蒸馏 苯与水互不相容,与碘水互不反应,碘在苯中的溶解度比水大 D 取少量液体与试管中,向其滴加淀粉溶液,若溶液变蓝,则含有单质碘
【解析】
(1)根据实验操作步骤①灼烧来分析用到的实验仪器;
(2)分离固体和液体用过滤;将苯和碘分离,应用的是两者的沸点不同;
(3)根据萃取剂的选择原理来回答;根据分液的操作来分析;
(4)根据碘单质遇到淀粉会变蓝色来检验是否还有碘单质。
(1)灼烧固体物质一般使用(瓷)坩埚,而坩埚加热需要用泥三脚支撑然后放在三脚架上,三脚架下面的空间放酒精灯,故答案为BDE;
(2)将悬浊液分离为残渣和含碘离子溶液应选择过滤的方法;将苯和碘分离,应用的是两者的沸点不同,即用蒸馏的方法;
(3)萃取剂的选择原理:和水互不相溶,苯与碘不反应,要萃取的物质在其中的溶解度大于在水中的溶解度,故可以选择苯;分液时,下层液体从下口流出,上层液体从上口倒出,由于苯的密度比水小,故碘的苯溶液在上层,水在下层,故先将水层从分液漏斗的下口放出,再将含碘苯溶液从上口倒出,故答案为D;
(4)提取碘后的水溶液中若是含有单质碘,则遇到淀粉会变蓝色,可以取少量提取碘后的水溶液于试管中,加入几滴淀粉试液,观察是否出现蓝色(如果变蓝,说明还有单质碘)。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】将20g两种金属的混合物投入足量的稀硫酸中,反应完全后得到标准状况下H2 11.2L,则该混合物的组成可能是( )
A. Na和Fe B. Mg和Cu C. Al和Mg D. Zn和Fe
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一种叶绿素分子(左)和血红蛋白分子(右)的局部结构简图,下列说法不正确的是( )

A.合成叶绿素和血红蛋白分别需要镁和铁
B.植物体缺氮会影响光合作用
C.人体缺铁会影响血红蛋白对氧的运输
D.Mg和Fe分别存在于植物和动物细胞中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知存在离子反应3S+6OH-=2S2-+SO32-+3H2O,关于该反应的说法正确的是
A. 该反应属于复分解反应
B. 该反应氢氧根离子作氧化剂
C. 该反应中氧化剂与还原剂的质量为2∶1
D. 每生成2个S2-反应转移的电子数为6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】见下图(A)处通入Cl2,当关闭(B)阀时,(C)处的湿润的红布条没有明显变化,当打开(B)阀时,(C)处的湿润红布条逐渐褪色,则(D)瓶中装的溶液是

A. 浓硫酸B. NaOH溶液C. 水D. NaCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是由短周期元素组成的一些单质及其化合物之间的转化关系图。各方框表示有关的一种反应物或生成物(某些物质已经略去),其中A、B、D在常温下均为无色无刺激性气味的气体,C是使湿润的红色石蕊试纸变蓝的气体,M是最常见的无色液体。

(1)物质G的化学式:______。
(2)物质B的电子式:______。
(3)写出A→D的化学方程式:______;G→E的离子方程式:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国新型火箭长征5号采用液氢和液氧作为推进剂。有关说法不正确的是( )
A.将氢、氧液化可增加火箭携带燃料总量
B.火箭依靠氢气和氧气燃烧放出的热推进
C.拆开氢、氧分子中的化学键需要吸收能量
D.燃料的总能量小于燃烧产物水的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知①CH3COOH(l)+2O2(g)===2CO2(g)+2H2O(l) ΔH1=-870.3 kJ/mol
②C(s)+O2(g)===CO2(g) ΔH2=-393.5 kJ/mol
③H2(g)+![]() O2(g)===H2O(l) ΔH3=-285.8 kJ/mol
O2(g)===H2O(l) ΔH3=-285.8 kJ/mol
则2C(s)+2H2(g)+O2(g)===CH3COOH(l)的反应热为
A. -870.3 kJ/mol B. -571.6 kJ/mol
C. +787.0 kJ/mol D. -488.3 kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com