
【题目】见下图(A)处通入Cl2,当关闭(B)阀时,(C)处的湿润的红布条没有明显变化,当打开(B)阀时,(C)处的湿润红布条逐渐褪色,则(D)瓶中装的溶液是

A. 浓硫酸B. NaOH溶液C. 水D. NaCl溶液
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】酒精是常用的医疗物资。下列有关酒精的说法不正确的是( )
A.乙醇的结构简式为C2H6O
B.酒精可以溶解碘制备碘酒
C.75%的酒精用于医疗消毒
D.工业酒精可由乙烯为原料制备
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)基态Cl原子中,电子占据的最高能层具有的原子轨道数为____。
(2)NH4CuSO3中金属阳离子的价电子排布式为________。N、O、S三种元素的第一电离能由大到小的顺序为________ (填元素符号)。
(3)氨基乙酸钠(H2NCH2COONa)中中心原子N原子的价层电子对数为________,C原子的杂化方式为________,1 mol氨基乙酸钠中含有σ键的数目为________。
(4)向CuSO4溶液中加入过量氨水,可生成[Cu(NH3)4]SO4溶液,在[Cu(NH3)4]2+中配原子为________。
(5)MgO和CaO均为离子晶体,两者的熔融混合物冷却时,先析出的晶体是____,原因是________
(6)BN的熔点是3000℃,密度为d g·cm-3,其晶胞结构如图所示,晶体中一个B原子周围距离最近的N原子有________个;若原子半径分别为rN pm和rB pm,阿伏加德罗常数值为NA,则BN晶胞中原子的体积占晶胞体积的百分率为__________(用含d、rN 、rB、NA的式子表示)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某无色透明溶液中仅含有包括Na+和CH3COO-在内的四种离子。
请回答下列问题。
(1)该溶液中的溶质可能有三种情况,请分别写出各种情况的化学式:
①_____________________;②________________________;③____________________ 。
(2)25℃,若由0.1 mol/L的CH3COOH溶液与0.1 mol/L的NaOH溶液等体积混合,测得混合溶液的pH=8,则c(CH3COOH)+c(H+)的精确值为___________________mol/L。
(3)若该溶液的pH=8,则c(Na+)-c(CH3COO-)的精确值为___________________mol/L。
(4)当溶液中各离子浓度大小的顺序为c(CH3COO-)>c(Na+)>c(H+)>c(OH-)时,则该溶液可能是____(填序号);
A.由0.1 mol/L的CH3COONa溶液与0.1 mol/L的CH3COOH溶液等体积混合而成
B.由0.1 mol/L的CH3COOH溶液与0.1 mol/L的NaOH溶液等体积混合而成
C.由0.2 mol/L的CH3COONa溶液与0.1 mol/L的HCl溶液等体积混合而成
D.由0.2 mol/L的CH3COOH溶液与0.1 mol/L的NaOH溶液等体积混合而成
(5)常温下,将a mol/L的CH3COOH溶液与0.01 mol/L的NaOH溶液等体积混合,反应平衡后溶液中c(Na+)=c(CH3COO-),用含a的代数式表示CH3COOH的电离平衡常数Ka=_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁和水反应放出大量热,该反应可用于野外供热。下列镁和水反应放热最快的是( )
A.100g镁条和100mL冰水反应
B.100g镁粉和100mL30℃水反应
C.100g镁条和100mlL30℃水反应
D.100g镁粉和100mL冰水反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验(苯,一种不溶于水,密度比水小的液体):
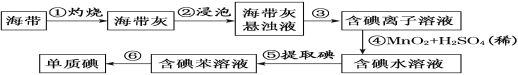
请回答下列问题:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是________(填标号)。
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器
(2)步骤③的实验操作名称是________;步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是________。
(3)步骤⑤是萃取、分液,某学生选择用苯来提取碘的理由是___________________。
在分液操作中,应充分振荡,然后静置,待分层后________(填标号)。
A.直接将含碘苯溶液从分液漏斗上口倒出
B.直接将含碘苯溶液从分液漏斗下口放出
C.先将水层从分液漏斗的下口放出,再将含碘苯溶液从下口放出
D.先将水层从分液漏斗的下口放出,再将含碘苯溶液从上口倒出
(4)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法:________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在标准状况下,5.6L A气体的质量是15g,则A的摩尔质量为___。
(2)一定量的液态化合物XY2,在一定量的O2中恰好完全燃烧,反应方程式为:XY2(液)+ 3O2(气)= XO2(气)+2YO2(气),冷却后,在标准状况下测得生成物的体积是672mL,密度是2.56g/L,则:
①反应前O2的体积是______。
②化合物XY2的摩尔质量是____。
③若XY2分子中X、Y两元素的质量之比为3:16,则X、Y两元素分别是_____和_____。(写元素符号)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一无色混合物的水溶液,可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Fe3+、CO32-、SO42-、H+,现取三份100mL溶液进行如下实验:(已知NH4++OH-![]() NH3+H2O;MgCO3是微溶物)(1)第一份加入足量AgNO3溶液有沉淀产生(2)第二份加足量NaOH溶液加热后,收集到气体0.04mol(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。根据上述实验,以下推测正确的是( )
NH3+H2O;MgCO3是微溶物)(1)第一份加入足量AgNO3溶液有沉淀产生(2)第二份加足量NaOH溶液加热后,收集到气体0.04mol(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。根据上述实验,以下推测正确的是( )
A. K+一定存在B. 100mL溶液中含0.01mol CO32-
C. Cl-一定存在D. Fe3+一定不存在,Mg2+可能存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 煤是复杂的混合物,含有苯、甲苯、二甲苯等一系列重要的化工原料
B. 石油分馏得到的汽油、煤油、柴油等都有固定的熔沸点
C. 石油炼制的目的是为了获得轻质油和重要化工原料(乙烯、丙烯等)
D. 天然气和沼气的主要成分是乙烯,它们都属于不可再生能源
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com