
| A. | 2SO2+O2═2SO3△H=-196.6 kJ/mol | B. | 2H2O (g)═2H2(g)+O2(g)△H=-483.6kJ/mol | ||
| C. | 2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ/mol | D. | C(s)+O2(g)═CO2(g)△H=+393.5 kJ/mol |
分析 A.热化学方程式中需要标出各物质的状态;
B.电解水为吸热反应,焓变值应该为正值;
C.氢气燃烧反应为放热反应,焓变为负值,结合热化学方程式的书写原则分析;
D.碳的燃烧为放热反应,焓变为负值.
解答 解:A.热化学方程式中应该标出各物质状态,正确的热化学方程式为:2SO2(g)+O2(g)═2SO3(g)△H=-196.6 kJ/mol,故A错误;
B.水的分解为吸热反应,焓变为正值,正确的热化学方程式为:2H2O(g)═2H2(g)+O2(g)△H=+483.6kJ/mol,故B错误;
C.氢气燃烧的热化学方程式为:2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ/mol,该热化学方程式满足书写原则,故C正确;
D.碳的燃烧为放热反应,焓变为负值,正确的热化学方程式为:C(s)+O2(g)═CO2(g)△H=-393.5 kJ/mol,故D错误;
故选C.
点评 本题考查了热化学方程式的书写方法判断,题目难度中等,明确热化学方程式的书写原则为解答关键,注意吸热反应、放热反应与焓变正负值的关系,试题培养了学生的规范答题能力.


 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
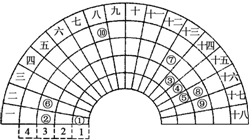 元素周期表的形式多种多样,下图是扇形元素周期表前四周期的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法正确的是( )
元素周期表的形式多种多样,下图是扇形元素周期表前四周期的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法正确的是( )| A. | ②、⑧、⑨对应原子半径依次增大 | |
| B. | ②、⑨的氢化物晶体类型相同 | |
| C. | 元素⑩处于常见周期表第四周期第VIIIB族 | |
| D. | ①、③、④、⑤形成的某种化合物中既含有共价键又含有离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
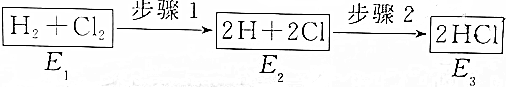
| A. | 步骤2是放热反应 | B. | 三个状态的能量E2最大 | ||
| C. | 要实现步骤1的转化,必须加热 | D. | 该反应放出的热量为E1一E3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com