
【题目】将等物质的量的A、B混合于2L的密闭容器中,发生下列反应:3A(g)+B(g)=xC(g)+2D(g)。经4min后测得D的浓度为0.5mol·L-1,c(A)∶c(B)=3∶5,C的平均反应速率为0.125mol·L-1·min-1,此时A的物质的量浓度减少了___,B的平均反应速率为___,x的值为___。
【答案】0.75mol·L-1 0.0625mol·L-1·min-1 2
【解析】
根据三段式,转化量与系数成比例关系,可得出4min时A的物质的量浓度减少量,根据![]() 或先求v(D),再根据v(B):v(D)=1:2,求得v(B),根据v(C): v(B)=x:1,求得x。
或先求v(D),再根据v(B):v(D)=1:2,求得v(B),根据v(C): v(B)=x:1,求得x。
由4min内D的浓度变化量为0.5molL1,设A、B的起始浓度为n,则可以得到下列关系: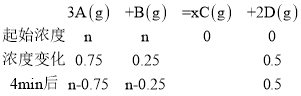
4min时A的物质的量浓度减少0.75molL1,由题意c(A):c(B)=(n0.75):(n0.25)=3:5,n=1.5 molL1;c(A)=(n0.75) molL1=0.75molL1,![]() =0.0625mol·L-1·min-1;v(C)=0.125mol·L-1·min-1,v(B)=0.0625mol·L-1·min-1,根据v(C):v(B)=x:1,求得x=2;
=0.0625mol·L-1·min-1;v(C)=0.125mol·L-1·min-1,v(B)=0.0625mol·L-1·min-1,根据v(C):v(B)=x:1,求得x=2;
故答案为:0.75mol·L-1 ;0.0625mol·L-1·min-1;2。


科目:高中化学 来源: 题型:
【题目】T℃时,向2L恒容密闭容器中充入1mol NO2与2mol SO2发生如下反应:NO2(g)+SO2(g) ![]() SO3(g)+NO(g)△H=﹣41.8kJ/mol。
SO3(g)+NO(g)△H=﹣41.8kJ/mol。
(1)下列能说明该反应达到平衡状态的是_____________。
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗n mol SO3的同时生成n mol NO2
(2)反应进行到20s 时,测得反应速率v(NO)=0.005mol/(Ls) , 则消耗的NO2为_____mol。
(3)下列措施能使反应加快的是___(仅改变一个条件)
a.降低温度 b.缩小容积 c.使用效率更高的催化剂
(4)若上述容器为绝热容器(与外界无热交换),则到达平衡所需时间将__________。
a.延长 b.缩短 c.不变 d.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙炔、乙烯均是重要的化工原料。回答下列问题:
(1)1902年,Sabatier首次发现,常压下过渡金属可以催化含有双键或叁键的气态烃的加氢反应。
①已知:C2H2(g)+H2(g)═C2H4(g)△H1=-174.3kJ·mol—1
K1(300K)=3.37×1024
C2H2(g)+2H2(g)=C2H6(g)△H2═-311.0kJ·mol一l
K2(300K)═1.19×1042
则反应C2H4(g)+H2(g)═C2H6(g)的△H=___kJ·mol一1,K(300K)=__(保留三位有效数字)。
②2010年Sheth等得出乙炔在Pd表面选择加氢的反应机理(如图)。其中吸附在Pd表面上的物种用*标注。
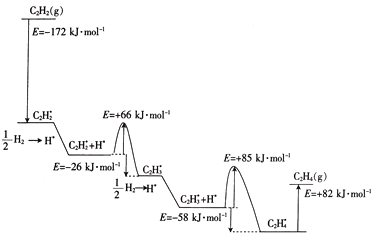
上述吸附反应为____(填“放热”或“吸热”)反应,该历程中最大能垒(活化能)为____kJ·mol-1,该步骤的化学方程式为____。
(2)在恒容密闭容器中充入乙烯,一定条件下发生反应C2H4(g)C2H2(g)+H2(g)。乙烯的离解率为a,平衡时容器内气体总压强为P总,则分压p(C2H4)═___(用p总和a表示)。
(3)用如图装置电解含CO2的某酸性废水溶液,阴极产物中含有乙烯。
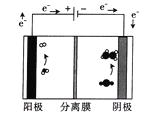
该分离膜为___(填“阳”或“阴”)离子选择性交换膜;生成乙烯的电极反应式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用如图所示装置进行化学反应X+2Y=2Z能量变化情况的研究。当向试管中滴加试剂Y时,观察到U形管中液面甲处下降、乙处上升。下列关于该反应的叙述正确的是( )
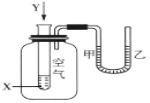
①该反应为放热反应
②该反应为吸热反应
③生成物的总能量比反应物的总能量高
④反应物的总能量比生成物的总能量高
⑤该反应过程可以看成贮存于X、Y内部的部分能量转化为热能而释放出来
A.仅①④⑤B.仅①④C.仅①③D.仅②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度、体积的密闭容器中,可逆反应A(s)+3B(g)![]() 2C(g)达到平衡时,下列说法能判断该反应达到平衡的是( )
2C(g)达到平衡时,下列说法能判断该反应达到平衡的是( )
①C的生成速率和C的分解速率相等
②单位时间内生成amolA,同时生成3amolB
③混合气体的密度不再变化
④混合气体的总压强不再变化
⑤A、B、C物质的量之比为1∶3∶2
⑥混合气体的平均相对分子质量不变
⑦容器中C的体积分数不变
A.②④⑤⑦B.①③④⑥⑦C.①④⑥⑦D.①③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】具有显著抗癌活性的10-羟基喜树碱的结构如图所示,

下列关于10-羟基喜树碱的说法正确的是
A. 10-羟基喜树碱属于芳香烃
B. 分子式为:C20H16N2O5
C. 不能发生酯化反应
D. 一定条件下,1mol该物质可与9molH2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“软电池”采用一张薄层纸片作为传导体,一面镀Zn,另一面镀MnO2。电池总反应为Zn+2MnO2+H2O=2MnO(OH)+ZnO。下列说法正确的是( )
A.该电池的正极为ZnO
B.Zn电极附近溶液的pH不变
C.电池正极的电极反应为2MnO2+2e-+2H2O=2MnO(OH)+2OH-
D.当0.1molZn完全溶解时,流经电解液的电子的物质的量为0.2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,对于密闭容器中进行的可逆反应A(g)+ 3B(g)![]() 2C(g), 下列说法能证明这一 反应已经达到化学平衡状态的是
2C(g), 下列说法能证明这一 反应已经达到化学平衡状态的是
A.生成C的速率与分解C的速率相等.
B.A. B、C的分子数之比为1:3:2
C.A、B、C的浓度相等
D.单位时间消耗nmolA,同时生成2nmolC
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com