
【题目】下列有关化学实验说法正确的是( )
A.用磨口玻璃塞的细口瓶盛放Na2CO3溶液
B.用酸式滴定管量取20.00 mL硫酸
C.电镀时,通常把镀层金属作阴极
D.中和反应反应热的测定实验中用到的所有玻璃仪器为烧杯、量筒、温度计
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案科目:高中化学 来源: 题型:
【题目】某消毒液的主要成分为NaClO,还含有一定量的NaOH,下列用来解释事实的方程式中不合理的是(已知:饱和NaClO溶液的pH约为11)( )
A. 该消毒液可用NaOH溶液吸收Cl2制备:Cl2 +2OH-=== Cl-+ ClO-+ H2O
B. 该消毒液的pH约为12:ClO-+ H2O![]() HClO+ OH-
HClO+ OH-
C. 该消毒液与洁厕灵(主要成分为HCl)混用,产生Cl2:2H++ Cl-+ ClO-= Cl2 ↑+ H2O
D. 该消毒液加白醋生成HClO,可增强漂白作用:CH3COOH+ ClO-= HClO+ CH3COO—
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】amL三种气态烃组成的混合物与足量氧气反应,恢复到原来的状态,体积共缩小2amL,则这三种烃可能是( )
A. CH4、C2H4、C3H4 B. C2H6、C3H6、C4H6 C. CH4、C2H6 C3H8 D. CH4、C2H4、C2H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由工业级碳酸锂(含有少量碳酸镁等杂质)制备高纯碳酸锂。实验过程如下:

(1)实验室中在右图所示装置中进行碳化反应:

① 碳化反应的主要反应离子方程式为__________。
② 碳化时温度需控制在 30℃,可采取的措施是_________。 温度不宜过高的原因是________。
(2)用 CO2调 pH 为 8~9,其目的是__________。
(3)已知在不同温度下蒸发分解碳酸锂的产率与溶解度关系如图:

90℃以下,随温度升高,碳酸锂产率升高的原因可能是__________。
(4)请补充完整由滤液制备高纯碳酸锂的实验方案:取滤液放置于烧杯中___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关金属的说法正确的是( )
A. 生铁与钢的区别在于生铁含碳杂质,而钢不含
B. 铜在自然界中的含量高,所以铜是人类最早使用的金属
C. 黑色金属材料包括铁、铬、锰及其化合物
D. 金属一般都具有导电性、导热性、延展性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知反应A(g)+B(g)![]() C(g)+D(g)的平衡常数和温度的关系如下:
C(g)+D(g)的平衡常数和温度的关系如下:
温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
请回答下列问题:
(1)该反应平衡常数表达式为K=_______;△H=_______0(选填“>”、“<”或“=”)。
(2)830℃时,向一个5L的密闭容器中充入0.40mol的A和0.60mol的B,反应在6min时达到平衡状态。
①该段时间内A的平均反应速率v(A)=__________,达到平衡时B的转化率为_________。
②如果这段时间内体系向外释放48kJ的热量,写出该反应的热化学方程式:_________。
③此时向该密闭容器中充入1mol氩气,平衡时A的转化率_______(选填“增大”、“减小”、“不变”)。
(3)判断该反应达到平衡的依据为_________(填正确选项的字母)。
a.压强不随时间改变 b.气体的密度不随时间改变
c.c(A)不随时间改变 d.单位时间里生成C和D的物质的量相等
e.单位时间内生成amolA的同时,消耗amolB
(4)1200℃时反应C(g)+D(g)![]() A(g)+B(g)的平衡常数的值为_________。
A(g)+B(g)的平衡常数的值为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室利用如图装置进行中和热的测定.回答下列问题: 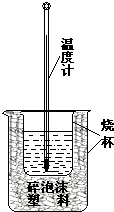
(1)如图装置中,为了酸碱能更充分地反应,应该增加一个(填玻璃仪器名称);大烧杯上没有盖上硬纸板,测得的中和热数值将会(填“偏大”、“偏小”或“无影响”).
(2)在操作正确的前提下提高中和热测定的准确性的关键是( 填代号)
A.进行实验时的气温
B.装置的保温隔热效果
C.实验所用酸碱溶液的体积
(3)如果用0.5 mol/L的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热”的数值将(填“偏大”、“偏小”、“不变”);原因是
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com