
【题目】硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组的同学欲测定该补血剂中铁元素的含量。实验步骤如下:
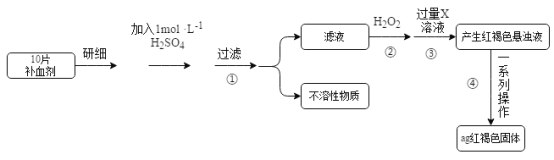
请回答下列问题:
(1)证明步骤①滤液中含有Fe2+的方法是取样,先滴加KSCN溶液,再滴加_____,该过程的现象为________。
(2)步骤②加入过量H2O2的目的是________。
(3)步骤③中反应的离子方程式是_________。
(4)步骤④中一系列处理的操作步骤:过滤、_____、灼烧、冷却、称量。
(5)若实验中铁无损耗,则每片补血剂中含铁元素的质量为_______g。
【答案】氯水(或双氧水、稀硝酸等合理氧化剂) 溶液由浅绿色变为红色 将Fe2+全部氧化为Fe3+ Fe3++3OH-=Fe(OH)3↓[或Fe3++3NH3·H2O=Fe(OH)3↓+3NH4+] 洗涤 0.07a
【解析】
(1)Fe3+遇KSCN溶液变红色,氯水、双氧水、稀硝酸等氧化剂能把Fe2+氧化为Fe2+;
(2)H2O2具有氧化性,能将Fe2+全部氧化为Fe3+;
(3)步骤③加入X的目的是生成氢氧化铁沉淀,所以X可以是氢氧化钠;
(4)从溶液中分离出固体沉淀的操作是过滤、洗涤;
(5)ag红棕色固体是氧化铁,根据氧化铁的质量计算铁元素的质量。
(1)证明步骤①滤液中含有Fe2+的方法是取样,先滴加KSCN溶液,再滴加氯水(或双氧水、稀硝酸等),若滤液由浅绿色变为红色,则说明滤液中含有Fe2+。
(2)由于H2O2具有氧化性,加入过量H2O2的目的是将Fe2+全部氧化为Fe3+;
(3)步骤③加入氢氧化钠,反应的离子方程式是Fe3++3OH-=Fe(OH)3↓;
(4)步骤④是分离出氢氧化铁沉淀并得到纯净的氧化铁,一系列处理的操作步骤:过滤、洗涤、灼烧、冷却、称量;
(5)ag红棕色固体是氧化铁,氧化铁中铁元素的质量是![]() ,则每片补血剂中含铁元素的质量为
,则每片补血剂中含铁元素的质量为![]() 。
。


科目:高中化学 来源: 题型:
【题目】有甲、乙两个完全相同的装置,分别在它们的侧管中装入1.06g Na2CO3和0.84g NaHCO3,试管中各有10mL相同浓度的盐酸(如图),同时将两个侧管中的物质全部倒入各自的试管中,下列叙述正确的是
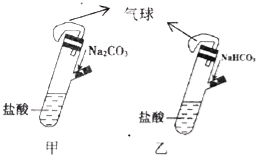
A. 甲装置的气球膨胀速率大
B. 若最终两气球体积相同,则一定有c(HCl)≥2 mol/L
C. 若最终两气球体积不同,则一定有c(HCl)≤1 mol/L
D. 最终两溶液中Na+、Cl﹣的物质的量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚(CH3OCH3)和甲醇(CH3OH)被称为21世纪的新型燃料,具有清洁、高效等优良的性能。以CH4和H2O为原料制备二甲醚和甲醇的工业流程如图:
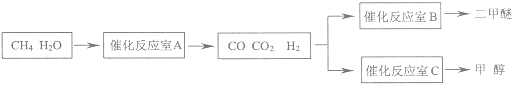
(1)催化反应室B中CO与H2合成二甲醚的化学方程式为___。
(2)催化反应室A中发生的反应为:
CH4(g)+H2O(g)![]() CO(g)+3H2(g)……(Ⅰ)
CO(g)+3H2(g)……(Ⅰ)
CO(g)+H2O(g)![]() CO2(g)+H2(g)……(Ⅱ)
CO2(g)+H2(g)……(Ⅱ)
催化反应室C中发生的反应为:
CO(g)+2H2(g)![]() CH3OH(g)……(Ⅲ)
CH3OH(g)……(Ⅲ)
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)……(Ⅳ)
CH3OH(g)+H2O(g)……(Ⅳ)
①已知:原子利用率=![]() ×100%。试求反应(Ⅳ)的原子利用率为___。
×100%。试求反应(Ⅳ)的原子利用率为___。
②反应(Ⅳ)的△S___0(填“>”、“=”或“<”)。
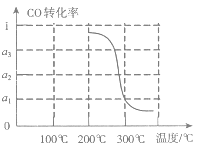
③在压强为5MPa,体积为V L的反应室c中,a mol CO与2a mol H2在催化剂作用下发生反应(Ⅲ)生成甲醇,CO的转化率与温度的关系如图。则该反应的△H___0(填“>”、“=”或“<”)。300℃时该反应的平衡常数K=___(用含字母的代数式表示)。
(3)我国某科研所提供一种碱性“直接二甲醚燃料电池”。该燃料电池负极的电极反应式为:CH3OCH3-12e-+16OH-=2CO32-+11H2O。有人提出了一种利用氯碱工业产品治理含二氧化硫(体积分数为x)废气的方法如下:
①将含SO2的废气通入电解饱和食盐水所得溶液中,得NaHSO3溶液;
②将电解饱和食盐水所得气体反应后制得盐酸;
③将盐酸加入 NaHSO3溶液中得SO2气体回收。
用上述碱性“直接二甲醚燃料电池”电解食盐水来处理标准状况下V L的废气,计算消耗二甲醚的质量___。(写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数,下列叙述正确的是( )
A. 标准状况下,1molFe分别与足量的盐酸和水蒸气反应转移的电子数均为2NA
B. 11.2LH2中含有的原子数为NA
C. Na2O与Na2O2的混合物共1mol,阴离子数目为NA
D. 1.0L1mol/L的Na2SO4水溶液中含有的氧原子数目为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图①—⑩分别代表有关反应中的一种物质,其中③气体能使酚酞试液变红,⑦是红综色气体,回答:

(1)①中的混合气体通过浓硫酸发生化学反应,主要生成物的化学式是____。
(2)写出碳酸氢铵中阳离子的检验方法______________________________。
(3)写出工业上合成③的化学方程式__________________________________。
(4)⑧与⑨反应的化学方程式是______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某气态烃A的产量可以用来衡量一个国家的石油化工发展水平。B和D都是生活中常见的有机物,D能跟碳酸氢钠反应,F有香味。它们之间的转化关系如图所示:
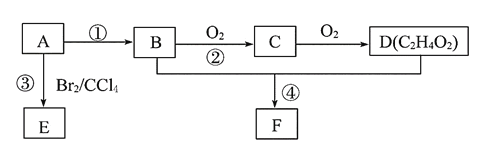
(1)A的结构式为______,D中官能团的名称为_____。
(2)反应③的化学方程式为___________。
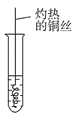
(3)反应②在Cu做催化剂的条件下进行,该实验的步骤是将红亮的铜丝置于酒精灯上加热,待铜丝变为黑色时,迅速将其插入到装有B的试管中(如图所示)。重复操作2~3次。该反应的化学方程式为___________。
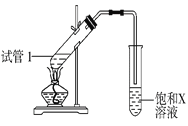
(4)B、D在浓硫酸的作用下实现反应④,实验装置如图所示,试管1中装入药品后加热。图中X的化学式为______。试管1中反应的化学方程式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠、钾与水反应的实验如下图所示:

(1)钠、钾与水反应两个实验现象的相同点:
①金属________水面上;
②金属________成闪亮的小球;
③小球四处游动;
④产生嘶嘶的声音;
⑤反应后的溶液使酚酞________。
(2)_______与水反应有轻微的爆鸣声,并很快燃烧起来。
(3)实验结论:________更易与水反应,且反应更_____________________________________。
(4)钾与水反应的化学方程式是___________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z在元素周期表中的相对位置如表所示,这四种元素的原子最外层电子数之和为21。下列说法不正确的是

A.W、Y两种元素都能与氧元素形成化合物WO2、YO2
B.原子半径大小:Y<X
C.W元素的单质能从X的某种化合物中置换出X单质
D.氧化物对应水化物的酸性:W<Y<Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是硫酸试剂瓶标签上的内容。请回答下列问题:
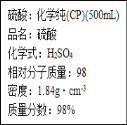
(1)该硫酸的物质的量浓度为____;
(2)实验室用该硫酸配制240mL0.46 mol·L-1的稀硫酸,则
①需要用量筒量取该硫酸的体积为_____mL;
②实验所用到的玻璃仪器除烧杯、玻璃棒外,还有_____;
③该同学实际配制得到的浓度为0.45 mol·L-1,可能的原因是_______。
A.量取浓H2SO4时仰视刻度 B.容量瓶洗净后未经干燥处理
C.没有将洗涤液转入容量瓶 D.定容时仰视刻度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com