
【题目】含硫化合物的种类很多,分类依据也很多。![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 是七种常见的含硫化合物。某同学按以下思路进行探究:
是七种常见的含硫化合物。某同学按以下思路进行探究:
(1)分类:若按酸、碱、盐、氧化物进行分类,则七种物质中属于盐的共有______种;若将硫元素化合价相同的物质分为一类,则这七种物质可分为______类。
(2)完成下列含硫化合物间的转化,写出相应的化学方程式(试剂可任选)。
![]() :______。
:______。
![]() :______。
:______。
![]() :______。
:______。
(3)为减少![]() 的污染并变废为宝,我国正在探索在一定条件下用
的污染并变废为宝,我国正在探索在一定条件下用![]() 还原
还原![]() 得到单质硫的方法来除去
得到单质硫的方法来除去![]() 。该反应的化学方程式为____________。
。该反应的化学方程式为____________。
【答案】4 3 ![]()
![]()
![]() (浓)
(浓)![]()

【解析】
(1)盐是在水溶液里能够电离出金属阳离子(或NH4+)和酸根离子,属于盐的是Na2SO3、BaSO4、FeS、CuSO4;S的化合价有-2价、+4价、+6价,据此分析;
(2)根据硫及其化合物的性质进行分析;
(3)CO还原SO2得到S单质,S的化合价降低,C的化合价升高,被氧化成CO2,据此分析;
(1)若按酸、碱、盐、氧化物进行分类.依据物质组成分析,属于酸的是![]() 、
、![]() ;属于盐的是
;属于盐的是![]() 、
、![]() 、
、![]() 、
、![]() ;属于氧化物的是
;属于氧化物的是![]() ;硫元素显
;硫元素显![]() 价的是
价的是![]() 、
、![]() 、
、![]() ,显
,显![]() 价的是
价的是![]() 、
、![]() ,显
,显![]() 价的是
价的是![]() 、
、![]() ;
;
(2)硫化亚铁和稀硫酸反应生成硫化氢,反应的化学方程式为![]() ;二氧化硫和足量氢氧化钠溶液反应生成亚硫酸钠,反应的化学方程式为
;二氧化硫和足量氢氧化钠溶液反应生成亚硫酸钠,反应的化学方程式为![]() ;浓硫酸和碳在加热条件下反应生成二氧化硫气体,反应的化学方程式为C+2H2SO4(浓)
;浓硫酸和碳在加热条件下反应生成二氧化硫气体,反应的化学方程式为C+2H2SO4(浓) ![]() CO2↑+2H2O+2SO2↑;
CO2↑+2H2O+2SO2↑;
(3)用![]() 还原
还原![]() 得到单质硫,则
得到单质硫,则![]() 被氧化成
被氧化成![]() ,发生反应的化学方程式为
,发生反应的化学方程式为 。
。


科目:高中化学 来源: 题型:
【题目】同学们在实验室里用不同的方法分别制取Cu(NO3)2,并在此基础上探究Cu(NO3)2的化学性质。
(1)甲组同学直接用铜屑与稀硝酸反应制取Cu(NO3)2,反应的化学方程式是_____________。
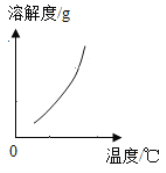
(2)乙组同学查阅了硝酸铜晶体的溶解度曲线(右图),据此设计了以下实验方案,先将铜粉在空气中充分灼烧,再将灼烧后的物质与适量稀HNO3反应,欲从反应后的溶液中得到Cu(NO3)2晶体,依次进行的操作是:蒸发浓缩、____________、过滤、洗涤、干燥。乙组同学认为此方案优于甲组的方案,理由之一是__________________________。
(3)丙组同学用Cu(NO3)2晶体,探究其热稳定性,实验装置如下所示。(夹持装置和加热仪器未画出)

①充分加热Cu(NO3)2晶体一段时间后,观察到U形管中气体变为红棕色,红棕色气体是____________。
②集气瓶最终被水充满,无气体剩余,则晶体分解的生成的气体还有________。
③欲证明试管中残留的黑色粉末是CuO[假设Cu(NO3)2晶体已全部分解],实验方案是 _________。
④由该实验可得出的结论是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列问题:
(1)氮和磷氢化物热稳定性的比较:NH3______PH3(填“>”或“<”)。
(2)PH3和NH3与卤化氢的反应相似,产物的结构和性质也相似。下列对PH3与HI反应产物的推断正确的是_________(填序号)。
a.不能与NaOH反应 b.含离子键、共价键 c.受热可分解
(3)已知H2与O2反应放热,断开1 mol H-H键、1 mol O=O键、1 mol O-H键所需要吸收的能量分别为Q1 kJ、Q2 kJ、Q3 kJ,由此可以推知下列关系正确的是______。
①Q1+Q2>Q3 ②2Q1+Q2<4Q3 ③2Q1+Q2<2Q3
(4)高铁电池总反应为:3Zn+2K2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4KOH,写出电池的正极反应:__________,负极反应 ________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2,已知该反应中H2O2只发生如下过程:H2O2→O2。
(1)该反应中的还原剂是____________。
(2)该反应中,发生还原反应的过程是____________→____________。
(3)写出该反应的化学方程式,并标出电子转移的方向和数目____________。
(4)如反应转移了0.3 mol电子,则产生的气体在标准状况下体积为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A+B→C △H <0,分两步进行 ① A+B→X △H>0 ② X→C △H<0 。下列示意图中,能正确表示总反应过程中能量变化的是
A.  B.
B. 
C.  D.
D. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于金属腐蚀与防护的说法不正确的是
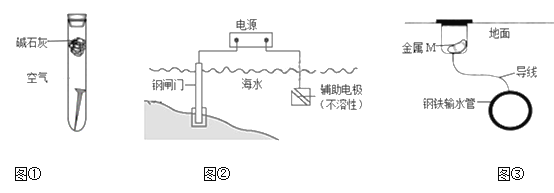
A. 图①,放置于干燥空气中的铁钉不易生锈
B. 图②,若将钢闸门与电源的正极相连,可防止钢闸门腐蚀
C. 图②,若断开电源,钢闸门将发生吸氧腐蚀
D. 图③,若金属M比Fe活泼,可防止输水管腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构见下图,电池总反应可表示为:2H2+O2=2H2O,下列有关说法正确的是
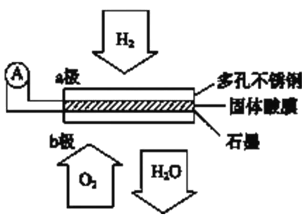
A. 电子通过外电路从b极流向a极
B. b极上的电极反应式为:O2+2H2O+4e--=4OH--
C. 每转移0.1mol电子,消耗1.12L的H2
D. H+由a极通过固体酸电解质传递到b极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业制HNO3的过程中排放的NO2和NO常用NaOH溶液吸收,反应的化学方程式为NO+NO2+2NaOH=2NaNO2+H2O、2NO2+2NaOH=NaNO2+NaNO3+H2O,NO不能被NaOH溶液吸收。若同温同压下NO2与NO的体积之比如下,其中不能被NaOH溶液完全吸收的是( )
A.1:1B.1:3C.2:1D.3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,1mol化学键断裂形成气态原子所需要的能量用![]() 表示。结合表中信息判断下列说法不正确的是( )
表示。结合表中信息判断下列说法不正确的是( )
共价键 | H-H | F-F | H-F | H-Cl | H-I |
E(kJ/mol) | 436 | 157 | 568 | 432 | 298 |
A. 432kJ/mol>E(H-Br)>298kJ/mol B. 表中最稳定的共价键是H-F键
C. H2(g)→2H(g) △H=+436kJ/mol D. H2(g)+F2(g)=2HF(g) △H=-25kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com