
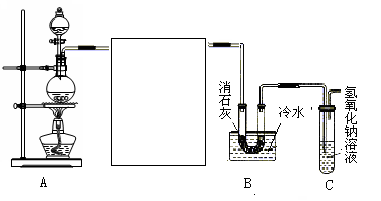
 Mn2+ + Cl2↑+ 2H2O
Mn2+ + Cl2↑+ 2H2O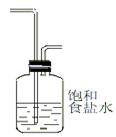
 Mn2+ + Cl2↑+ 2H2O。
Mn2+ + Cl2↑+ 2H2O。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
| A.①③④⑤⑥⑦⑧ | B.②③⑤⑥⑦⑧⑨ |
| C.①②③⑤⑥⑦⑨ | D.①②③④⑤⑥⑨ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
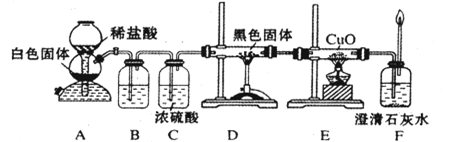
 2CaSO4+2Cl2↑+2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。
2CaSO4+2Cl2↑+2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。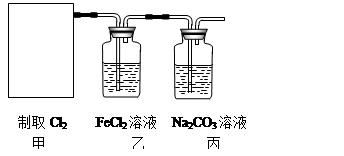
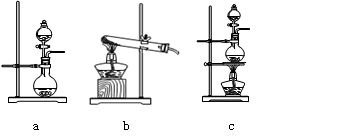
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 CO+H2 CO + H2O
CO+H2 CO + H2O CO2 + H2 C + CO2
CO2 + H2 C + CO2 2CO
2CO 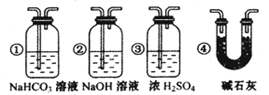
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
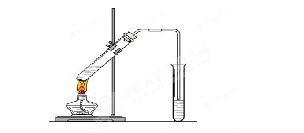
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
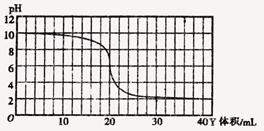
| A.X和Y可能是KOH和CH3COOH |
| B.X和Y可能是NH3·H2O和HCl |
| C.X与Y恰好中和时, 混合液呈中性 |
| D.X与Y恰好完全反应时的溶液中滴入酚酞会变色 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

| 分项 内容 | CO2发生装置(X) 随开随用,随关随停 | 除杂洗气装置(Y) | 制备产品装置(Z) |
| 选择的装置(填序号) | | | C |
| 选择的药品(填序号) | | | ① |
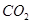 发生装置(X)的气密性,请写出主要操作过程:
发生装置(X)的气密性,请写出主要操作过程: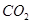 气体,其原因是_________________;通入过量
气体,其原因是_________________;通入过量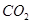 后,Z装置内的溶液中离子浓度大小顺序为:_______________________ 。
后,Z装置内的溶液中离子浓度大小顺序为:_______________________ 。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 SiHCl3 + H2(g)
SiHCl3 + H2(g) Si(s)+ 3HCl(g)
Si(s)+ 3HCl(g)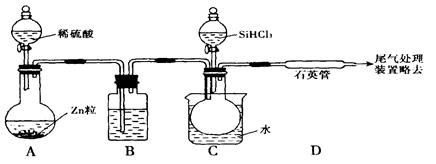
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com