
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
某有机物的结构为下图所示,这种有机物不可能具有的性质是( )
①可以燃烧; ②能使酸性KMnO4溶液褪色;
③能跟NaOH溶液反应; ④能发生酯化反应;
⑤能发生加聚反应; ⑥能发生水解反应
A.①④ B.只有⑥ C.只有⑤ D.④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)淀粉的化学式是 ;玻璃、陶瓷、水泥一定含 元素。造成赤潮的主要元素
是 ;油脂在体内水解后的产物是 和高级脂肪酸。
(2)常见的塑料有两类,一类是 塑料,如聚乙烯,一类是 塑料,如酚醛树脂等。
硫化后的橡胶适合制造汽车轮胎,加入 可增强轮胎的耐磨性。
(3)在“棉花、尼龙、黏胶纤维、蚕丝”这四中纤维中,属于天然纤维的是 ;属于
人造纤维的是 ;属于合成纤维的是 。
(4)药品标签上应贴有 “OTC”或“R”符号,①“OTC”它表示 ,②“R”表示 ,
氢氧化铝和碳酸氢钠都可用作抗胃酸药。写出:
③氢氧化铝与胃酸作用的离子方程式: ;
④碳酸氢钠与胃酸作用的化学方程式: 。
(5)一个体重50kg的健康人,体内约含有2g铁,这2g铁在人体内不是以单质的形式存在,而
是以Fe2+ 和Fe3+的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+
的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的Fe3+还原成Fe2+,有利于人体吸收。
①往KMnO4溶液中滴入维生素C溶液,KMnO4溶液褪色说明维生素C具有 性,
②人体长期缺乏维生素C会引起 病,
③市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸的作用下
转化成亚铁盐。此反应的离子方程式为
(6)我国城市为了减少燃煤造成的大气污染,对民用燃料的煤作了多方面的改进。
①绿色能源是人类的理想能源不会造成环境污染,下列能源不属于绿色能源的是
A.氢能源 B.太阳能 C.风能 D.石油
②为了除去煤中的含硫化合物,采用FeCl3脱硫,即用FeCl3溶液浸洗煤粉,发生如下反
应:FeS2+14FeCl3+8H2O===2FeSO4+13FeCl2+16HCl 该反应中的氧化剂是 ;
为了充分利用Fe2+并减少酸(HCl)污染,本方法中可利用工业废铁屑和氯气让废液重新
利用生成FeCl3。请写出这一过程中有关的离子方程式:
、 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知常温下,AgBr的Ksp=4.9×10-13 mol2·L-2、AgI的Ksp=8.3×10-17 mol2·L-2 下列说法正确的是:
A、在常温下AgI水溶液中,Ag+和I-浓度的乘积是一个常数
B在常温下,在任何含AgI固体的溶液中,c(Ag+)=c(I-)且Ag+与I-浓度的乘积等于8.3×10-17 mol2·L-2
C常温下,将1mL 1.0×10-2 mol/L的KI与AgNO3溶液等体积混合,则生成AgI沉淀所需AgNO3溶液的最小浓度为3.32×10-14 mol/L
D、向AgI饱和溶液中加入AgBr固体,c(I-)不变,Ksp值不变
查看答案和解析>>
科目:高中化学 来源: 题型:
I、回答下列问题
1)、已知常温下,在NaHSO3溶液中c(H2SO3 ) < c(SO32 -) ,且H2SO3 的电离平衡常数为K1=1.5×10-2 K2=1.1×10-7 ;氨水的电离平衡常数为K=1.8×10-2 ;
则等物质的量浓度的下列五种溶液:①NH3·H2O ②(NH4)2CO3 ③KHSO3 ④KHCO3 ⑤Ba(OH)2,溶液中水的电离程度由大到小排列顺序为_____________
2)、NaHSO3具有较强还原性可以将碘盐中的KIO3氧化为单质碘,试写出此反应的离子反应方程式_______________________________________
3)、在浓NH4Cl溶液中加入镁单质,会产生气体,该气体成分是_________________,用离子方程式表示产生上述现象的原因:__________________
II、已知25 ℃时Ksp[Mg(OH)2]=5.6×10-12,Ksp[Cu(OH)2]=2.2×10-20,
Ksp[Fe(OH)3]=4.0×10-38,Ksp[Al(OH)3]=1.1×10-33
(1)①在25 ℃下,向浓度均为0.1 mol·L-1的AlCl3和CuCl2混合溶液中逐滴加入氨水,先生成________沉淀(填化学式)。
②用MgCl2、AlCl3的混合溶液(A) 与过量氨水(B) 反应,为使Mg2+、Al3+同时生成沉淀,应先向沉淀反应器中加入________(填“A”或“B”),再滴加另一反应物。
(2)溶液中某离子物质的量浓度低于1.0×10-5 mol·L-1时,可认为已沉淀完全。现向一定浓度的AlCl3和FeCl3的混合溶液中逐滴加入氨水,当Fe3+完全沉淀时,测定c(Al3+)=0.2 mol·L-1。此时所得沉淀中________(填“还含有”或“不含有”)Al(OH)3。请写出计算过程_____________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
下列推断正确的是
A.SO2和CO2都是酸性氧化物,都能与NaOH溶液反应
B.Na2O和Na2O2组成元素相同,与CO2反应产物也完全相同
C.NO和NO2的密度都比空气大,都可以用向上排空气法收集
D.C3H8和CH3CH2OH相对分子质量相近,二者沸点也相近
查看答案和解析>>
科目:高中化学 来源: 题型:
未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。下列属于未来新能源标准的是
①天然气 ②煤 ③核能 ④石油 ⑤太阳能 ⑥生物质能 ⑦风能 ⑧氢能
A.①②③④ B.⑤⑥⑦⑧
C.③⑤⑥⑦⑧ D.③④⑤⑥⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
①已知t℃时AgCI的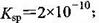 ;②在t℃时Ag2CrO4
;②在t℃时Ag2CrO4
在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
A.在t℃时,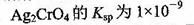
B.在饱和Ag2CrO4溶液中加入K2CrO4可使溶液由Y点到
X点
C.在t℃时,以0.01 mol/LAgNO3溶液滴定20 mL 0.01 mol/L
KCI和0.01 mol/L的K2CrO4的混和溶液,CrO42-先沉淀
D.在t℃时,反应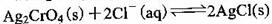
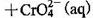 的平衡常数
的平衡常数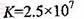
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com