
 经测定乙醇的化学式是C2H6O,由于有机物普遍存在同分异构现象,推测乙醇的结构可能是下列二种之一.
经测定乙醇的化学式是C2H6O,由于有机物普遍存在同分异构现象,推测乙醇的结构可能是下列二种之一. (Ⅱ)
(Ⅱ)
| 乙醇的物质的量(mol) | 氢气的体积(L) | 0.10 | 1.12(标准状况) |
| 1 |
| 2 |


 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:阅读理解

为测定其结构,应利用物质的特殊性进行定性、定量实验,现给出乙醇、钠、水及必要的仪器,请甲、乙、丙、丁四同学直接利用下图给定装置开始进行实验确定乙醇的结构。
(1)学生甲得到一组实验数据:
乙醇的物质的量/mol | 氢气的体积/L |
0.10 | 1.12(标准状况) |
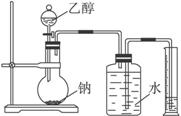
根据以上数据推断乙醇的结构应为________(用Ⅰ、Ⅱ表示),理由为____________________。
(2)同学乙分别准确称量
(3)同学丙认为实验成功的关键有:①装置气密性要良好 ②实验开始前准确确定乙醇的量 ③钠足量 ④广口瓶内水必须充满 ⑤氢气体积的测算方法正确、数据准确。其中正确的有__________。(填序号)
(4)同学丁不想通过称量乙醇的质量来确定乙醇的量,那么他还需知道的数据是__________。
(5)实验后,四名同学从乙醇的可能结构分析入手对乙醇和钠的量的关系进行了讨论,如果乙醇的物质的量为n mol,那么对钠的物质的量的取值要求必须是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(12分)经测定乙醇的化学式是C2H6O,由于有机物普遍存在同分异构现象,推测乙醇的结构可能是下列两种之一。
为测定其结构,应利用物质的特殊性进行定性、定量实验。现给出乙醇、钠、水及必要的仪器,请甲、乙两位同学直接利用如图给定装置开始进行实验确定乙醇的结构。
(1)学生甲得到一组实验数据如上表:
| 乙醇的物质的量/mol | 氢气的体积/L |
| 0.10 | 1.12(标准状况) |
根据以上数据推断乙醇的结构为 (用Ⅰ、Ⅱ表示),理由为
,
该反应的化学方程式为: 。
(2)同学乙分别准确称量4.60 g 乙醇进行多次实验,结果发现以排在量筒内水的体积作为生成的H2体积,换算成标准状况后都小于1.12L,如果忽略量筒本身及乙同学读数造成的误差,那么乙认为可能是由于样品中含有少量水造成的,你认为正确吗? (填“正确”或“不正确”)。请说明你判断的理由 。
(3)实验后,两名同学从乙醇的可能结构分析入手,对乙醇和钠的量的关系进行了讨论,如果乙醇的物质的量为n mol,那么对钠的物质的量的取值要求必须是 n(填“大于”、“小于”或“等于”)。
查看答案和解析>>
科目:高中化学 来源:2010年福建省南安一中高一下学期期末考试化学试卷 题型:填空题
(12分)经测定乙醇的化学式是C2H6O,由于有机物普遍存在同分异构现象,推测乙醇的结构可能是下列两种之一。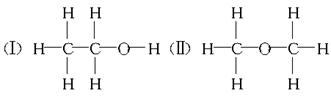
为测定其结构,应利用物质的特殊性进行定性、定量实验。现给出乙醇、钠、水及必要的仪器,请甲、乙两位同学直接利用如图给定装置开始进行实验确定乙醇的结构。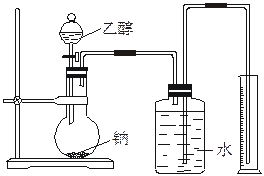
(1)学生甲得到一组实验数据如上表:
| 乙醇的物质的量/mol | 氢气的体积/L |
| 0.10 | 1.12(标准状况) |
查看答案和解析>>
科目:高中化学 来源:2010年福建省高一下学期期末考试化学试卷 题型:填空题
(12分)经测定乙醇的化学式是C2H6O,由于有机物普遍存在同分异构现象,推测乙醇的结构可能是下列两种之一。
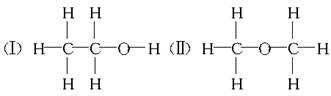
为测定其结构,应利用物质的特殊性进行定性、定量实验。现给出乙醇、钠、水及必要的仪器,请甲、乙两位同学直接利用如图给定装置开始进行实验确定乙醇的结构。

(1)学生甲得到一组实验数据如上表:
|
乙醇的物质的量/mol |
氢气的体积/L |
|
0.10 |
1.12(标准状况) |
根据以上数据推断乙醇的结构为 (用Ⅰ、Ⅱ表示),理由为
,
该反应的化学方程式为: 。
(2)同学乙分别准确称量4.60 g 乙醇进行多次实验,结果发现以排在量筒内水的体积作为生成的H2体积,换算成标准状况后都小于1.12L,如果忽略量筒本身及乙同学读数造成的误差,那么乙认为可能是由于样品中含有少量水造成的,你认为正确吗? (填“正确”或“不正确”)。请说明你判断的理由 。
(3)实验后,两名同学从乙醇的可能结构分析入手,对乙醇和钠的量的关系进行了讨论,如果乙醇的物质的量为n mol,那么对钠的物质的量的取值要求必须是 n(填“大于”、“小于”或“等于”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com